Вариант № 603
1.На трёх электронных слоях размещаются все электроны в атомах каждого из двух химических элементов:
1)  и
и  2)
2)  и
и  3)
3) 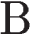 и
и  4)
4) 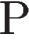 и
и 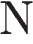
2.Какой из элементов 2-го периода имеет наибольшую электроотрицательность?
1)  2)
2)  3)
3)  4)
4) 
3.Какой вид химической связи в оксиде хлора(VII)?
1) ковалентная полярная 2) ионная
3) ковалентная неполярная 4) металлическая
4.В каком соединении фосфор имеет наивысшую степень окисления?
1) 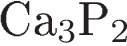 2)
2)  3)
3) 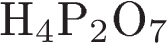 4)
4) 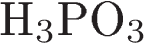
5.Медь реагирует с
1) разбавленной  2) разбавленной
2) разбавленной 
3) раствором  4) раствором
4) раствором 
6.Взаимодействие раствора сульфата меди(II) с железом относится к реакциям
1) замещения 2) соединения 3) обмена 4) разложения
7.При диссоциации какой соли образуется больше положительных ионов, чем отрицательных?
1)  2)
2) 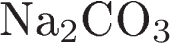 3)
3)  4)
4) 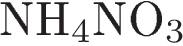
8.Взаимодействию гидроксида меди(II) с раствором серной кислоты соответствует сокращённое ионное уравнение
1) 
2)
3)
4)
9.Водород вступает в реакцию с
1)  2) 3)
2) 3)  4)
4) 
10. Оксид цинка реагирует с каждым из двух веществ:
1) 2)
3) 4)
11. Среди веществ, формулы которых: реагируют с гидроксидом натрия
1) только  2)
2)  и
и
3) и  4) все приведённые вещества
4) все приведённые вещества
12. С раствором сульфата меди (II) реагирует
1) 2)  3) 4)
3) 4)
13.Верны ли следующие утверждения о правилах работы в школьной лаборатории?
А. Все опыты, проводимые в лаборатории, должны быть записаны в лабораторный журнал.
Б. При нагревании жидких и твёрдых веществ в пробирках и колбах нельзя направлять их отверстия на себя и соседей.
1) верно только А 2) верно только Б
3) верны оба утверждения 4) оба утверждения неверны
14.Элемент кремний является окислителем в реакции
1) 2)
3) 4)
15.Массовая доля кислорода в нитратe железа(III) равна
1) 59,5% 2) 6,6% 3) 16,0% 4) 56,1%
16.Для ряда химических элементов кремний → алюминий → магний → натрий характерны следующие закономерности:
1) увеличивается число электронных слоев в атоме
2) увеличивается радиус атома
3) уменьшается относительная атомная масса
4) увеличивается высшая степень окисления
5) уменьшается восстановительная способность
17.Свойства этилена:
1) хорошо растворим в воде
2) при обычных условиях представляет собой твёрдое вещество
3) молекула содержит двойную связь
4) является сильным окислителем
5) вступает в реакции присоединения
18.На рисунке изображён способ получения
1) сернистого газа 2) водорода 3) аммиака 4) хлороводорода
19.Установите соответствие между исходными веществами и продуктами реакции.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| A) | 1) |
| Б) | 2) |
| B) | 3) |
|
| 4) |
|
| 5) |
20.Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
Определите окислитель и восстановитель
21.К 300 г баритовой воды добавили избыток раствора карбоната натрия, выпал осадок массой 11,82 г. Определите массовую долю гидроксида бария в исходном растворе.
22.Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращенное ионное уравнение реакции.
Вариант №607
1.
Схема строения электронных оболочек соответствует атому химического элемента
1) 2-го периода VIIA группы 2) 5-го периода VIIA группы
3) 2-го периода VA группы 4) 5-го периода IIА группы
2.Кислотные свойства высших оксидов ослабевают в ряду:
1) 2)
3) 4)
3.Ионная химическая связь реализуется в
1) хлороводороде 2) гидроксиде натрия
3) оксиде углерода(II) 4) оксиде углерода(IV)
4.Максимально возможную степень окисления атом серы проявляет в соединении
1)  2)
2)  3) 4)
3) 4) 
5.Ангидридом кислоты  является
является
1)  2) 3) 4)
2) 3) 4)
6.К окислительно-восстановительным относится реакция термического разложения
1) 2) 3) 4)
7.Одинаковое количество катионов и анионов образуется при полной диссоциации
1) 2) 3)  4)
4)
8.Сокращенному ионному уравнению соответствует взаимодействие веществ
1) и 2) и
3)  и 4)
и 4)  и
и 
9.Возможно химическое взаимодействие между следующими веществами:
1)  и
и  2)
2)  и
и  3)
3)  и
и  4)
4)  и
и 
10. Оксид железа(II) взаимодействует с раствором
1) аммиака 2) бромоводорода 3) карбоната калия 4) хлорида натрия
11.Раствор гидроксида калия может реагировать с каждым из веществ:
1) 2) 3) 4)
12.Каждая из трёх солей — и  — реагирует с
— реагирует с
1) медью 2) азотной кислотой 3) хлоридом кальция
4) гидроксидом калия
13.Верны ли следующие утверждения о правилах безопасной работы в школьной лаборатории?
А. Чтобы погасить пламя спиртовки, его следует задуть.
Б. При нагревании пробирки с раствором её следует располагать строго вертикально.
1) верно только А 2) верно только Б
3) верны оба утверждения 4) оба утверждения неверны
14.Установите соответствие между схемой окислительно-восстановительной реакции и степенью окисления окислителя в ней.
| СХЕМА РЕАКЦИИ | СТЕПЕНЬ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ |
| A) | 1) 0 |
| Б) | 2) −2 |
| B) | 3) +2 |
|
| 4) −4 |
|
| 5) +4 |
15.Массовая доля кислорода в сульфате железа(III) равна
1) 4,0% 2) 16,0% 3) 48,0% 4) 56,2%
16.Ослабление кислотных свойств высших оксидов происходит в рядах:
1) 2)
3) 4)
5)
17.Для этанола верны следующие утверждения:
1) в состав молекулы входит один атом углерода
2) атомы углерода в молекуле соединены двойной связью
3) является жидкостью (н.у.), хорошо растворимой в воде
4) вступает в реакцию со щелочными металлами
5) сгорает с образованием угарного газа и водорода
18.
В приборе, изображённом на рисунке, нельзя получить и собрать
1) азот
2) кислород
3) хлороводород
4) метан
19.Установите соответствие между названием вещества и реагентами, с каждым из которых это вещество может взаимодействовать
| НАЗВАНИЕ ВЕЩЕСТВА | | РЕАГЕНТЫ |
| А) углерод Б) гидроксид калия В) хлорид алюминия | | 1) 2) 3) 4) 5) |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
20.Используя метод электронного баланса, составьте уравнение реакции:
Определите окислитель и восстановитель.
21.Через раствор гидроксида натрия пропустили 4,48 л сернистого газа. Образовалось 126 г раствора сульфита натрия. Вычислите массовую долю соли в полученном растворе.
22.Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для последней реакции составьте сокращённое ионное уравнение.
























