

Теория радикалов
(30 гг. XIX в Й.Берцелиус , Ю.Либих, Ж.Дюма)
- В состав органических веществ входят радикалы;
- Радикалы всегда постоянны, не подвергаются изменениям, переходят из одной молекулы в другую;
- Радикалы могут существовать в свободном виде.
Понятие «радикал» прочно вошло в химию

Теория типов
(40-50 гг. XIX в. Ш.Жерар, А.Кекуле и др.)
- Все органические вещества – производные простейших неорганических – типа водорода, воды, аммиака и др.
- Формулы выражают не внутреннее строение молекулы, а способы образования, свойства определяют все атомы молекулы;
- Невозможно познать строение вещества, у каждого вещества столько формул, сколько его превращений существует.
Теория позволила классифицировать орг. Вещества, предсказать и открыть некоторые, особое внимание – химическим превращениям, но не могла прогнозировать, указывать пути синтеза новых веществ.

«Органическая химия может сейчас кого угодно свести с ума. Она представляется мне дремучим лесом, полным удивительных вещей, безграничной чащей, из которой нельзя выбраться, куда не осмеливаешься проникнуть»
(из письма Ф.Велера к Й.Берцелиусу 1835г.)

Основные «противоречия»
органической химии
- Многообразие веществ – образовано небольшим числом элементов;
- Кажущееся несоответствие валентности в органических веществах – С 3 Н 8 ;
- Различные физические и химические свойства соединений, имеющих одинаковую молекулярную формулу (С 6 Н 12 О 6 – глюкоза, фруктоза; С 4 Н 10 О – бутиловый спирт, диэтиловый эфир)

Предпосылки возникновения теории
- Развитие и утверждение атомистических представлений ( съезд в Карслруэ, 1860г.);
- Установление понятий валентности (Э. Франкленд, 1853г.);
- Понятие четырехвалентности углерода (А. Кекуле, 1858г.);
- Идеи о соединении атомов углерода в цепи (А. Кекуле, А. Купер, 1857г.)
Целостной теории, подтвержденной экспериментом, не существовало.

Основные положения теории строения органических веществ
(А.М. Бутлеров 1861 – 1864 гг.)
1. Атомы в молекулах веществ соединены согласно их валентности . Углерод в органических соединениях всегда четырехвалентен, а его атомы способны соединяться друг с другом, образуя различные цепи. Порядок соединения атомов в молекулах может быть отображен при помощи структурных формул.

2. Свойства веществ определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т.е. химическим строением вещества. Различное строение при одном и том же составе и относительной молекулярной массе вещества обуславливает явление изомерии.
3. Свойства органических соединений зависят от взаимного влияния атомов и групп атомов в молекуле друг на друга. Наибольшее влияние оказывают атомы, непосредственно связанные друг с другом. Влияние атомов или групп атомов, не связанных непосредственно, ослабевает по мере их удаления друг от друга.

4. Зная строение вещества, можно предположить его свойства. И наоборот, зная свойства вещества, можно предположить его строение.
СН 3 СН 2 ОН этиловый спирт
С 2 Н 6 О
СН 3 О СН 3 диметиловый эфир
Если известно, что вещество, имеющее молекулярную формулу С 2 Н 6 О, вступает в химические реакции, характерные для спиртов (П: выделяет водород в реакции с металлическим натрием), то можно сделать вывод, что мы говорим об этиловом спирте С 2 Н 5 ОН.

Свойства веществ зависят не только от их химического строения, но также и от их электронного и пространственного строения
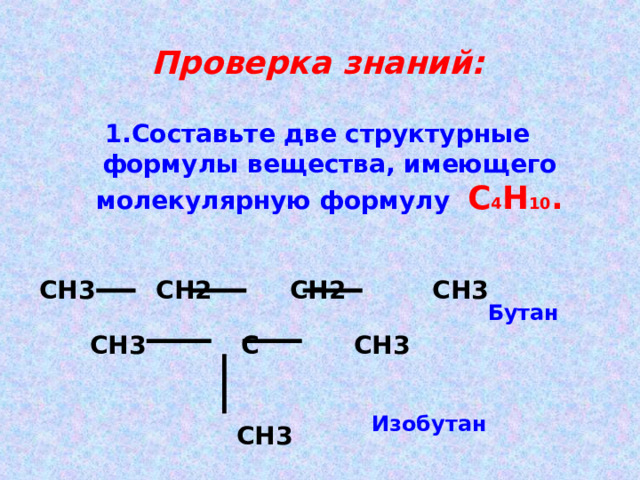
Проверка знаний:
- Составьте две структурные формулы вещества, имеющего молекулярную формулу С 4 Н 10 .
СН3 СН2 СН2 СН3
Бутан
СН3 С СН3
СН3
Изобутан
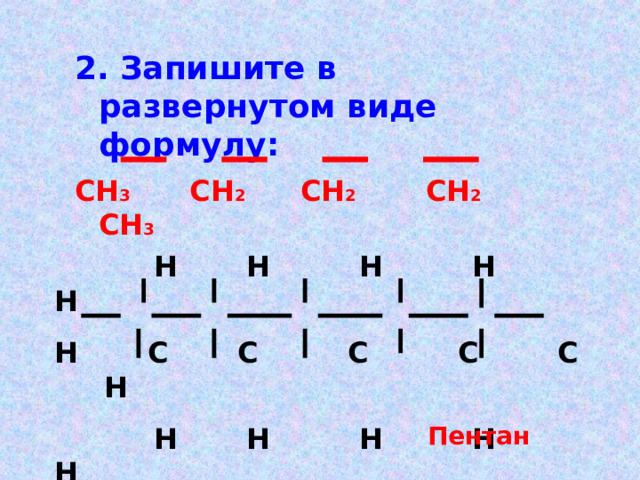
2. Запишите в развернутом виде формулу:
СН 3 СН 2 СН 2 СН 2 СН 3
Н Н Н Н Н
Н С С С С С Н
Н Н Н Н Н
Пентан
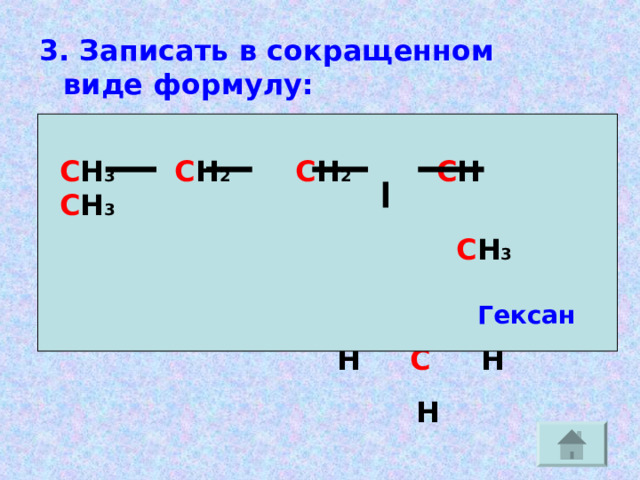
3. Записать в сокращенном виде формулу:
Н Н Н Н Н
Н С С С С С Н
Н Н Н Н
Н С Н
Н
С Н 3 С Н 2 С Н 2 С Н С Н 3
С Н 3
Гексан
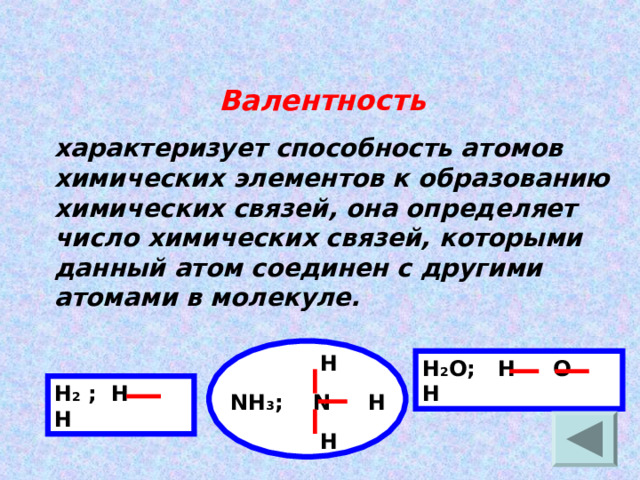
Валентность
характеризует способность атомов химических элементов к образованию химических связей, она определяет число химических связей, которыми данный атом соединен с другими атомами в молекуле.
H
NH 3 ; N H
H
Н 2 О; Н О Н
Н 2 ; Н Н

Вещества, которые имеют один и тот же качественный и количественный составы, но отличаются по своему строению и свойствам, называются изомерами , а явление существования таких веществ носит название изомерии
СН 3 СН СН 3
СН 3
СН 3 СН 2 СН 2 СН 3
БУТАН (С 4 Н 10 )
( t кип. = - 0,5 С)
ИЗОБУТАН (С 4 Н 10 )
( t кип. = -11,7 С)
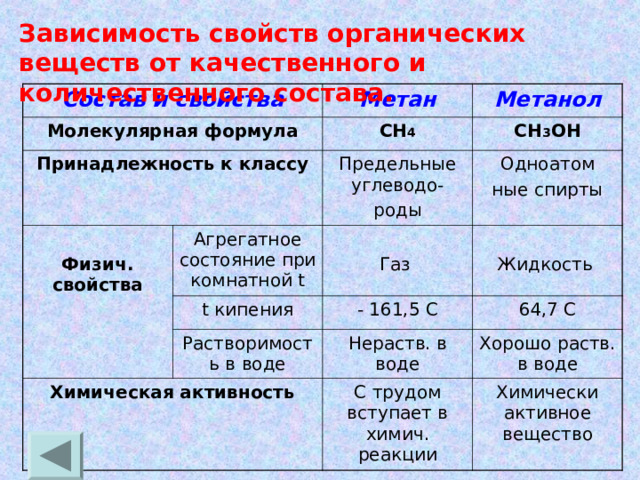
Зависимость свойств органических веществ от качественного и количественного состава.
Состав и свойства
Молекулярная формула
Принадлежность к классу
Метан
Метанол
СН 4
Физич. свойства
СН 3 ОН
Предельные углеводо-
роды
Агрегатное состояние при комнатной t
Одноатом
ные спирты
Газ
t кипения
Растворимость в воде
Жидкость
- 161,5 С
Химическая активность
64,7 С
Нераств. в воде
Хорошо раств. в воде
С трудом вступает в химич. реакции
Химически активное вещество
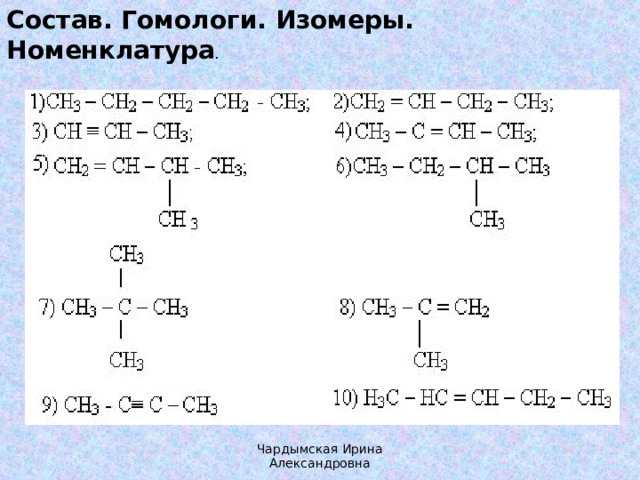
Состав. Гомологи. Изомеры. Номенклатура .
Чардымская Ирина Александровна
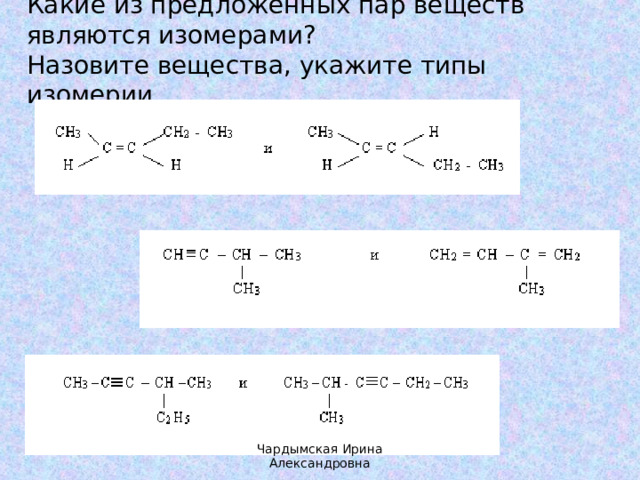
Какие из предложенных пар веществ являются изомерами?
Назовите вещества, укажите типы изомерии.
Чардымская Ирина Александровна

Какое из положений теории А.М. Бутлерова объясняет различие в реакциях соединений одинакового состава:
2 CH 3 -CH 2 -O-H + 2 Na 2 CH 3 -CH 2 -O-Na + H 2 CH 3 -O-CH 3 + Na реакция не идет
Ответ 1 : Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентности. Ответ 2 : Химическое строение можно устанавливать химическими методами. Ответ 3 : По свойствам данного вещества можно определить строение его молекул, а по строению молекул - предсказать свойства. Ответ 4 : Атомы и группы атомов в молекуле оказывают друг на друга взаимное влияние.
с
с
Чардымская Ирина Александровна

Изомерами называются . . .
Ответ 1 : вещества, имеющие сходное строение и сходные химические свойства, но разный количественный состав Ответ 2 : вещества, имеющие одинаковый качественный состав, но различные свойства Ответ 3 : вещества, имеющие одинаковый качественный и количественный состав, но различное строение молекул Ответ 4 : вещества, молекулы которых содержат одинаковое количество атомов углерода, но разное количество атомов других элементов
Чардымская Ирина Александровна

Какие из представленных на рисунке соединений являются изомерами?
Ответ 1 : 1, 2 и 1, 5 Ответ 2 : 1, 2 и 3, 6 Ответ 3 : 3, 6 и 1, 5 Ответ 4 : 2, 3 и 1, 5
Чардымская Ирина Александровна

Что такое атомная орбиталь?
Ответ 1 : Орбита, по которой движется электрон в поле ядра атома. Ответ 2 : Часть пространства, в котором вероятность нахождения электрона минимальна. Ответ 3 : Область наиболее вероятного пребывания электрона в поле ядер атомов, составляющих молекулу. Ответ 4 : Область наиболее вероятного пребывания электрона в электрическом поле ядра атома.
Чардымская Ирина Александровна

Ковалентная связь образуется . . .
Ответ 1 : парой электронов, предоставляемых атомом. Ответ 2 : за счет обобществления пары электронов при перекрывании атомных орбиталей двух (или более) атомов. Ответ 3 : за счет электростатического притяжения между заряженными частицами с завершенными внешними электронными оболочками.
Чардымская Ирина Александровна

Какая связь называется -связью ?
Ответ 1 : ковалентная связь, образованная при боковом перекрывании атомных р-орбиталей связываемых атомов. Ответ 2 : ковалентная связь, образованная при перекрывании атомных орбиталей вдоль межъядерной оси. Ответ 3 : ионная связь, образованная при осевом перекрывании атомных орбиталей связываемых атомов. Ответ 4 : ионная связь, образованная при боковом перекрывании атомных орбиталей связываемых атомов.
Чардымская Ирина Александровна

-Связью называется . . .
Ответ 1 : ковалентная связь, образованная при осевом перекрывании любых атомных орбиталей связываемых атомов. Ответ 2 : ковалентная связь, образованная при перекрывании атомных р-орбиталей вдоль межъядерной оси. Ответ 3 : ковалентная связь, образованная при боковом перекрывании атомных р-орбиталей связываемых атомов. Ответ 4 : ионная связь, образованная при боковом перекрывании атомных орбиталей связываемых атомов.
Чардымская Ирина Александровна

Гибридизация атомных орбиталей - это . . .
Ответ 1 : взаимодействие атомных орбиталей разных атомов с образованием гибридных орбиталей. Ответ 2 : взаимодействие разных по типу, но близких по энергии атомных орбиталей данного атома с образованием гибридных орбиталей одинаковой формы и энергии. Ответ 3 : взаимодействие одинаковых по типу, но разных по энергии атомных орбиталей данного атома с образованием гибридных орбиталей одинаковой формы и энергии.
Чардымская Ирина Александровна

Франкленд (Frankland) Эдуард (1825-99), английский химик-органик, иностранный член-корреспондент Петербургской АН (1876). Ввел термин «валентность» (1853).

Бутлеров Александр Михайлович (1828-86), российский химик-органик, академик Петербургской АН (1874). Создал (1861) и обосновал теорию химического строения, согласно которой свойства веществ определяются порядком связей атомов в молекулах и их взаимным влиянием. Первым объяснил (1864) явление изомерии. Открыл полимеризацию изобутилена. Синтезировал ряд органических соединений (уротропин, полимер формальдегида и др.). Труды по сельскому хозяйству, пчеловодству. Поборник высшего образования для женщин.

Берцелиус (Berzelius) Йенс Якоб (1779-1848), шведский химик и минералог, иностранный почетный член Петербургской АН (1820). Открыл церий (1803), селен (1817), торий (1828). Создал (1812-19) электрохимическую теорию химического сродства, на ее основе построил классификацию элементов, соединений и минералов. Определил (1807-18) атомные массы 45 элементов, ввел (1814) современные химические знаки элементов. Предложил термин «катализ».

Кекуле (Kekule) Фридрих Август (1829-96), немецкий химик-органик, иностранный член-корреспондент Петербургской АН (1887). Труды по теории строения органических соединений. Показал, что углерод четырехвалентен (1857) и его атомы могут соединяться друг с другом в цепи (1858). Предложил (1865) циклическую формулу бензола.

Велер Фридрих (1800-82), немецкий химик, иностранный член-корреспондент Петербургской АН (1853). Впервые синтезировал из неорганических веществ органическое соединение (1824) и установил его тождество с мочевиной (1828). Исследования Велера поставили под сомнение правоту витализма.






















































