Просмотр содержимого документа
«Разработка презентации по теме "Производство аммиака"»

Министерство образования и науки Республики Татарстан
ГОСУДАРСТВЕННОЕ АВТОНОМНОЕ ПРОФФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «КАЗАНСКИЙ НЕФТЕХИМИЧЕСКИЙ КОЛЛЕДЖ ИМЕНИ В.П. ЛУШНИКОВА»
Выполнила:
Преподаватель: Григорьева О.М.

- Аммиак
- И стория
- Химические свойства
- Применение
- Производство аммиака

бесцветный газ с резким запахом, температура плавления 80° С, температура кипения 36° С, хорошо растворяется в воде, спирте и ряде других органических растворителей. Синтезируют из азота и водорода.

Аммиак был впервые выделен в чистом виде Дж. Пристли в 1774 году, который назвал его «щелочной воздух» . Через одиннадцать лет, в 1785 году К. Бертолле установил точный химический состав аммиак .

С изменением степени окисления :
« И в том и в другом случае аммиак за счет атома азота проявляет свойства восстановителя.»


Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота:
Реакция происходит с выделением тепла и понижением объёма. Следовательно, исходя из принципа Ле-Шателье, реакцию следует проводить при возможно низких температурах и при высоких давлениях — тогда равновесие будет смещено вправо. Однако скорость реакции при низких температурах ничтожно мала, а при высоких увеличивается скорость обратной реакции. Проведение реакции при очень высоких давлениях требует создания специального, выдерживающего высокое давление оборудования, а значит и больших капиталовложений.
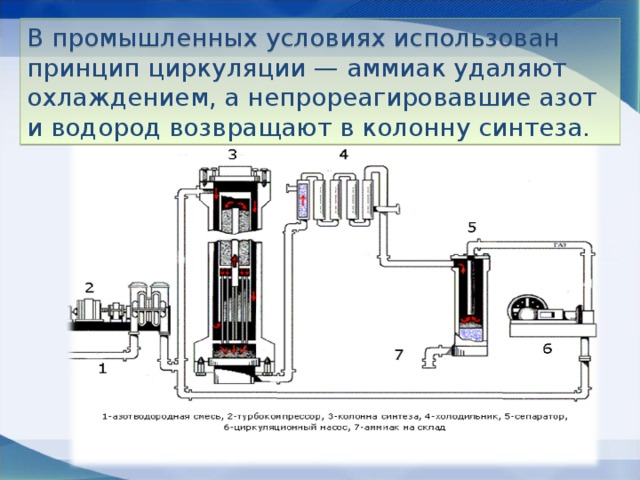
В промышленных условиях использован принцип циркуляции — аммиак удаляют охлаждением, а непрореагировавшие азот и водород возвращают в колонну синтеза.

Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония:
Обычно лабораторным способом аммиак получают слабым нагреванием смеси хлорида аммония с гашеной известью.


































