

19/02/19
РАСЧЕТЫ по химическим уравнениям

Цель: научиться вести расчеты по уравнению химической реакции, зная количество вещества, массу или объем одного из исходных веществ или продуктов реакции.

Что означает запись?
3 О 2
3 молекулы кислорода
НNО 3
1 молекула азотной кислоты
3 О
3 атома кислорода
N 2
1 молекула азота
3НСl
3 молекулы хлороводородной кислоты

Коллекция учебных динамических слайдов по химии 8 класс.
Уравнения химических реакций.
Уравнение химической реакции – это условная запись химической реакции, с помощью химических формул и коэффициентов.
Пример:
2NH 3
N 2
N 2
+
NH 3
H 2
+
3H 2
t 0 C кат.
t 0 C кат.
- реагирующие вещества (исходные , потребовались)
- продукты реакции (образуется, выделяется)
- взаимодействие (вступили в реакцию)
- условие протекания реакции
5
Баженов Алексей Анатольевич
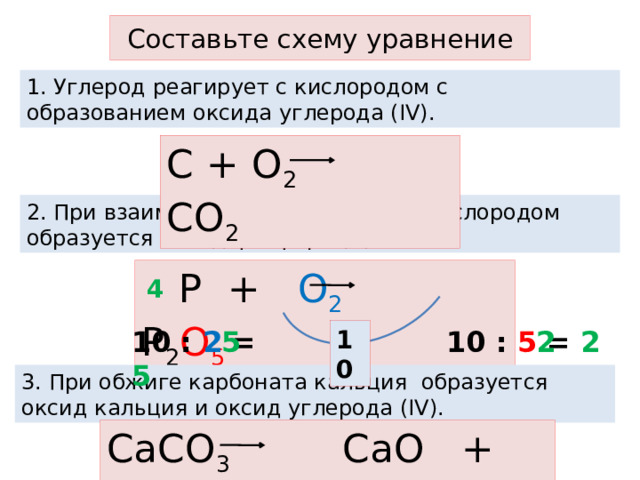
Составьте схему уравнение
1. Углерод реагирует с кислородом с образованием оксида углерода (IV).
С + О 2 СО 2
2. При взаимодействии форфора с кислородом образуется оксид фосфора (V).
Р + О 2 Р 2 О 5
4
10
10 : 5 = 2
10 : 2 = 5
5
2
3. При обжиге карбоната кальция образуется оксид кальция и оксид углерода (IV).
СаСО 3 СаО + СО 2

Определите
коэффициенты
1) Na + Сl 2 → Na Сl ;
2) Аl + S → Аl 2 S 3 ;
3) N Н 3 → N 2 + Н 2 ;
4) Р + Сl 2 → Р Сl 3 ;
5) Н 2 О → Н 2 + О 2 ;
6) ZnО + НСl → ZnСl 2 + Н 2 О;
2
2
2
2 : 1 =
2 : 2 = 1
2
2
3 : 1 = 3
3
3
6
6 : 3 = 2
2
6 : 2 = 3
3
2
6
6 : 2 = 3
3
2
6 : 3 = 2
2
2
2
2 : 1 = 2
2
2 : 1 = 2
2
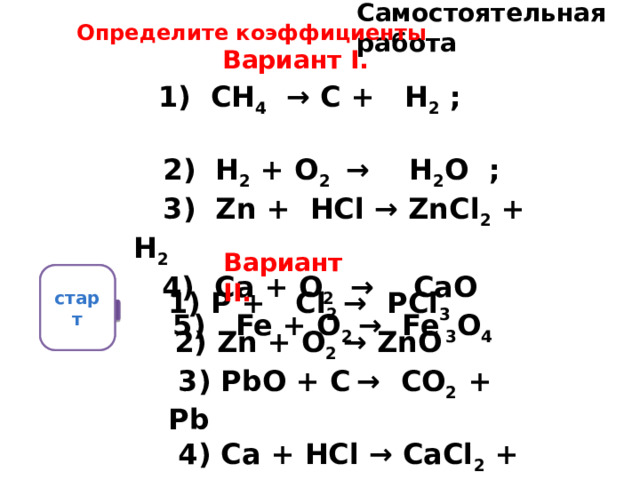
Самостоятельная работа
Определите коэффициенты
Вариант I.
1) СН 4 → С + Н 2 ;
2) Н 2 + О 2 → Н 2 О ;
3) Zn + НСl → ZnСl 2 + Н 2
4) Са + О 2 → СаО
5) Fe + О 2 → Fe 3 О 4
1) Р + Сl 2 → РСl 3
2) Zn + O 2 → ZnO
3) РbО + С → СО 2 + Рb
4) Cа + НСl → СаСl 2 + Н 2
5) НgО → Нg + О 2
Вариант II.
старт
5
1
2
3
10
9
8
0
7
6
4
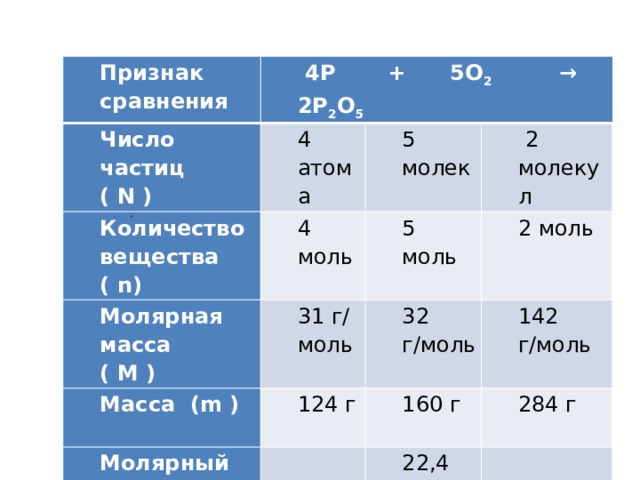
Признак сравнения
4Р + 5О 2 → 2Р 2 О 5
Число частиц
Количество вещества ( n)
4 атома
( N )
4 моль
5
Молярная масса
Масса (m )
31 г/моль
молек
2
5 моль
( M )
32 г/моль
124 г
Молярный объем ( V m
2 моль
молекул
160 г
142 г/моль
Объем ( V )
284 г
22,4 л/моль
112 л
.

Условие. Вычислите количество вещества кислорода, необходимое для получения 4 моль оксида фосфора.
Решение:
x моль 4 моль
4P + 5 О 2 = 2 P 2 О 5
5 моль 2 моль
Пропорция:
x 4 моль
5 моль 2 моль
x · 2 = 5 · 4
x = 10 моль О 2
Ответ: n(О 2 ) = 10 моль
Дано:
n(P 2 О 5 ) =4 моль
n (О 2 ) = ?
=
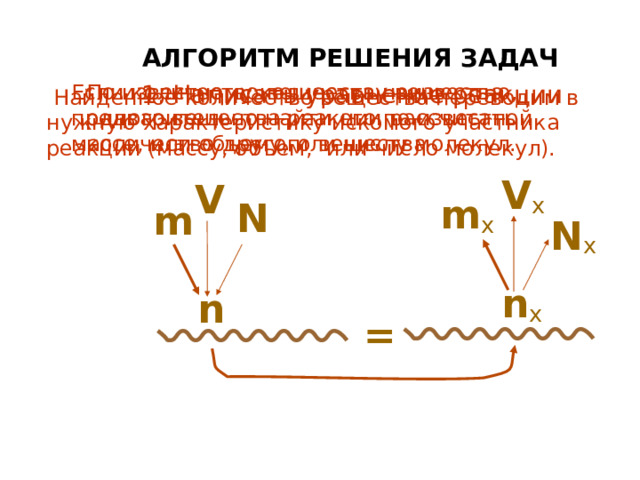
АЛГОРИТМ РЕШЕНИЯ ЗАДАЧ
По известному количеству вещества одного вещества реакции рассчитать количество другого вещества
Если количество вещества неизвестно, предварительно найти его по известной массе, или объему, или числу молекул.
1. Написать уравнение реакции
Найденное количество вещества переводим в нужную характеристику искомого участника реакции (массу, объем, или число молекул).
V x
V
m x
N
m
N x
n x
n
?
=
11
Вычислите массу оксида меди (II), образующегося при разложении 196 г гидроксида меди (II).
х моль
Дано:
Cu(OH) 2 = CuO + H 2 O
m(Cu(OH) 2 )=196 г
1 моль
1 моль
m
196 г
2 моль
=
2 моль Cu(OH) 2
m(CuO) = ?
=
n(Cu(OH) 2 ) =
98 г/моль
M
m
n = М
2 моль
х моль
=
1 моль
1 моль
M(Cu(OH) 2 ) =
х = 2 моль CuO
= 64+(16+1)·2 =
= 98 г/моль
m(CuO) = n · M
m(CuO) = n(CuO)·M(CuO) =
M(CuO) =
= 0,15 моль·80 г/моль = 12 г
= 64 +16 =
= 80г/моль
Ответ: m(CuO) = 12 г

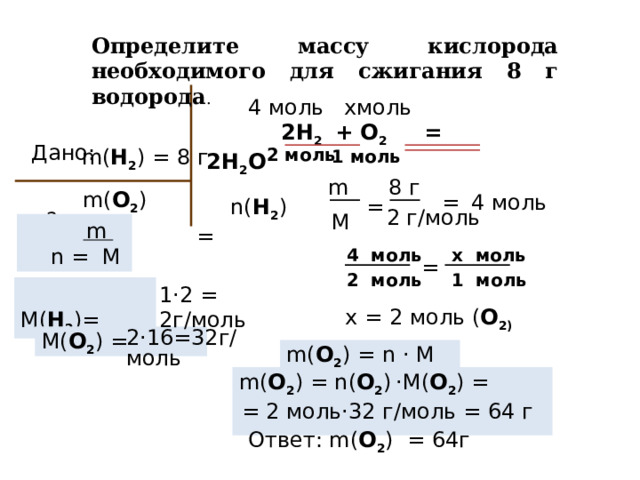
Определите массу кислорода необходимого для сжигания 8 г водорода .
4 моль хмоль
Дано:
2H 2 + О 2 = 2H 2 O
m( H 2 ) = 8 г
2 моль
1 моль
m
8 г
4 моль
=
m( О 2 ) = ?
n( H 2 ) =
=
2 г/моль
M
m
n = М
4 моль
х моль
=
2 моль
1 моль
M( Н 2 )=
1·2 = 2г/моль
х = 2 моль ( О 2)
2·16=32г/моль
M( О 2 ) =
m( О 2 ) = n · M
m( О 2 ) = n( О 2 ) ·M( О 2 ) =
= 2 моль·32 г/моль = 64 г
Ответ: m( О 2 ) = 64г

Какой объем кислорода (н.у.) образуется при разложении 120 г оксида магния.
x моль
Дано:
MgO = Mg + O 2 ↑
2
2
m(MgO) = 120 г
2 моль 1 моль
V(O 2 ) = ?
m
120 г
3 моль
n(MgO) =
= 3 моль
=
M(MgO) =
= 40 г/моль
24+16 =
40 г/моль
M
3 моль
х моль
=
2 моль
1 моль
Vm = 22,4 л/моль
х = 1,5 моль O 2
V(O 2 ) = n · Vm
0,15 моль· 22,4 л/моль
=3,36 г
V(O 2 ) = n(O 2 )·Vm =
Ответ: V(O 2 ) = 3,36 л

САМОСТОЯТЕЛЬНАЯ РАБОТА:
ВАРИАНТ 1:
1. Вычислите массу меди, которая образуется при взаимодействии 4 г водорода с оксида меди (II). CuO + H 2 = Cu + H 2 O
2 моль х моль
2. Составьте условие и решите: Са + O 2 = СаО
ВАРИАНТ 2:
1. В реакцию с серной кислотой вступило 20 г гидроксида натрия. Рассчитайте массу образовавшейся соли сульфата натрия.
2NaOH + H 2 SO 4 = Na 2 SO 4 + 2H 2 O
2 моль х моль
2. Составьте условие и решите: Мg + O 2 = МgО

Домашнее задание:
§ 28, с.160-166,
упр. 2,3.







































