Просмотр содержимого документа
«Производство серной кислоты»

Производство серной кислоты нитрозным ( башенным) способом
Михайлов Никита 11 “ А ”

Цель
- Узнать как создают серную кислоты нитрозным способом.
Задачи
- Изучит материал о получение серной кислоты нитрозным способом.

Серная кислота – одна из самых активных неорганических кислот. Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обменного разложения, энергично соединяется с водой, обладает окислительными и другими важными химическими свойствами.
Серная кислота является одним из основных продуктов химической промышленности и применяется в различных отраслях народного хозяйства. Серная кислота находит разнообразное применение в нефтяной, металлургической и других отраслях промышленности, она широко используется в производстве различных солей и кислот, всевозможных органических продуктов, красителей, дымообразующих и взрывчатых веществ, применяется в качестве водоотнимающего и осушающего средства, используется в процессах нейтрализации, травления и многих других.
Именно поэтому её так важно производить, ведь без этой кислоты, остановится огромное количество производства.
В этом проекте, мы поговорим о том, как производят серную кислоту при помощи нитрозного способа.

Нитрозный способ получения серной кислоты существует уже более 200 лет. Первый раз его обнаружили в Англии в 1740 году.
Камерная сернокислотная система начала 30-х годов XIX в. а - паровик; в - серная печь; d, e, f - свинцовые перегородки; g - труба для выпуска газов

Сущность нитрозного метода состоит в том, что обжиговый газ после очистки от пыли обрабатывается серной кислотой, в которой растворены оксиды азота, – так называемой нитрозой. Диоксид серы поглощается нитрозой и затем окисляется оксидами азота по реакции :
Усовершенствованная заводская камерная сернокислотная установка (конец XIX в.) 1 - печи обжига пирита; 2 - башня Гловера; 3 - свинцовые камеры; 4 - башня Гей-Люссака; 5 - насос; 6 - холодильник

Образующийся NO плохо растворим в нитрозе и поэтому выделяется из нее, а затем частично окисляется кислородом в газовой фазе до диоксида NO2 . Смесь оксидов азота NO и NO2 вновь поглощаются серной кислотой и т.д. Оксиды азота, по существу, не расходуются в нитрозном процессе и возвращаются в производственный цикл. Однако вследствие неполного поглощения их серной кислотой они частично уносятся отходящими газами; это составляет невозвратимые потери оксидов.
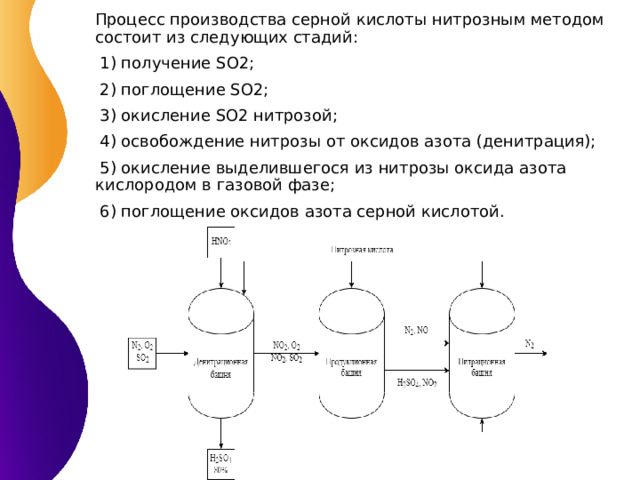
Процесс производства серной кислоты нитрозным методом состоит из следующих стадий:
1) получение SO2;
2) поглощение SO2;
3) окисление SO2 нитрозой;
4) освобождение нитрозы от оксидов азота (денитрация);
5) окисление выделившегося из нитрозы оксида азота кислородом в газовой фазе;
6) поглощение оксидов азота серной кислотой.
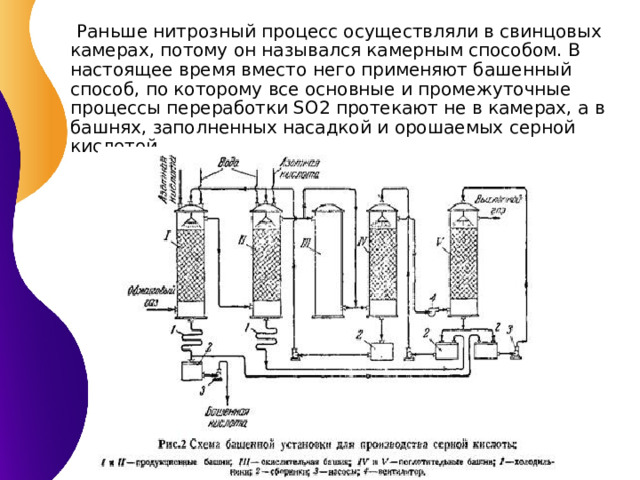
Раньше нитрозный процесс осуществляли в свинцовых камерах, потому он назывался камерным способом. В настоящее время вместо него применяют башенный способ, по которому все основные и промежуточные процессы переработки SO2 протекают не в камерах, а в башнях, заполненных насадкой и орошаемых серной кислотой.
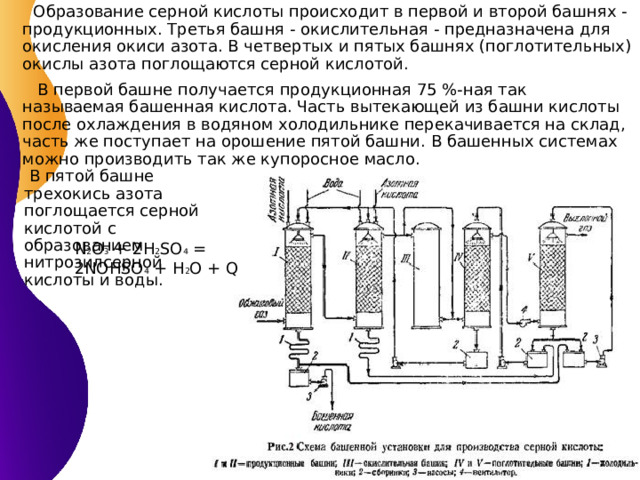
Образование серной кислоты происходит в первой и второй башнях - продукционных. Третья башня - окислительная - предназначена для окисления окиси азота. В четвертых и пятых башнях (поглотительных) окислы азота поглощаются серной кислотой.
В первой башне получается продукционная 75 %-ная так называемая башенная кислота. Часть вытекающей из башни кислоты после охлаждения в водяном холодильнике перекачивается на склад, часть же поступает на орошение пятой башни. В башенных системах можно производить так же купоросное масло .
В пятой башне трехокись азота поглощается серной кислотой с образованием нитрозилсерной кислоты и воды.
N 2 O 3 + 2H 2 SO 4 =
2NOHSO 4 + H 2 O + Q
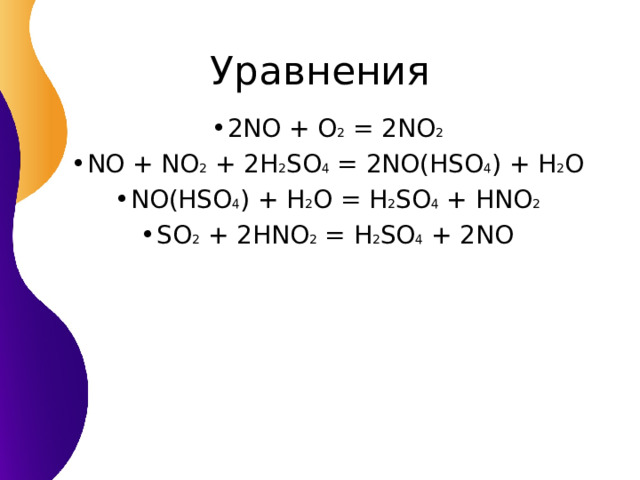
- 2 NO + O 2 = 2NO 2
- NO + NO 2 + 2H 2 SO 4 = 2NO(HSO 4 ) + H 2 O
- NO(HSO 4 ) + H 2 O = H 2 SO 4 + HNO 2
- SO 2 + 2HNO 2 = H 2 SO 4 + 2NO




































