Просмотр содержимого документа
«Природный газ. Алканы. 10 класс»

Тема урока
Алканы.

План.
- Определение. Общая формула класса углеводородов.
- Гомологический ряд.
- Виды изомерии.
- Номенклатура алканов
- Строение алканов.
- Физические свойства.
- Способы получения.
- Химические свойства.
- Применение.
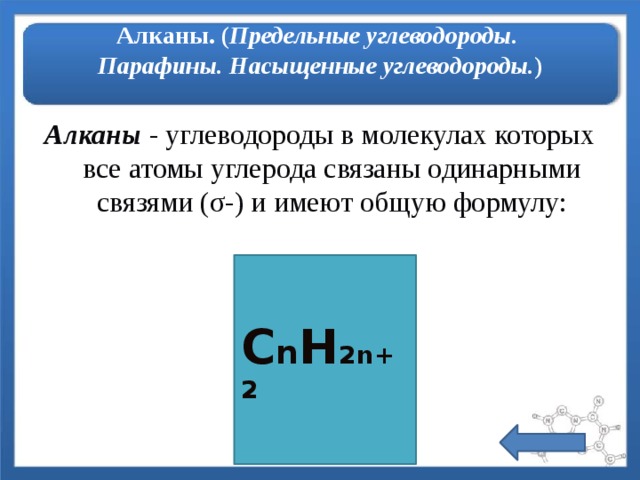
Алканы. ( Предельные углеводороды. Парафины. Насыщенные углеводороды. )
Алканы - углеводороды в молекулах которых все атомы углерода связаны одинарными связями (σ-) и имеют общую формулу:
C n H 2n+2

Гомологический ряд метана
Гомологи – это вещества, сходные по строению и свойствам
и отличающиеся на одну или более групп СH 2 .
СН 4 мет ан
С 2 H 6 эт ан
C 3 H 8 проп ан
C 4 H 10 бут ан
C 5 H 12 пент ан
C 6 H 14 гекс ан
C 7 H 16 гепт ан
C 8 H 18 окт ан
C 9 H 20 нон ан
C 10 H 22 дек ан
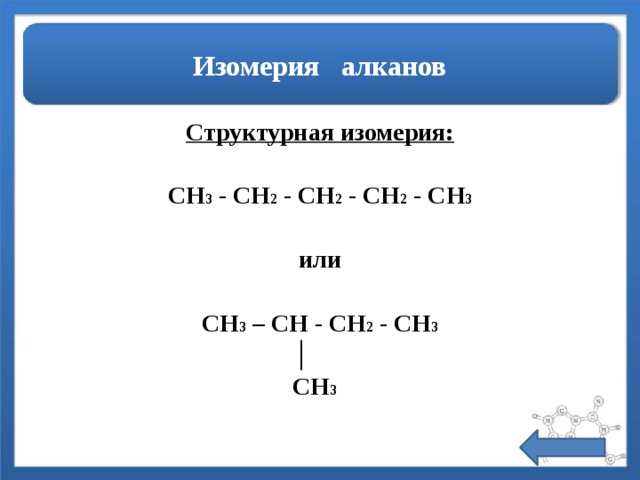
Изомерия алканов
Структурная изомерия:
CH 3 - CH 2 - CH 2 - CH 2 - CH 3
или
CH 3 – CH - CH 2 - CH 3
│
CH 3

номенклатура алканов
Алгоритм.
CH 3 – CH - CH 2 - CH 3
│
CH 3

Номенклатура алканов
2 . Нумерация атомов главной цепи:
1 2 3 4
CH 3 – CH - CH 2 - CH 3
│
CH 3
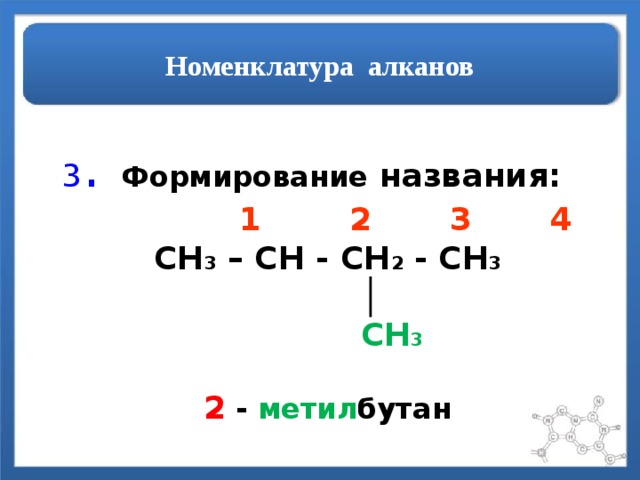
Номенклатура алканов
3 . Формирование названия:
1 2 3 4
CH 3 – CH - CH 2 - CH 3
│
CH 3
2 - метил бутан
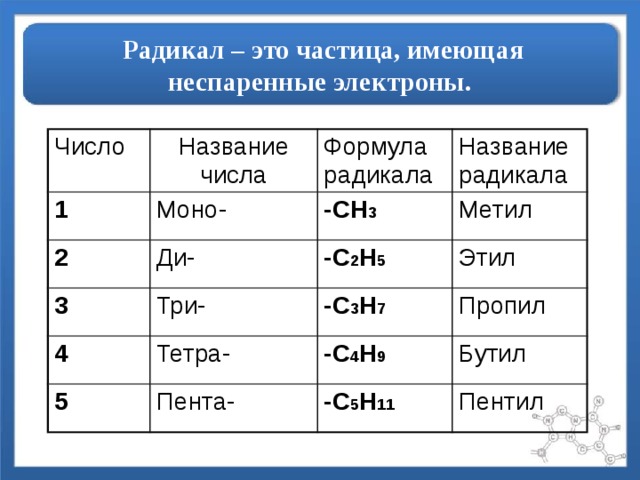
Радикал – это частица, имеющая неспаренные электроны.
Число
Название числа
1
Моно-
Формула радикала
2
Название радикала
-СН 3
Ди-
3
Три-
Метил
-С 2 Н 5
4
5
Тетра-
Этил
-С 3 Н 7
Пропил
Пента-
-С 4 Н 9
Бутил
-С 5 Н 11
Пентил
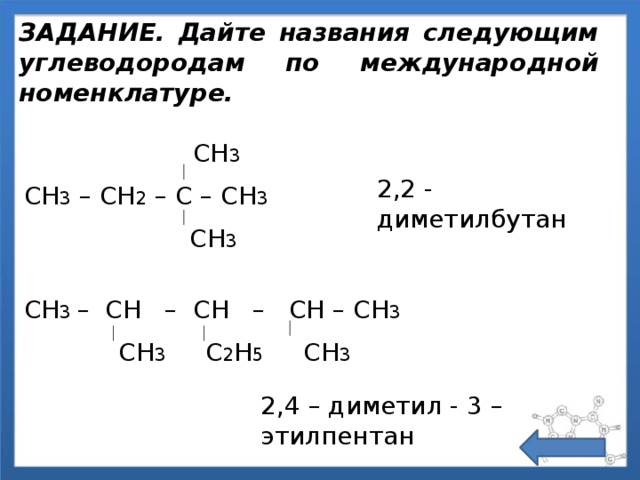
ЗАДАНИЕ. Дайте названия следующим углеводородам по международной номенклатуре.
СН 3
СН 3 – СН 2 – С – СН 3
СН 3
2,2 - диметилбутан
СН 3 – СН – СН – СН – СН 3
СН 3 С 2 Н 5 СН 3
2,4 – диметил - 3 – этилпентан
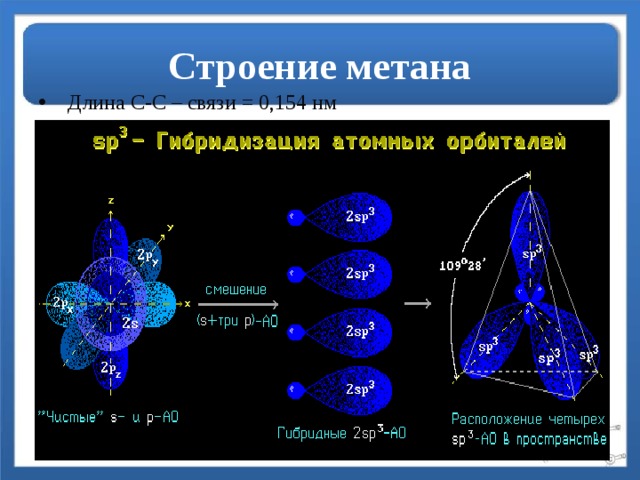
Строение метана
- Длина С-С – связи = 0,154 нм
Строение метана
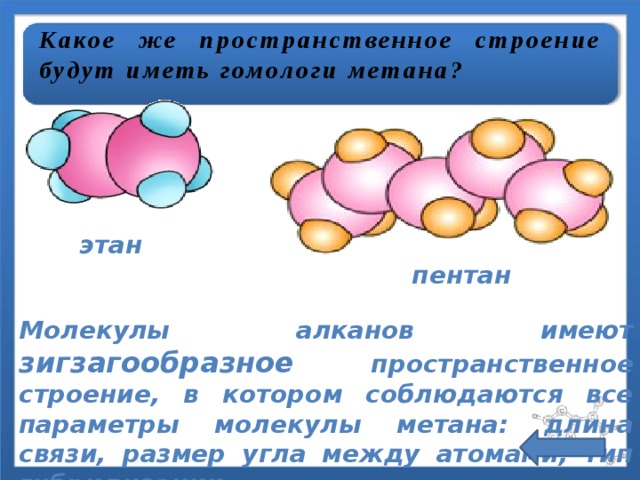
Какое же пространственное строение будут иметь гомологи метана?
этан
пентан
Молекулы алканов имеют зигзагообразное пространственное строение, в котором соблюдаются все параметры молекулы метана: длина связи, размер угла между атомами, тип гибридизации.
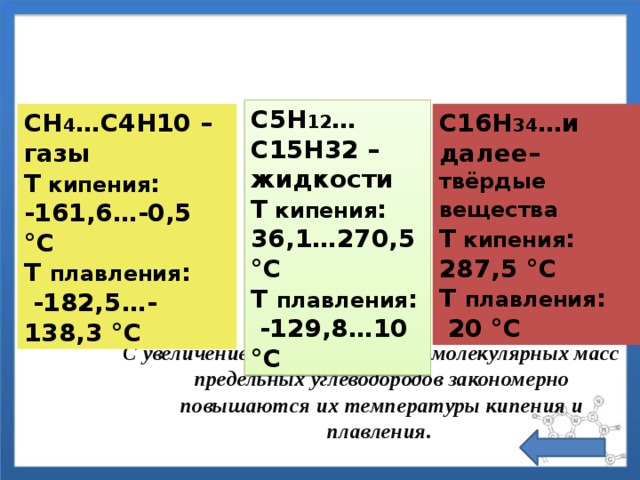
Физические свойства
С5Н 12 …C15Н32 – жидкости
T кипения :
36,1…270,5 °C
T плавления :
-129,8…10 °C
С16Н 34 …и далее– твёрдые вещества
СН 4 …C4Н10 – газы
T кипения :
T кипения :
-161,6…-0,5 °C
287,5 °C
T плавления :
T плавления :
-182,5…-138,3 °C
20 °C
С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются их температуры кипения и плавления.
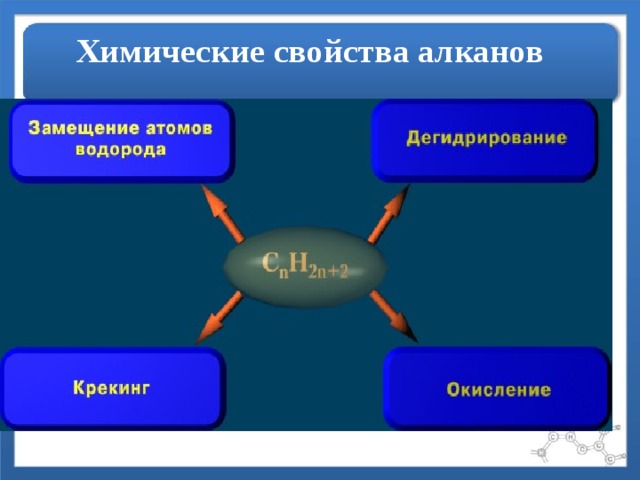
Химические свойства алканов

6. Реакция горения:
CH 4 + 2O 2 → CO 2 + 2H 2 O + Q
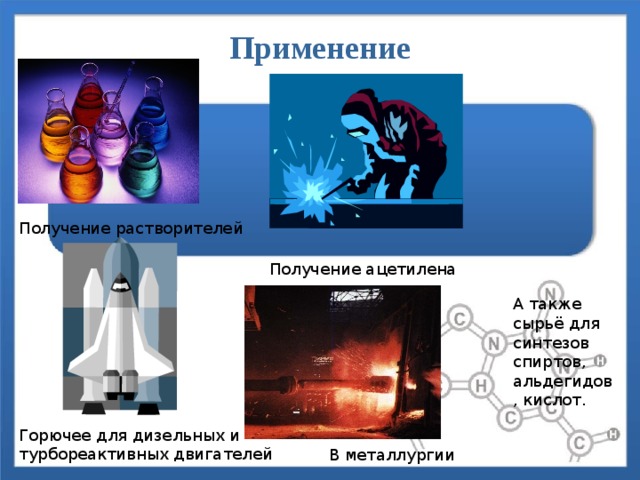
Применение
Получение растворителей
Получение ацетилена
А также сырьё для синтезов спиртов, альдегидов, кислот.
Горючее для дизельных и турбореактивных двигателей
В металлургии

Применение алканов
1-3 – производство сажи
(1 – картрижи;
2 – резина;
3 – типографическая краска)
4-7 – получение
органических веществ
(4 – растворителей;
5 – хладогентов,
используемых
в холодильных установках;
6 – метанол;
7 - ацетилен)

Проверка знаний
- Какие углеводороды относят к алканам?
- Запишите формулы возможных изомеров гексана и назовите их по систематической номенклатуре.

Домашнее задание
Учебник О.С. Габриелян
(10 класс базовый уровень)
§ 3, упр. 4, 7, 8 (стр. 32)











































