
- овладение знаниями об особенностях строения молекул аммиака, зависимости свойств от строения,
- ознакомление со способами получения аммиака в лаборатории, областями его использования и особенностями его влияния на живые организмы

1 . УСВОИТЬ ОСОБЕННОСТИ ОБРАЗОВАНИЯ КОВАЛЕНТНОЙ СВЯЗИ В МОЛЕКУЛЕ АММИАКА. 2 . СФОРМИРОВАТЬ ПРЕДСТАВЛЕНИЯ О СВОЙСТВАХ АММИАКА В ЗАВИСИМОСТИ ОТ СТРОЕНИЯ МОЛЕКУЛЫ. 3 . ПРИОБРЕСТИ УМЕНИЯ ПОЛУЧЕНИЯ АММИАКА В ЛАБОРАТОРИИ. 4.НАУЧИТЬСЯ ПРИМЕНЯТЬ ПОЛУЧЕННЫЕ ЗНАНИЯ ДЛЯ ОБЪЯСНЕНИЯ ПРИМЕНЕНИЯ АММИАКА В РАЗЛИЧНЫХ ОБЛАСТЯХ НАРОДНОГО ХОЗЯЙСТВА. 5 . СФОРМИРОВАТЬ ЭКОЛОГИЧЕСКИЕ ЗНАНИЯ О РОЛИ АММИАКА В ОКРУЖАЮЩЕЙ СРЕДЕ.

- ПОЛЯРНОСТЬ МОЛЕКУЛЫ АММИАКА. . ДОНОРНО- АКЦЕПТОРНЫЙ МЕХАНИЗМ ОБРАЗОВАНИЯ КАТИОНА АММОНИЯ . ОВР АММИАКА . ЭКОЛОГИЧЕСКАЯ РОЛЬ АММИАКА В ПРИРОДЕ

1. О КАКОМ ЭЛЕМЕНТЕ ПОЙДЁТ РЕЧЬ НА УРОКЕ? 2.КАКОВО ЕГО ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д.И.МЕНДЕЛЕЕВА? 3.КАКОЕ ЗНАЧЕНИЕ В ПРИРОДЕ ОН ИМЕЕТ?

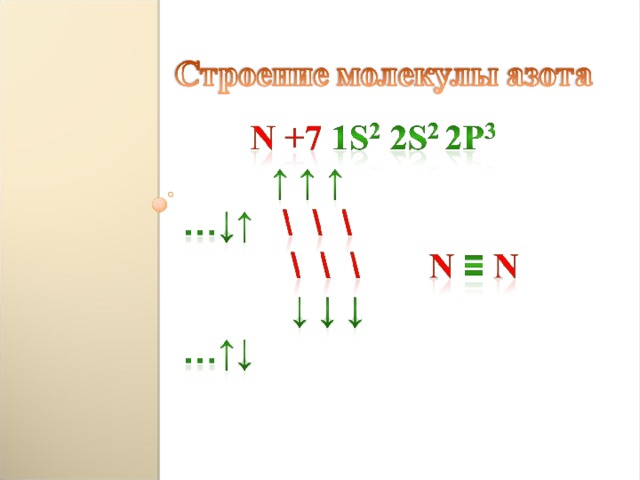

В СОСТАВЕ БЕЛКОВ ЖИВЫХ ОРГАНИЗМОВ -3% .БИОМАССА СУШИ – 10 МЛРД.Т . БИОМАССА ГИДРОСФЕРЫ – 300 МЛН.Т . В ВОЗДУХЕ – 72 %, 4 . 10 15 Т . НА 1 М 2 ПОВЕРХНОСТИ ЗЕМЛИ – 7500 Т

. ГАЗ, БЕЗ ЦВЕТА И ЗАПАХА, . НЕМНОГО ЛЕГЧЕ ВОЗДУХА, . РАСТВОРИМОСТЬ В ВОДЕ НЕЗНАЧИТЕЛЬНАЯ, . ИМЕЕТ НИЗКИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ( -195,8 0 )

1. УКАЖИТЕ ГРУППУ, В КОТОРОЙ ВСЕ ВЕЩЕСТВА БУДУТ ВЗАИМОДЕЙСТВОВАТЬ С АЗОТОМ: А)Н 2 , О 2 , М G Б)Н 2 , С L 2 , L I В)С, В R 2 , СИ 2.УКАЖИТЕ УРАВНЕНИЯ, КОТОРЫЕ ХАРАКТЕРИЗУЮТ СВОЙСТВА АЗОТА КАК ВОССТАНОВИТЕЛЯ. УРАВНЯЙТЕ УРАВНЕНИЕ №2 МЕТОДОМ ЭЛЕКТРОННОГО БАЛАНСА. А) N 2 +О 2 = Б) М G + N 2 = В) N 2 +Н 2 =
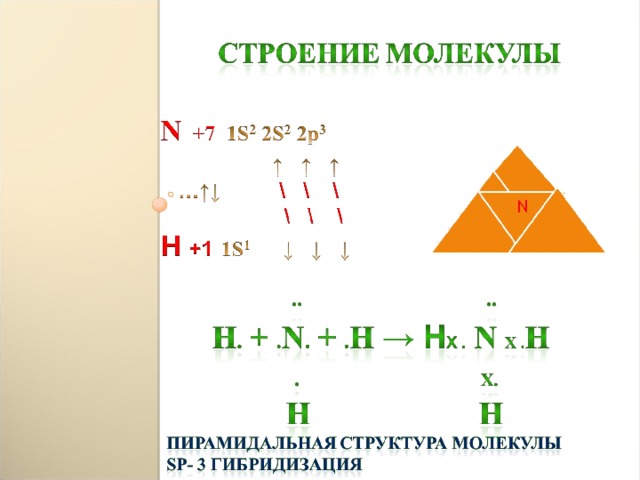



А) неполное Б) каталитическое
t Р t
4 NH 3 + 3 O 2 = 2 N 2 ↑ + 6 H 2 O N Н 3 +О 2 = N О ↑ + Н 2 О
-3 0 -3 +2
2 N -6е → N 2 4 /2 в - ль N – 5е → N 4 в - ль
0 -2 0 -2
О 2 +4е →2О 6/ 3 ок - ль О 2 +4е →2О 5 ок – ль
.. + - + - .. + - + -
N Н 3 + Н С l = N Н 4 С l N Н 3 + Н ОН → N Н 4 ОН
←

3 FEO+2NH 3 =3FE+N 2 ↑+3H 2 O

Свойства/
вещества
Применение
Гидроксид аммония
Аммиачная селитра
В медицине в качестве нашатырного спирта, в выведении пятен.
Для получения удобрений, солей аммония.
Способность к каталитическому окислению
Высокая теплота испарения
В производстве азотной кислоты.
В холодильных установках в качестве хладагентов
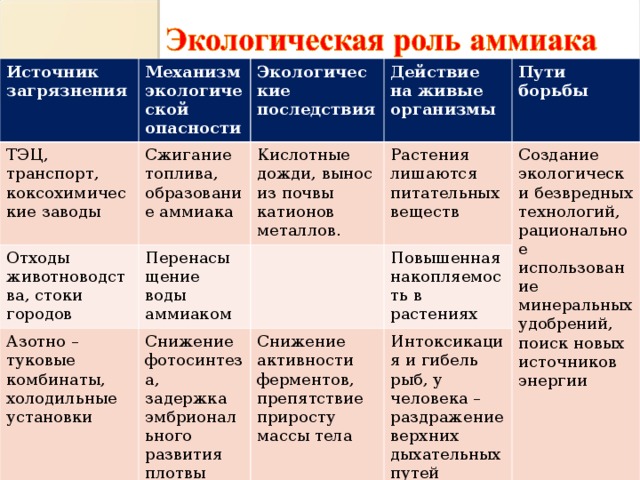
Источник загрязнения
Механизм экологической опасности
ТЭЦ, транспорт, коксохимические заводы
Сжигание топлива, образование аммиака
Экологические последствия
Отходы животноводства, стоки городов
Азотно – туковые комбинаты, холодильные установки
Перенасыщение воды аммиаком
Кислотные дожди, вынос из почвы катионов металлов.
Действие на живые организмы
Растения лишаются питательных веществ
Пути борьбы
Снижение фотосинтеза, задержка эмбрионального развития плотвы
Создание экологически безвредных технологий, рациональное использование минеральных удобрений, поиск новых источников энергии
Снижение активности ферментов, препятствие приросту массы тела
Повышенная накопляемость в растениях
Интоксикация и гибель рыб, у человека – раздражение верхних дыхательных путей

1. В КАКОМ НАПРАВЛЕНИИ СМЕСТИТСЯ ХИМИЧЕСКОЕ РАВНОВЕСИЕ РЕАКЦИИ:
NH 3 +H 2 O→NH 4 OH + Q
←
А) при увеличении температуры
Б) при добавлении щёлочи
В) при добавлении кислоты.
2.Укажите уравнения, протекающие с увеличением степени окисления азота:
t
А) NH 3 + О 2 →
Б) N 2 + Н 2 →
В) NH 3 +H 2 O→
3.Расположите соединения в порядке уменьшения степени окисления азота:
N О, N 2 , N О 2 , Н N О 3 , Н N О 2 , N Н 4 ОН

4. Восстановите недостающие части уравнений. Уравняйте методом электронного баланса уравнение №3.
1. N Н 3 +…→ N Н 4 ОН
2.( N Н 4 ) 2 S О 4 + Са(ОН) 2 →…
3.А l 2 О 3 + N Н 3 →…
4…+ Н 2 S О 4 → ( N Н 4 ) 2 S О 4
5.Осуществите превращения:
1. N 2 → N Н 3 → N О
↓ +Н N О 3
Х
6.Решите задачу:
Какая масса соли образуется при взаимодействии 0,072 л аммиака с 9,8 г серной кислоты?











































