Просмотр содержимого документа
«Презентация "Строение электронных оболочек атомов химических элементов №1-20"»

Строение электронных оболочек атомов химических элементов №1-20
ВЫПОЛНИЛА
МАМИТОВА К. Г
УЧИТЕЛЬ ХИМИИ И БИОЛОГИИ МБОУ СОШ С. КОСТА
2016

Содержание
- 1. Мотивация к учебной деятельности.
- 2. Актуализация знаний
- 3. Формулирование темы урока, постановка цели
- 4. Изучение нового материала
- 5. Закрепление.
6. Домашнее задание.
- 7. Литература
- 8. Приложения.

Актуализация знаний .
- Чему равно общее количество электронов в атоме?
- Чему равно общее количество электронов в атоме?
- Что такое энергетический уровень?
- Что такое энергетический уровень?
- Как определить число энергетических уровней?
- Как определить число энергетических уровней?
- Как определить число электронов на внешнем уровне?
- Как определить число электронов на внешнем уровне?

Расшифруйте ребусы, укажите их положение в ПСХЭ, определите число электронов в атомах этих химических элементов.

Ответы:
- 1. Никель ( 4 период ( большой), VIII группа ( побочная подгруппа) , порядковый № 28; электронов -28.
- 2.Йод ( 5 период ( большой), VII группа( главная подгруппа) , порядковый № 53; электронов -53.
- 3. Азот ( 2 период ( малый), V группа( главная подгруппа) , порядковый № 7; электронов -7.
- 4. Бор ( 3 период ( малый), III группа( главная подгруппа) , порядковый № 5; электронов -5.
- 5. Марганец( 4 период ( большой), VII группа( побочная подгруппа) , порядковый № 25; электронов -25.
- 6. Кремний( 3 период ( малый), IV группа( главная подгруппа) , порядковый № 14; электронов -14.

Ответы
- 7. Мышьяк( 4 период ( большой), V группа( главная подгруппа) , порядковый № 33; электронов -33.
- 8. Углерод( 2 период ( малый), I V группа( главная подгруппа) , порядковый № 6; электронов -6.
- 9. Цирконий( 5 период ( большой), IV группа( побочная подгруппа) , порядковый № 40; электронов -40.
- 10. Аргон( 3 период ( малый), VIII группа( главная подгруппа) , порядковый № 18; электронов -18.
- 11. Медь( 4 период ( большой), I группа( побочная подгруппа) , порядковый № 29; электронов -29.
- 12. Криптон( 4 период ( большой), VIII группа( главная подгруппа) , порядковый № 36; электронов -36.

ТЕМА УРОКА
- «Строение электронных оболочек атомов химических элементов
№ 1-20».

Цель урока:
- научиться составлять электронные формулы атомов элементов первых трех периодов ПСХЭ;
- объяснять зависимость и закономерные изменения свойств химических элементов от электронного строения их атомов
.

Электронная оболочка
- Совокупность всех электронов в атоме, окружающих ядро
- Каждый электрон имеет свою траекторию движения и запас энергии
- Электроны расположены на различном расстоянии от ядра: чем ближе электрон к ядру, тем он прочнее с ним связан, его труднее вырвать из электронной оболочки
- По мере удаления от ядра запас энергии электрона увеличивается, а связь с ядром становится слабее
.

Энергетические уровни состоят из подуровней : S, p, d, f
Число подуровней на уровне равно номеру уровня
1
Е 1
2
Подуровни состоят из орбиталей. Число орбиталей на уровне - n 2
Максимальное число электронов на энергетическом уровне определяется по формуле 2n 2
ядро
3
Электронные слои (энергетические уровни - n ) – совокупность электронов на одной оболочке, имеют одинаковый запас энергии
Число энергетических уровней в атоме равно номеру периода, в котором располагается атом
Сколько энергетических уровней у атомов:
углерода, натрия, золота, водорода, железа?
Е
n=7
n=6
f
d
p
n=5
n=4
S
n=3
p
d
S
n=2
p
S
n=1
S

- Энергетические уровни , содержащие максимальное число электронов, называются завершенными . Они обладают повышенной устойчивостью и стабильностью
- Энергетические уровни, содержащие меньшее число электронов, называются незавершенными
- n=1 – 1 подуровень ( S ), 2 электрона
- n= 2 – 2 подуровня ( S , р), 8 электронов
- n= 3 – 3 подуровня ( S , р, d ), 1 8 электронов
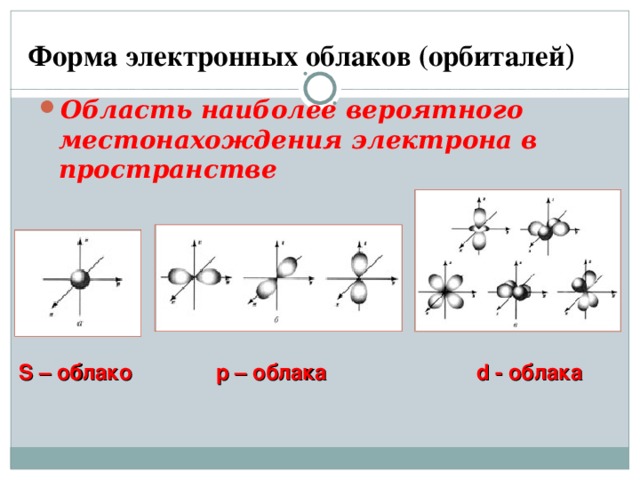
Форма электронных облаков (орбиталей )
- Область наиболее вероятного местонахождения электрона в пространстве
S – облако р – облака d - облака

Выводы:
- Электроны, двигаясь вокруг ядра атома, образуют электронную оболочку.
- Электронная оболочка состоит из электронных слоев.
- Каждый электронный слой состоит из электронов с близким значением энергии, поэтому электронные слои называются еще и энергетическими уровнями.
- Число энергетических уровней в атоме равно № периода.
- Максимальное число электронов, которое может находиться на определенном энергетическом уровне, можно вычислить по формуле 2 n 2 , где n - номер энергетического уровня.
.

1 период
Н + 1
1 S 1
n=1
S
1
Одиночный электрон на незавершенной оболочке
S - элементы
Н e + 2
1 S 2
n=1
S
2
2 спаренных электрона на завершенной оболочке
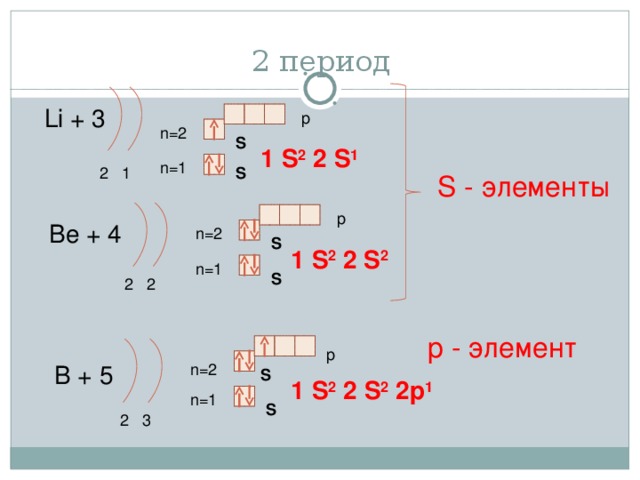
2 период
Li + 3
p
n=2
S
1 S 2 2 S 1
n=1
2 1
S
S - элементы
p
Be + 4
n=2
S
1 S 2 2 S 2
n=1
S
2 2
р - элемент
p
n=2
B + 5
S
1 S 2 2 S 2 2p 1
n=1
S
2 3
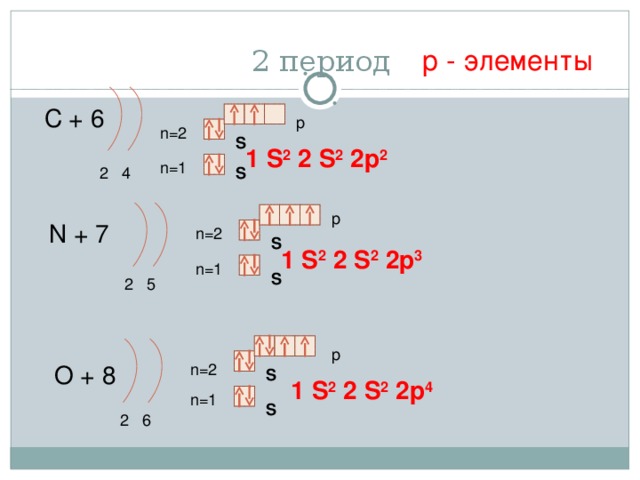
2 период
р - элементы
С + 6
p
n=2
S
1 S 2 2 S 2 2p 2
n=1
2 4
S
p
N + 7
n=2
S
1 S 2 2 S 2 2p 3
n=1
S
2 5
p
n=2
O + 8
S
1 S 2 2 S 2 2p 4
n=1
S
2 6

3 период
d
S- р - элементы
p
S
n= 3
Mg + 12
p
n=2
S
1 S 2 2 S 2 2p 6 3 S 2
n=1
2 8 2
S
S
n= 3
p
Al + 13
n=2
S
1 S 2 2 S 2 2p 6 3 S 2
3p 1
n=1
2 8 3
d
p
n= 3
Si + 14
S
p
n=2
1 S 2 2 S 2 2p 6 3 S 3p 2
S
2 8 4
n=1
S
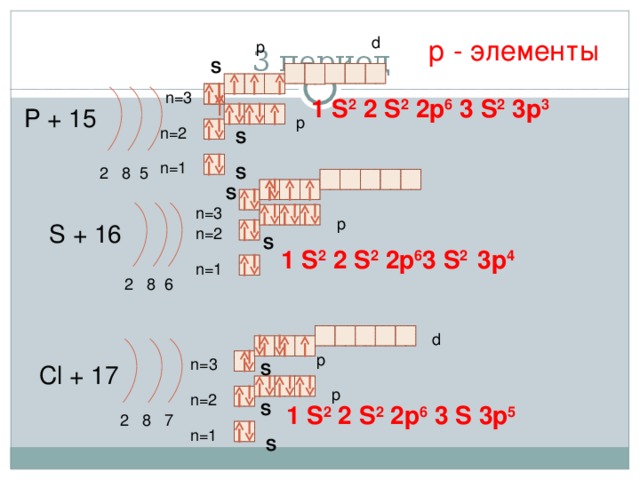
3 период
р - элементы
d
p
S
n= 3
1 S 2 2 S 2 2p 6 3 S 2 3p 3
P + 15
p
n=2
S
n=1
2 8 5
S
S
n= 3
p
S + 16
n=2
S
3p 4
1 S 2 2 S 2 2p 6 3 S 2
n=1
2 8 6
d
p
n= 3
Cl + 17
S
p
n=2
1 S 2 2 S 2 2p 6 3 S 3p 5
S
2 8 7
n=1
S

Игра в «Крестики- нолики» выигрышный путь составляют :
А)элементы одного периода
1s²2s²
1s²2s1
1s²2s²2p²
1s²2s²2p6 3s1
1s²2s²2p6 3s²
1s²2s²2p5
1s²2s²2p3
1s²2s²2p4
1s²

Игра в «Крестики- нолики»
выигрышный путь составляют :
Б)элементы одной главной подгруппы
1s ² 2s ²
1s ² 2s 2 2p 4
1s ² 2s ² 2p 6
1s 1
1s ² 2s 1
1s ² 2s ² 2p 6 3s 1
1s ² 2s ² 2p 5
1s ² 2s ² 2p 1
1s ² 2 s ² 2p 3

Игра в «Крестики- нолики»
выигрышный путь составляют :
В)элементы, расположенные рядом в ПСХЭ
1s ² 2s 1
1s ²
1s ² 2s ² 2p 5
1s ² 2s ² 2p 2
1s ² 2s 2
1s ² 2s ² 2p 6
1s ² 2s ² 2p 3
1s ² 2s ² 2p 4
1s ² 2 s ² 2p 1
Рефлексия
Я все понял, могу объяснить другому
По данной теме у меня остались вопросы
Недостаточно понял тему, сам ошибаюсь

Выводы
- Причина сходства элементов заключается в одинаковом строении внешних энергетических уровней их атомов
- Одинаковое строение внешних энергетических уровней периодически (т.е. через определенные промежутки - периоды) повторяется , поэтому периодически повторяются и свойства химических элементов

Домашнее задание

















































