Просмотр содержимого документа
«Презентация "Соли"»

Здравствуйте!

«Соли» класс неорганических соединений
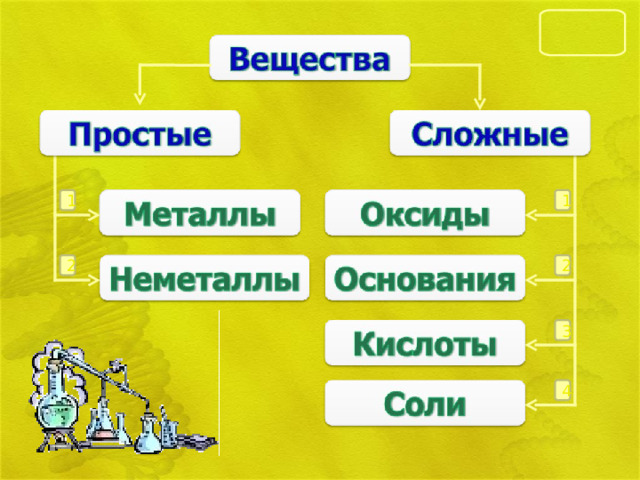
1
1
2
2
3
4
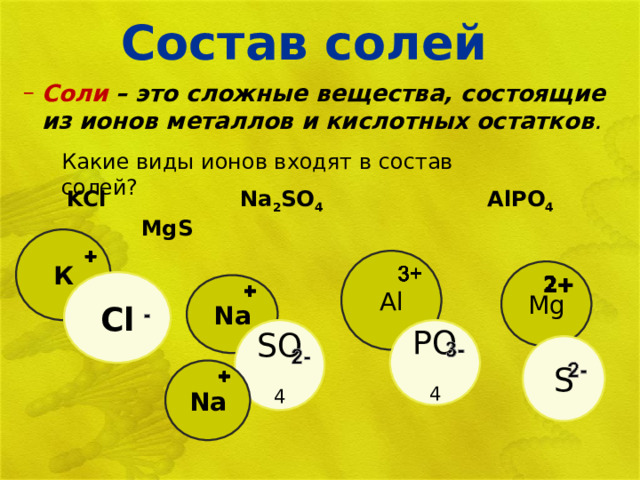
Состав солей
- Соли – это сложные вещества, состоящие из ионов металлов и кислотных остатков .
- Соли – это сложные вещества, состоящие из ионов металлов и кислотных остатков .
Какие виды ионов входят в состав солей?
KCl Na 2 SO 4 AlPO 4 MgS
К
Al
Mg
Cl
Na
SO 4
PO 4
S
Na
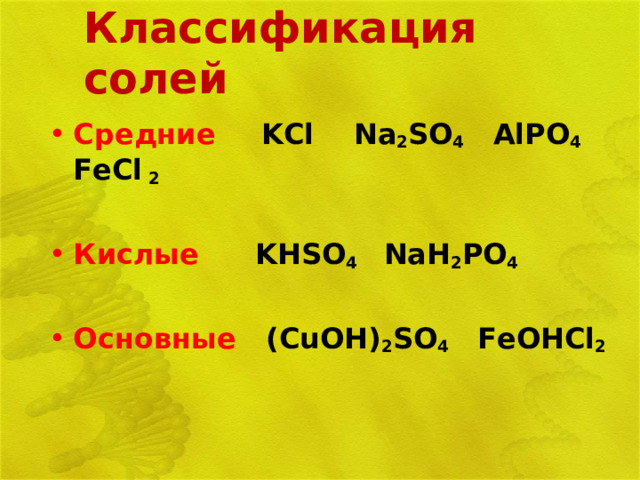
Классификация солей
- Средние KCl Na 2 SO 4 AlPO 4 FeCl 2
- Основные (CuOH) 2 SO 4 FeOHCl 2
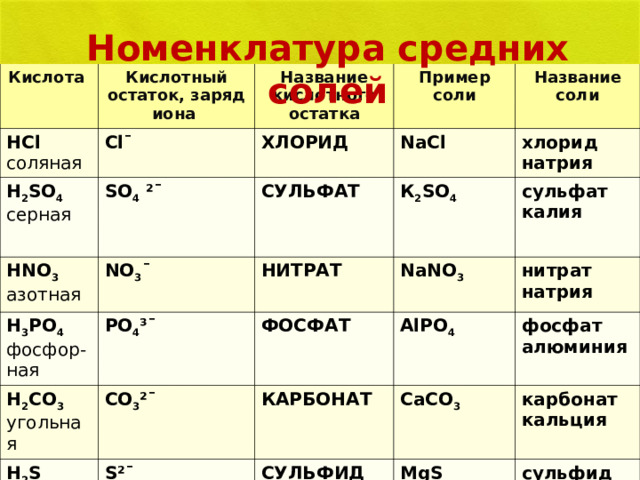
Номенклатура средних солей
Кислота
HCl
соляная
Кислотный остаток, заряд иона
Cl¯
Н 2 S О 4
серная
Название кислотного остатка
ХЛОРИД
S О 4 ²¯
Пример соли
Н NO 3
азотная
Название соли
NaCl
СУЛЬФАТ
NO 3 ¯
Н 3 РО 4
фосфор-ная
хлорид натрия
РО 4 ³¯
К 2 S О 4
НИТРАТ
Н 2 СО 3 угольная
NaNO 3
ФОСФАТ
сульфат калия
СО 3 ²¯
Н 2 S
серово-дородная
AlP О 4
нитрат натрия
КАРБОНАТ
S²¯
фосфат алюминия
СаСО 3
СУЛЬФИД
карбонат кальция
MgS
сульфид магния

Номенклатура кислых и основных солей
- У кислых солей приставка ГИДРО добавляется к названию аниона.
- KHSO 4 гидро сульфат калия
- NaH 2 PO 4 ди гидро сульфат натрия
- У основных солей приставка ГИДРОКСО добавляется к названию аниона.
- (CuOH) 2 SO 4 гидроксо сульфат меди ( II )
- FeOHCl 2 гидроксо хлорид железа ( III )

Сделай сам!
- Даны формулы солей. Раздели их на 3 группы, назови каждую соль.
- KHCO 3 K 2 SO 4 NaH 2 PO 4 (CuOH) 2 CO 3 CaSiO 3

Алгоритм составления формулы соли по названию.
- 1. Записать ионы металла и кислотного остатка, указать заряды ионов.
- 2. Найти наименьшее общее кратное и поочередно разделить на заряды ионов.
- 3. Полученные числа записать как индексы у соответствующего иона.

Сделай сам!
Составь формулы солей:
- а) сульфат лития
- б) гидросульфат лития
- в) дигидрофосфат лития

Физические свойства солей

Представители класса «Соли»
CuSO 4
KNO 3
MgSO 4
KNO 3
MgSO 4
CuSO 4
CaCO 3 (мел )
CaCO 3 (мел )
KCl (сильвин)
FeTiO 3
(ильменит )
KMnO 4
FeCl 3
FeCl 3
KMnO 4
FeTiO 3
(ильменит )
KCl (сильвин)

«Черный ящик»
- Вещество, без которого невозможна жизнь растений, животных и человека.
- Это химическое соединение необходимо для существования в крови эритроцитов, сокращения мышц, переваривания пищи в желудке.
- В год каждый человек потребляет от 3 до 5 кг. этого вещества.
- Это вещество- символ гостеприимства и радушия русской нации.
- Говорят, чтобы узнать человека, надо с ним пуд этого вещества съесть.

"Среди всех природных минеральных солей, самая главная та, которую мы называем просто “соль” А.Е.Ферсман

Добыча соли
из соляных шахт
из соленых озер

Знаете ли вы, что…
- Толщина пласта соли в Соль- Илецке превышает 1,5 км.
- Поваренной солью, извлеченной только из морской воды, можно было бы засыпать всю сушу Земного шара слоем 130 м.
- А для территории Европы этого количества хватило бы для слоя толщиной около 5 км.

Меловые горы CaCO 3

Моллюски, раки, радиолярии, кораллы – все имеют известковый скелет

Минералы карбоната кальция находятся в горных породах:
Известняк

Химические свойства
1.Взаимодействие с кислотами:
CO 2
CaCO 3 + HCl → CaCl 2 + H 2 CO 3
H 2 O
Сильные кислоты вытесняют более слабые из их солей!

Химические свойства
2. Взаимодействие со щелочами:
3Na ОН + FeCl 3 → Fe(OH) 3 + 3NaCl

Химические свойства
3. Взаимодействие с металлами:
CuSO 4 + Fe FeSO 4 + Cu

Химические свойства
4. Взаимодействие солей
между собой
Na 2 S + Cu(NO 3 ) 2 → CuS + 2NaNO 3

Химические свойства
- Разложение при нагревании
СаСО 3 = СО 2 + Н 2 О

Домашнее задание:
§ 41, упр.2;

Ответьте на утверждение знаком
«+» или «-»:
1. На уроке было над
чем подумать
2. Я понял новую тему
3. На все возникшие у меня
вопросы я получил ответы
4. На уроке я поработал
добросовестно
5. Оцените свою работу на уроке по пятибалльной системе.

Спасибо за работу! Всего доброго!





















































