
В 1782 году Карл Шееле , окисляя этиловый спирт оксидом марганца (IV) в серной кислоте, заметил, что помимо основного продукта — уксусной кислоты — образовалось еще какое-то резко пахнущее соединение, выделить которое не удалось.
Шульга Л.В. Агротехнический колледж № 7

В 1821 году
Иоганн Вольфганг Дёберейнер
окислял этиловый спирт в присутствии платинового катализатора и получил некоторое количество смеси исходного спирта с продуктами его окисления. Дёберейнер отправил полученный им образец Ю. Либиху

В 1835 году
Ю.Либих
выделил чистое вещество, содержащее на два атома водорода меньше, чем этанол. Ученый установил его состав (С 2 Н 4 О) и объявил, что получил новое вещество, названное Alkohol dehydrogenatus — безводородный алкоголь или сокращенно альдегид

Поскольку первый из известных альдегидов содержал два атома углерода, начались попытки получения первого представителя гомологического ряда.
В 1868 году
немецкий химик-органик
Август Вильгельм Гофман ,
пропуская пары метилового спирта над раскаленной платиновой спиралью, получил газообразное вещество состава СН 2 О.
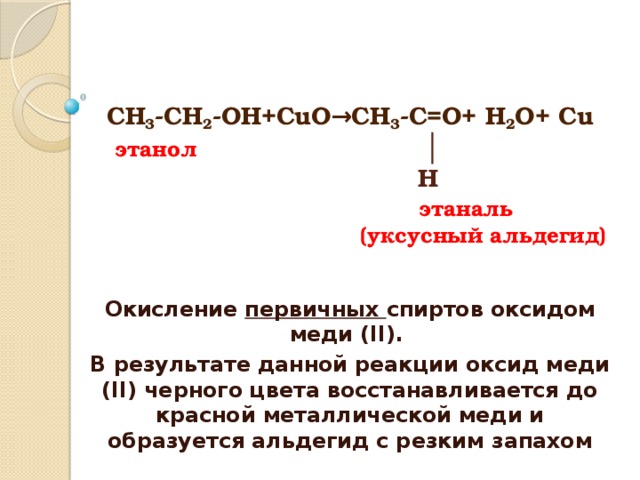
СН 3 -СН 2 -ОН+СuO →CH 3 -C=O+ H 2 О+ Cu этанол │ H этаналь (уксусный альдегид)
Окисление первичных спиртов оксидом меди (II).
В результате данной реакции оксид меди (II) черного цвета восстанавливается до красной металлической меди и образуется альдегид с резким запахом
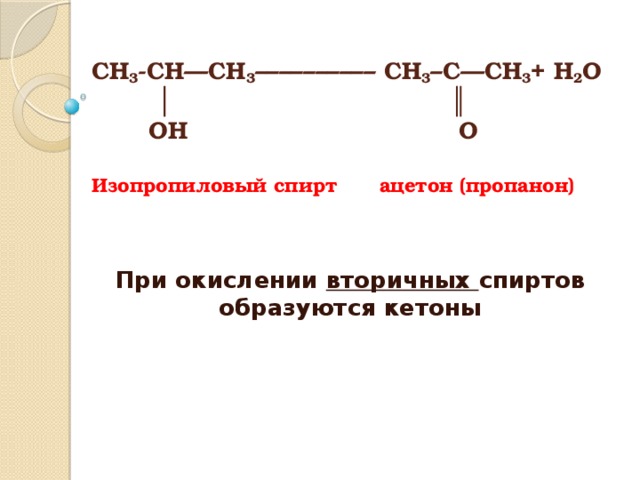
СН 3 -СН—СН 3 –––––––––– СН 3 –С—СН 3 + Н 2 О │ ║ ОН О Изопропиловый спирт ацетон (пропанон)
При окислении вторичных спиртов образуются кетоны
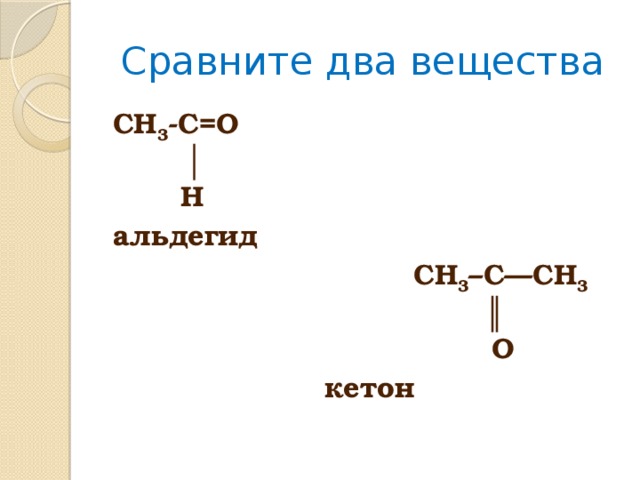
Сравните два вещества
CH 3 -C=O │ H
альдегид
СН 3 –С—СН 3 ║ О
кетон
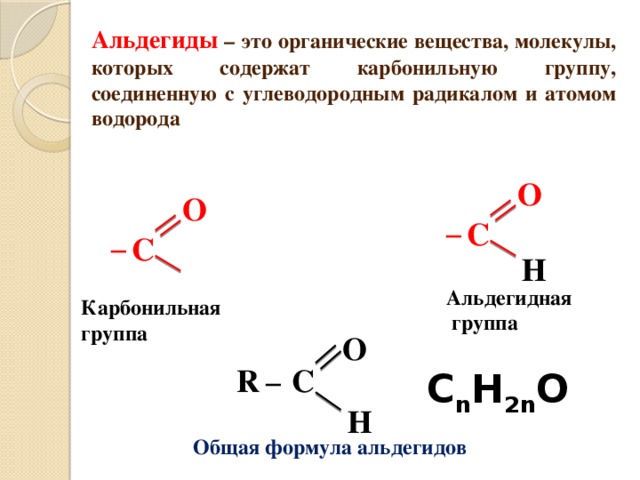
Альдегиды – это органические вещества, молекулы, которых содержат карбонильную группу, соединенную с углеводородным радикалом и атомом водорода
О
О
С
─
С
─
Н
Альдегидная
группа
Карбонильная группа
О
С
R ─
C n H 2n O
Н
Общая формула альдегидов
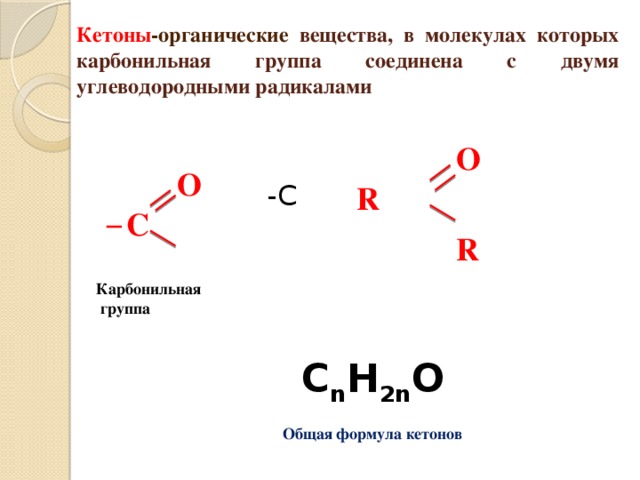
Кетоны -органические вещества, в молекулах которых карбонильная группа соединена с двумя углеводородными радикалами
-C
О
О
R
С
─
R
Карбонильная
группа
C n H 2n O
Общая формула кетонов

Тема урока
Альдегиды и кетоны

Ожидание
Цели урока:
- познакомиться со строением альдегидов и кетонов
- знать физические свойства альдегидов
- уметь давать названия по систематической номенклатуре
- зависимость химических свойств от состава и строения
- применение и получение

Дерево решений
1 экипаж - Классификация альдегидов, физические свойства альдегидов, строение карбонильной группы
2 экипаж- Гомологический ряд альдегидов, номенклатура, изомерия, общая формула альдегидов
3 экипаж - Получение альдегидов
4 экипаж - Применение формальдегида и ацетальдегида
5 экипаж- Кетоны, строение, номенклатура, свойства
9
Шульга Л.В. Агротехнический колледж № 7

Классификация альдегидов
ароматические
Н-С=О
СН
С
СН
СН
Н-С=О
СН
СН
Альдегиды
насыщенные
Н-С=О
СН
С
ненасыщенные
С

Гомологический ряд альдегидов
Метаналь (формальдегид)
Этаналь (ацетальдегид)
Пропаналь
Бутаналь
Пентаналь
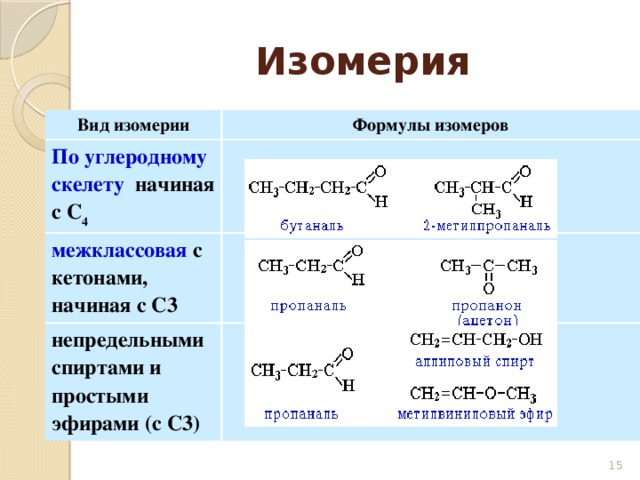
Изомерия
Вид изомерии
Формулы изомеров
По углеродному скелету начиная с С 4
межклассовая с кетонами, начиная с С3
непредельными спиртами и простыми эфирами (с С3)
13
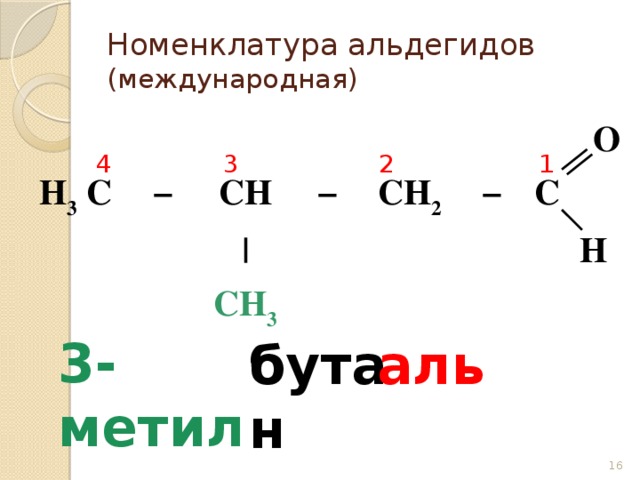
Номенклатура альдегидов (международная)
H 3 C
−
CH
−
|
CH 3
CH 2
−
O
C
H
4
3
2
1
3-метил
бутан
аль
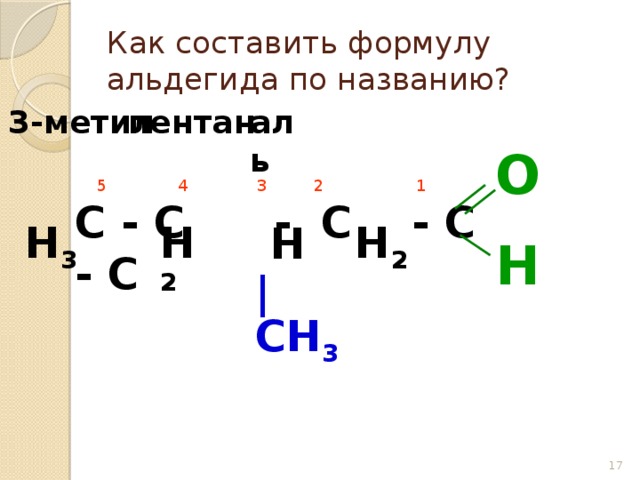
Как составить формулу альдегида по названию?
пентан
аль
3-метил
O
H
5 4 3 2 1
H
С - С - С - С - С
H 3
H 2
H 2
|
CH 3
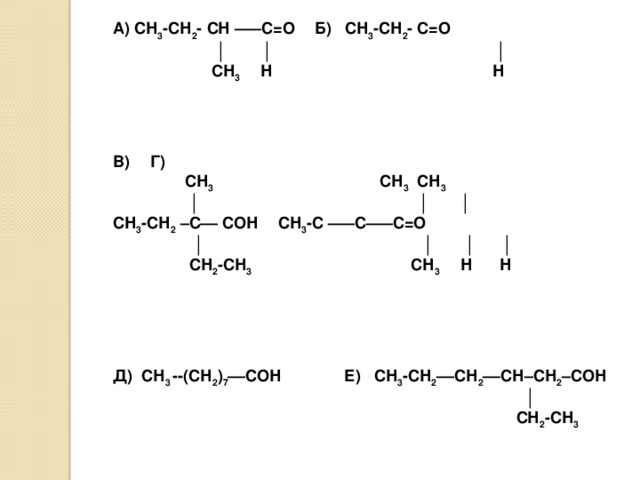
А) СН 3 -СН 2 - СН –––С=О Б) СН 3 -СН 2 - С=О
│ │ │
СН 3 Н Н
В) Г)
СН 3 СН 3 СН 3
│ │ │
СН 3 -СН 2 –С–– СОН СН 3 -С –––С–––С=О
│ │ │ │
СН 2 -СН 3 СН 3 Н Н
Д) СН 3 --(СН 2 ) 7 ––СОН Е) СН 3 -СН 2 ––СН 2 ––СН–СН 2 –СОН
│
СН 2 -СН 3

Взаимодей-ствие
Реакции
Гидриро
Окисление
Реакция «серебряно-
Соединение одинаковых молекул
Взаимодей-ствие
Реакции поликонденсации
Гидриро
Окисление
Реакция «серебряно-
Соединение одинаковых молекул
Химические свойства альдегидов
Соединение одинаковых молекул
Реакции восстановления
Гидриро
Окисление
Реакция «серебряно-
Соединение одинаковых молекул
Взаимодей-ствие
Реакции окисления
Гидриро
Окисление
Реакция «серебряно-
Взаимодей-ствие
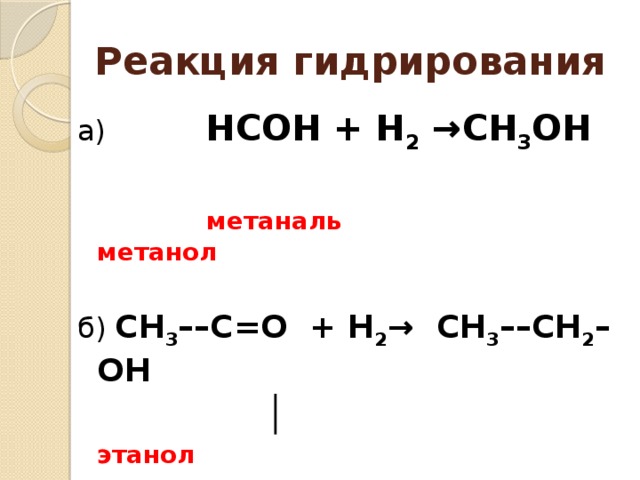
Реакция гидрирования
а) НСОН + Н 2 →СН 3 ОН
метаналь метанол
б) СН 3 ––С=О + Н 2 → СН 3 ––СН 2 – ОН
│ этанол
Н
этаналь

Реакция «серебряного зеркала» - взаимодействие с аммиачным раствором оксида серебра
НСОН + Аg 2 O → НСООН + 2 Аg↓
муравьиный муравьиная
альдегид кислота

Окисление гидроксидом меди (II)
НСОН + 2Cu(OH) 2 → НСООН+ 2 CuOH + Н 2 О
муравьиный муравьиная желтый
альдегид кислота ↓
Cu 2 O+ Н 2 О
красный
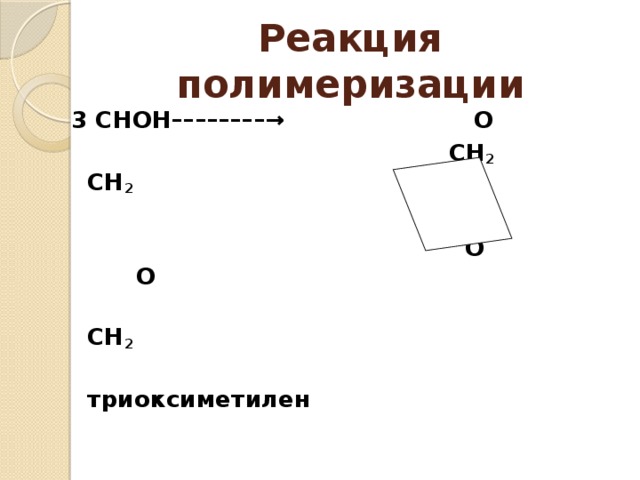
Реакция полимеризации
3 СНОН––––––––→ О
СН 2 СН 2
О О
СН 2
триоксиметилен
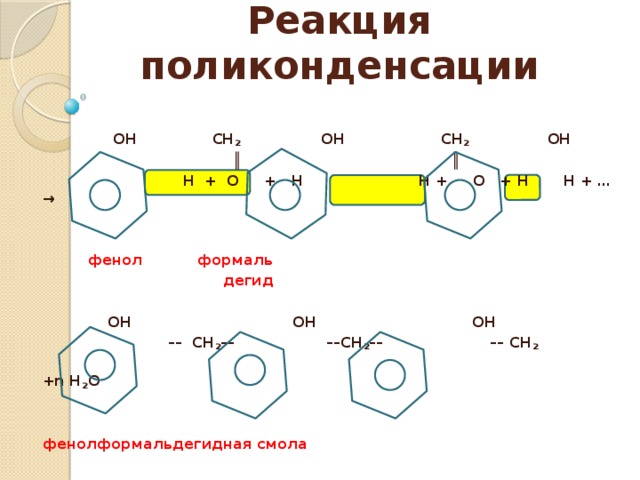
Реакция поликонденсации
ОН СН 2 ОН СН 2 ОН
║ ║
Н + О + Н Н + О + Н Н + …→
фенол формаль
дегид
ОН ОН ОН
–– СН 2 –– ––СН 2 –– –– СН 2
+n Н 2 О
фенолформальдегидная смола

Горение альдегидов
2CH 3 CHO + 5O 2 → 4CO 2 + 4H 2 O
этаналь
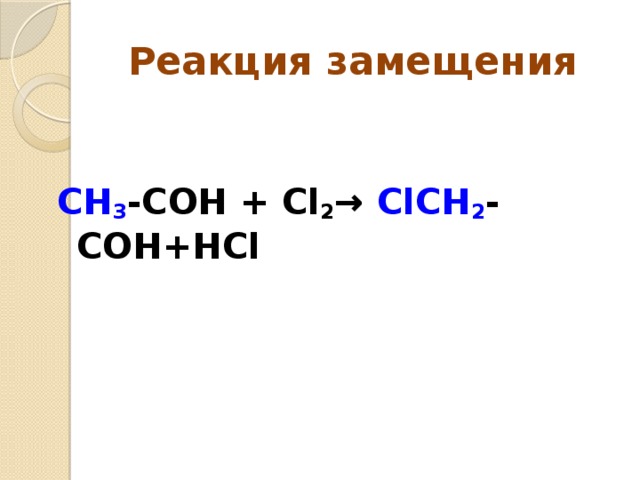
Реакция замещения
СН 3 -СОН + Cl 2 → ClСН 2 -СОН+НCl
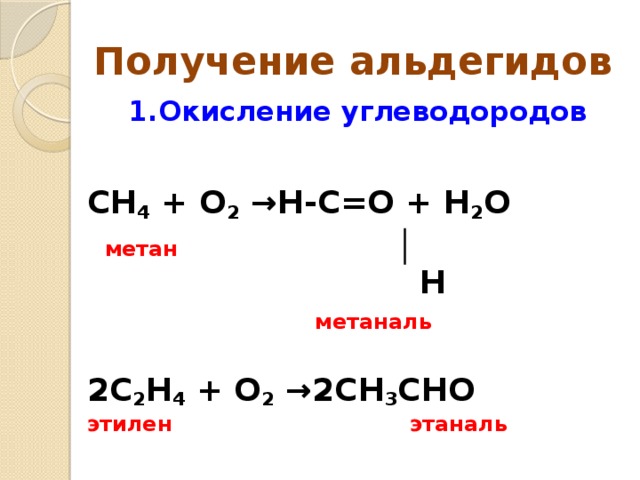
Получение альдегидов
1.Окисление углеводородов
CH 4 + O 2 → H-C=O + H 2 O
метан │ Н метаналь 2C 2 H 4 + O 2 → 2CH 3 CHO этилен этаналь
![2.окисление первичных спиртов СН 3 -СН 2 -СН 2 ОН [ О]→ СН 3 -СН 2 -С=О + Н 2 О пропанол-1 │ Н пропаналь 2. CH 3 OH + CuO → HCHO + Cu + H 2 O метанол метаналь](https://fsd.multiurok.ru/html/2017/02/10/s_589dcfbea4915/img27.jpg)
2.окисление первичных спиртов
- СН 3 -СН 2 -СН 2 ОН [ О]→ СН 3 -СН 2 -С=О + Н 2 О
пропанол-1 │
Н
пропаналь 2. CH 3 OH + CuO → HCHO + Cu + H 2 O
метанол метаналь

Интересная справка!
При употреблении алкогольных напитков большую опасность, чем этанол, представляет уксусный альдегид, который образуется при окислении этого спирта.
Уксусный альдегид в 30 раз токсичнее спирта. Он вызывает изменения коры головного мозга, на уровне ДНК. Это приводит к возникновению мутаций и различным видам уродств у эмбрионов, а так же появлению генов алкоголизма, психических заболеваний.
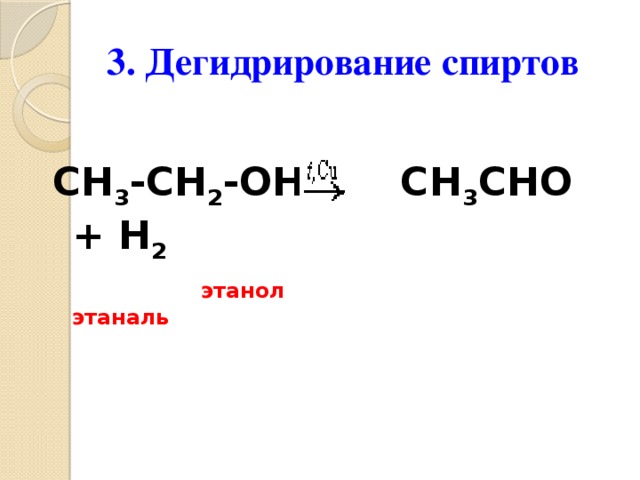
3. Дегидрирование спиртов
CH 3 -CH 2 -OH CH 3 CHO + H 2
этанол этаналь
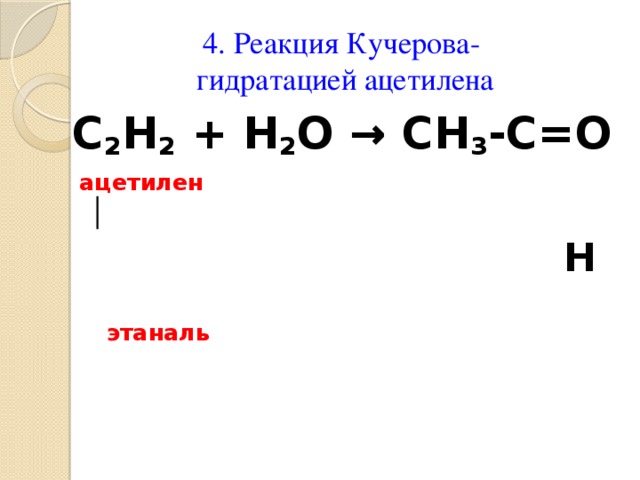
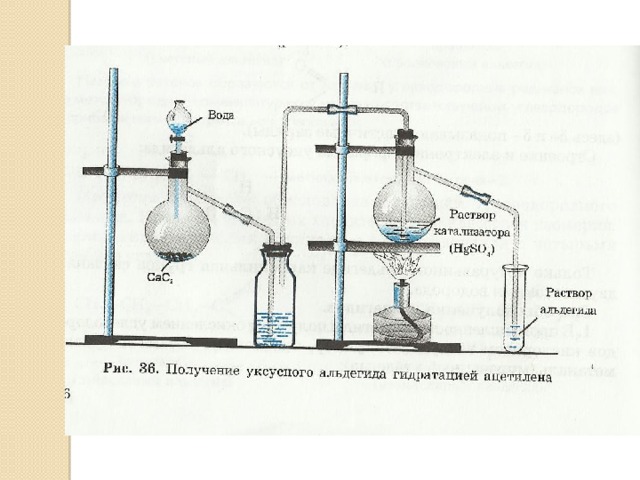
4. Реакция Кучерова- гидратацией ацетилена
С 2 Н 2 + Н 2 О → СН 3 -С=О
ацетилен │
Н
этаналь

Применение альдегидов
Булочки ванильные, корицы аромат,
Амаретто, шоколад
Альдегидов вкус таят
В землянике и кокосе
И в жасмине и в малине
И в духах и в еде
Альдегидов след везде.
Что за запах, что за прелесть,
И откуда эта свежесть?
Это высший альдегид
Аромат вам свой дарит.


Ацетальдегид
Ацетатное волокно
пластмасса
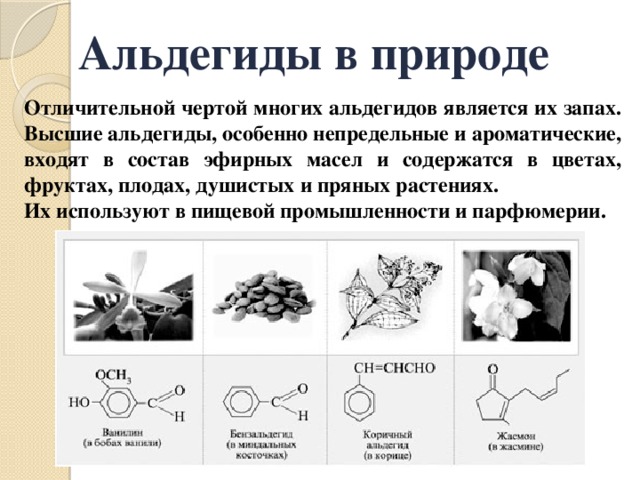
Альдегиды в природе
Отличительной чертой многих альдегидов является их запах. Высшие альдегиды, особенно непредельные и ароматические, входят в состав эфирных масел и содержатся в цветах, фруктах, плодах, душистых и пряных растениях.
Их используют в пищевой промышленности и парфюмерии.
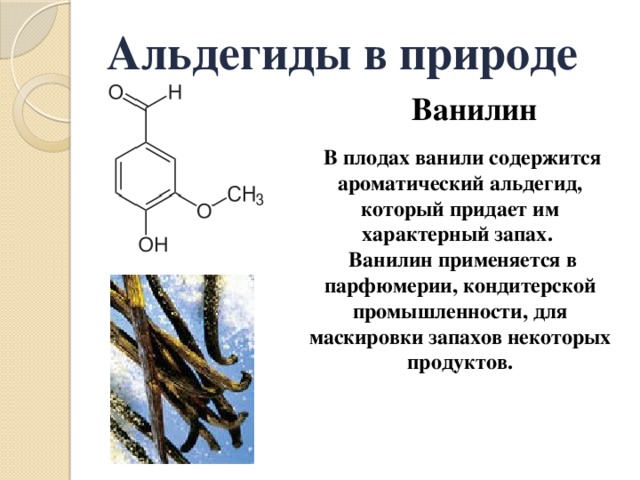
Альдегиды в природе
Ванилин
В плодах ванили содержится ароматический альдегид, который придает им характерный запах.
Ванилин применяется в парфюмерии, кондитерской промышленности, для маскировки запахов некоторых продуктов.

Альдегиды в природе
Цитраль
Запах цитрусовых обусловлен данным диеновым альдегидом. Его применяют в качестве отдушки средств бытовой химии, косметических и парфюмерных веществ.
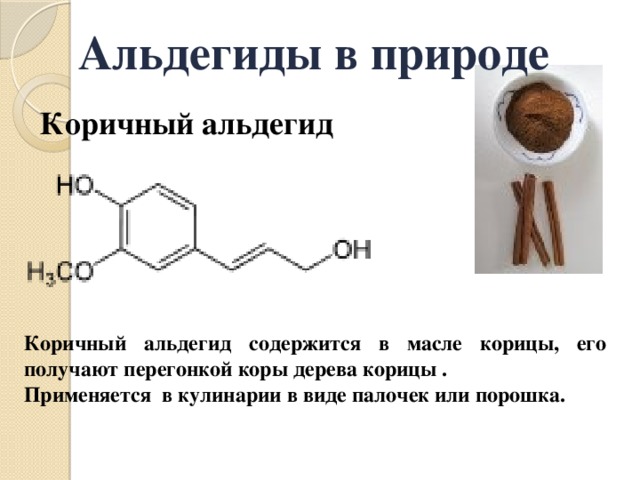
Альдегиды в природе
Коричный альдегид
Коричный альдегид содержится в масле корицы, его получают перегонкой коры дерева корицы .
Применяется в кулинарии в виде палочек или порошка.
Альдегиды в природе
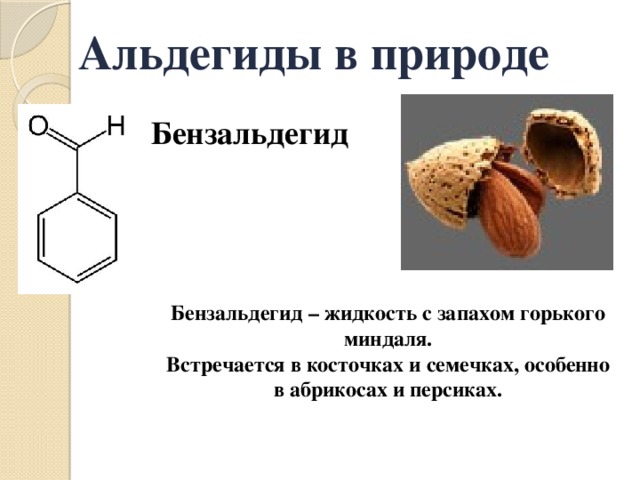
Бензальдегид
Бензальдегид – жидкость с запахом горького миндаля.
Встречается в косточках и семечках, особенно в абрикосах и персиках.

Альдегиды в природе
Фенилэтаналь
Фенилэтаналь по сравнению с бензальдегидом лучше соответствует рецептору цветочного запаха.
Фенилэтаналь пахнет гиацинтом.
Кетоны в природе
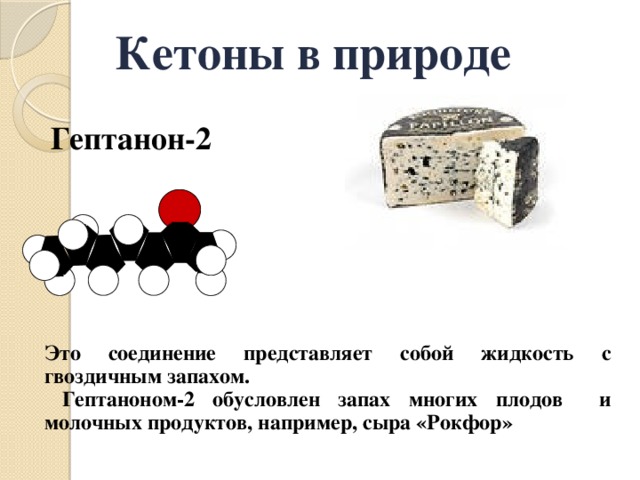
Гептанон-2
Это соединение представляет собой жидкость с гвоздичным запахом.
Гептаноном-2 обусловлен запах многих плодов и молочных продуктов, например, сыра «Рокфор»

Кетоны в природе
n-Гидроксифенилбутанон-2
Этот кетон обуславливает в основном запах спелых ягод малины.
Его включают в состав синтетических душистых композиций


































![2.окисление первичных спиртов СН 3 -СН 2 -СН 2 ОН [ О]→ СН 3 -СН 2 -С=О + Н 2 О пропанол-1 │ Н пропаналь 2. CH 3 OH + CuO → HCHO + Cu + H 2 O метанол метаналь](https://fsd.multiurok.ru/html/2017/02/10/s_589dcfbea4915/img27.jpg)


































