Презентация к уроку: "Металлы побочной подгруппы. Железо".
Цель и задачи урока:
•формирования у учащихся представлений о физических и химических свойствах железа как химического элемента побочной подгруппы, о его важнейших природных соединениях. (предметный результат)
•формирования у учащихся умения генерировать идеи, выявлять причинно-следственные связи, умения пользоваться схемами и моделями, формирования умений анализировать факты при наблюдении и объяснении явлений, умения работать с информационными ресурсами, умений работать с лабораторным оборудованием, умений работать индивидуально и в команде. (метапредметный результат)
•формирования навыков практического и аналитического решения поставленных или самостоятельно сформулированных задач. (метапредметный результат)
•формирования умений управлять своей учебной деятельностью, развитие внимания, памяти, логического и творческого мышления. (личностный результат)

Просмотр содержимого документа
«Презентация к уроку: "Металлы побочной подгруппы. Железо".»




«Загадка»:
- Очень древний я металл, Счёт столетьям потерял. Был нескромным я не в меру, Тысячи лет до нашей эры. А за блеск, мерцавший холодом, Люди там платили золотом!
- Я давно в названии века, В организме человека. Называют мной характер, Из меня почти весь трактор. Очень в яблоке полезно, И зовут меня …
(Железо).

Тема урока: Железо.
Железо не только основа всего мира, самый главный металл окружающей нас природы, оно основа культуры и промышленности, оно орудие войны и мирного труда. И трудно во всей таблице Менделеева найти другой такой элемент, который был бы так связан с прошлыми, настоящими и будущими судьбами человечества.
Академик А.Е.ФЕРСМАН

Цель урока: Познакомится с элементом побочной подгруппы – железом: его историей, строением атома, физическими и химическими свойствами, нахождением в природе.
Положение металла в ПСХЭ Д.И.Менделеева
История металла
Строение .
Нахождение в природе
Fe
Биологическая роль
Физические свойства
Химические свойства
Применение

- История.
- прослушайте сообщения учащихся, ответьте на вопрос:
- Почему железо имеет такое историческое значение для развития цивилизации, что одна из эпох названа железным веком?

2. Положение металла в ПСХЭ. Строение.
- Работая в паре, определите местоположение элемента в Периодической системе, составьте электронную формулу атома. Сделайте записи в тетради.
- Порядковый номер:
- Период:
- Группа:
- Подгруппа:
- Электронная формула атома:
- Тип кристаллической решетки:
- Вид химической связи:

- 3.Нахождение в природе.
- Задание: 1. Назвать важнейшие руды и минералы, содержащие железо. Для работы воспользуйтесь физической картой учебника и информационными ресурсами: http://files.school-collection.edu.ru/dlrstore/0ab8f177-4185-11db-b0de-0800200c9a66/ch09_04_06.jpg
2. Показать важнейшие месторождения на карте. 3. Заполнить таблицу.
Название минерала
Формула
Важнейшие месторождения

- 4 . Физические свойства простого вещества.
- Задание: определить и доказать физические свойства железа:
- Оборудование : гвоздь с ниткой, стакан на 100 мл. с водой, железная стружка, магнит, провод (кусочек). Проведя опыты, заполните таблицу:
Цвет:
Запах:
Металлический блеск:
Твердость:
Пластичность:
Теплопроводность:
Электропроводность:
Магнитные свойства
Плотность:
Температура плавления:

5 . Химические свойства простого вещества.
- Задание: Изучить химические свойства железа. Проделайте опыты, составьте уравнения химических реакций железа с соляной кислотой. Сделайте выводы. Результаты запишите в таблицу. Если затрудняетесь в написании уравнений, обратитесь к учебнику.
- Реактивы и оборудование : пробирки, Fe(порошок), S , CuSO 4 , HCl, , железный гвоздь. Исходя из знаний о химических свойствах металлов, как вы думаете, какими химическими свойствами будет обладать железо +2, +3 ? Проводится эксперимент.
- Правила безопасности . Соблюдайте осторожность при работе с растворами кислот и щелочей. При нагревании прогревайте сначала всю пробирку. Направляйте ее отверстие в сторону от себя и соседей.

- Опыт 1. Взаимодействие железа с раствором медного купороса.
- В пробирку поместите железный гвоздь на нитке. Добавьте 1мл. медного купороса. Объясните наблюдаемое. Составьте уравнение химической реакции.
- Опыт 2. Взаимодействие железа с соляной кислотой.
- В пробирку поместите стружку железа. Добавьте 1 мл соляной кислоты.
- Объясните наблюдаемое. Составьте уравнение химической реакции.
- Опыт 3. Взаимодействие железа с кислородом.
- Видеоопыт. http://files.school-collection.edu.ru/dlrstore/d77a30af-8cff-11db-b606-0800200c9a66/x11_056.wmv
- Опыт 4. Взаимодействие железа с хлором.
- Видеоопыт: http://files.school-collection.edu.ru/dlrstore/44d91229-d534-4874-b849-86a0a19c7e66/056.wmv

Подведем итог:
Химические свойства:
1. Взаимодействие с простыми веществами - неметаллами .
Fe + S= FeS (при нагревании)
2Fe +3Cl 2 = 2FeCl 3
3 Fe +2 O 2 = Fe 3 O 4 ( Fe 2 O 3 FeO ) –раскаленное железо сгорает в кислороде с образованием железной окалины.
2. На воздухе железо легко окисляется – ржавеет (25% железа гибнет от коррозии)
.4 Fe +6 H 2 O + 3 O 2 4 Fe ( OH ) 3
3. С разбавленными кислотами HCl
Fe + 2 HCl = FeCl 2 + H 2
4 . С солями , если металл соли находится в ряду активности правее железа
Fe + CuSO 4 = FeSO 4 + Cu (учащиеся опускают привязанный на нитке гвоздь в водный р-р CuSO 4 )
5. С водой 3 Fe + 4H 2 O (пары) = Fe 3 O 4 + 4H 2 при температуре 700-900 о С . Эту реакцию использовал Лавуазье для получения водорода.
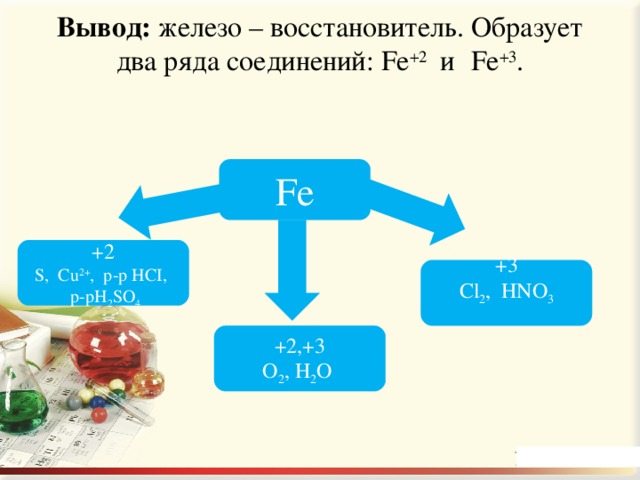
Вывод: железо – восстановитель. Образует два ряда соединений: Fe +2 и Fe +3 .
Fe
+2
S, Cu 2+ , p- р HCI,
p- р H 2 SO 4
+ 3
Cl 2 , HNO 3
+2 , + 3
O 2 , H 2 O

2.Стадия осмысления: работа по программам деятельности
6. Биологическая роль железа.
Задание: прочитайте текст, заполните таблицу.
Какова роль железа в жизни человека и растений?
- Сообщая учащимся информацию о биологической роли железа для организма человека – реализуется принцип экологизации.
Для человека
Для растений

Применение
Задание: воспользуйтесь информационными ресурсами и укажите области применения железа и его сплавов. Составьте схему:
Fe


Железо взаимодействует с концентрированными кислотами H 2 SO 4 и HNO 3 .
Железо легко куется.
Ошибка
Железо взаимодействует с разбавленными кислотами.
Железо – это активный щелочной металл.
Ошибка
Температура плавления железа - 1539 0 С
На внешнем энергетическом уровне атома железа два электрона, следовательно, это элемент II группы
Ошибка
Ошибка
Атомы железа проявляют восстановительные свойства.
М аксимальная степень окисления железа равна номеру группы, в которой находится, то есть +8.

- Вернемся к теме сегодняшнего урока.
- Какие цели мы поставили в начале его?
- Удалось ли нам их выполнить?
- К какому выводу вы пришли?
- Сегодня я понял (а), что……….
- Главным на уроке для меня было………
- Больше всего мне запомнилось………….

- Вопросы для всех:
- В чем состоит главное отличие в строении атома железа от атомов металлов, изученных ранее?
- Можно ли железо назвать элементом с постоянной степенью окисления? Сколько электронов может отдавать атом железа при взаимодействии с окислителями? От чего это зависит?
- Какова распространенность железа в природе? Какие железные руды вы можете назвать?
- Химически чистое железо практически не подвергается коррозии на воздухе. Почему же так быстро ржавеют железные гвозди, болты, трубы и другие изделия?
- Концентрированные серную и азотную кислоты перевозят в стальных баллонах, не опасаясь их разрушения. Почему?
- С помощью каких реагентов можно обнаружить присутствие в растворе ионов Fe 2+ и Fe 3+ ?
- Какие продукты питания наиболее богаты железом?

- Задачи для желающих подумать:
- Близ города Дели в Индии стоит железная колонна без малейшего пятнышка ржавчины, хотя ее возраст 2800 лет. Это знаменитая Кутубская колонна высотой 7 м и массой 6,5 т. Надпись на колонне говорит о том, что она была поставлена в 9 веке до н.э. Чем объяснить ее долговечность и коррозионную стойкость? (Колонна была изготовлена из чистого металла: железа в колонне оказалось 99,72 %. Как удалось получить такой чистый металл в то время до сих пор загадка).
- Чтобы обнаружить примеси железа в платиновой посуде, например, чашке, ее нагревают до температуры красного каления. Тогда ее поверхность покрывается красным налетом. С чем связано появление налета? Как удалить этот налет не повредив изделие?

- http://pedsovet.su/load/420-1-0-29379 - шаблон презентации
- http://icache2.rutraveller.ru/icache/place/7/001/701_340x340.jpg
- http://s00.yaplakal.com/pics/pics_original/4/0/9/4661904.jpg
- http://www.motto.net.ua/pic/201209/1280x768/motto.net.ua-7741.jpg
- http://rushkolnik.ru/tw_files2/urls_3/99/d-98018/98018_html_35fad88.jpg
- http://files.school-collection.edu.ru/dlrstore/0ab8f177-4185-11db-b0de-0800200c9a66/ch09_04_06.jpg
- http://files.school-collection.edu.ru/dlrstore/d77a30af-8cff-11db-b606-0800200c9a66/x11_056.wmv
- http://files.school-collection.edu.ru/dlrstore/44d91229-d534-4874-b849-86a0a19c7e66/056.wmv















































