
Какова тема урока?

Кислоты, их классификация и свойства в свете ТЭД
Взаимодействие кислот
с оксидами ме, основаниями, солями

Цель: повторить химические свойства кислот, ликвидировать индивидуальные пробелы в знаниях, отработать навык составления молекулярных и ионных уравнений и решения задач

Выберите формулы кислот
NaСl, HCl, P 2 O 5 , NaOH, S, H 2 S, SO 2 , CaO, H 2 SO 3 , P, H 3 PO 4 , Ca, Na 2 O, HF, HI, Ca(OH) 2 , HBr, Na 2 SO 3 , HNO 2 , HCN, Ca 3 (PO 4 ) 2
HClO 4 , NaH 2 PO 4

Выберите формулы кислот, дайте названия
NaСl, HCl, P 2 O 5 , NaOH, S, H 2 S, SO 2 , CaO, H 2 SO 3 , P, H 3 PO 4 , Ca, Na 2 O, HF, HI, Ca(OH) 2 , HBr, Na 2 SO 3 , HNO 2 , HCN, Ca 3 (PO 4 ) 2
HClO 4 , NaH 2 PO 4

Химическая игра
1) Название кислоты
2) формула кислоты
3) название солей этой кислоты. Новая кислота
…

Повторение: азотная HNO 3 нитраты азотистая HNO 2 нитриты соляная= хлороводородная HCl хлориды серная H 2 SO 4 сульфаты сернистая H 2 SO 3 сульфиты сероводородная H 2 S сульфиды бромоводородная HBr бромиды йодоводородная HI йодиды фтороводородная HF фториды угольная H 2 CO 3 карбонаты кремниевая H 2 SiO 3 силикаты фосфорная H 3 PO 4 фосфаты
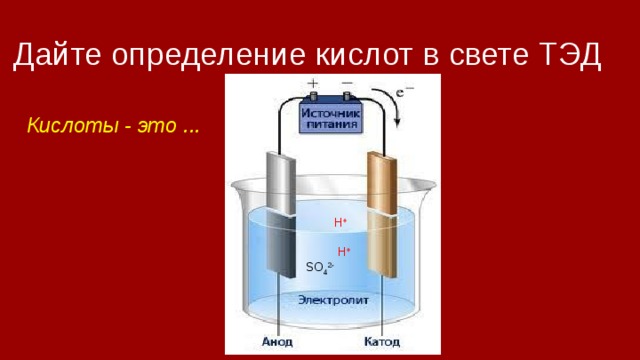
Дайте определение кислот в свете ТЭД
Кислоты - это ...
H +
H +
SO 4 2-
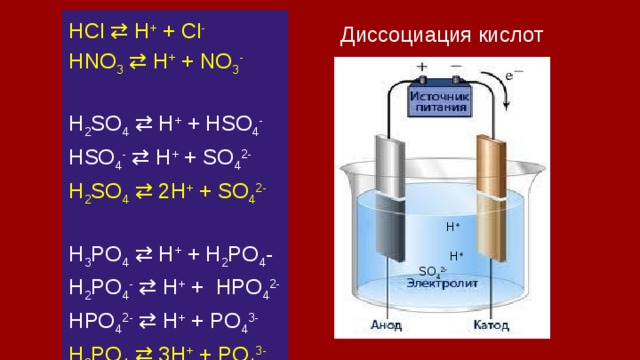
HCl ⇄ H + + Cl -
HNO 3 ⇄ H + + NO 3 -
H 2 SO 4 ⇄ H + + HSO 4 -
HSO 4 - ⇄ H + + SO 4 2-
H 2 SO 4 ⇄ 2H + + SO 4 2-
H 3 PO 4 ⇄ H + + H 2 PO 4 -
H 2 PO 4 - ⇄ H + + HPO 4 2-
HPO 4 2- ⇄ H + + PO 4 3-
H 3 PO 4 ⇄ 3H + + PO 4 3-
Диссоциация кислот
H +
H +
SO 4 2-

Химические свойства р-ров кислот
- H + изменяют цвет индикатора.
Почему к данному уроку выбран красный фон для презентации?

Химические свойства р-ров кислот
2. С ме (до Н) → соль + H 2 ↑
0 0
Zn + 2 HCl → ZnCl 2 + H 2 ↑

Химические свойства р-ров кислот
2. С ме (до Н) → соль + H 2 ↑
0 0
Zn + 2 HCl → ZnCl 2 + H 2 ↑
0 0
Zn + 2H + + 2Cl - → Zn 2+ +2Cl - + H 2 ↑

Химические свойства р-ров кислот
2. С ме (до Н) → соль + H 2 ↑
0 0
Zn + 2 HCl → ZnCl 2 + H 2 ↑
0 0
Zn + 2H + + 2Cl - → Zn 2+ +2Cl - + H 2 ↑
0 0
Zn + 2H + → Zn 2+ + H 2 ↑

Химические свойства р-ров кислот
3. С основными оксидами → соль + H 2 О
СuO + 2 HCl → CuCl 2 + H 2 O
CuO + 2H + + 2Cl - → Cu 2+ +2Cl - + H 2 O
CuO + 2H + → Cu 2+ + H 2 O

Химические свойства р-ров кислот
4. С основаниями → соль + H 2 О
Сa(OН) 2 + 2 HCl → CaCl 2 + 2H 2 O
Ca 2+ + 2OH - + 2H + + 2Cl - → Ca 2+ +2Cl - + 2H 2 O
2OH - + 2H + → 2H 2 O
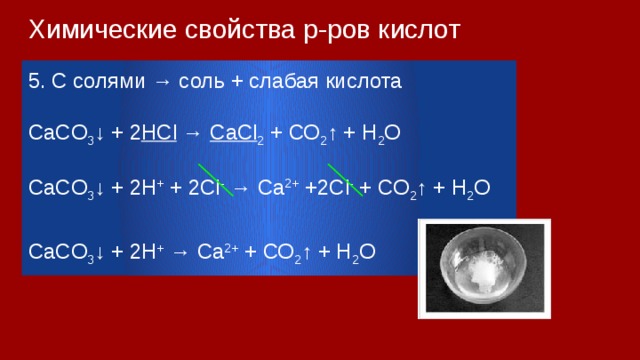
Химические свойства р-ров кислот
5. С cолями → соль + слабая кислота
СaСO 3 ↓ + 2 HCl → CaCl 2 + СО 2 ↑ + H 2 O
СaСO 3 ↓ + 2H + + 2Cl - → Ca 2+ +2Cl - + СО 2 ↑ + H 2 O
СaСO 3 ↓ + 2H + → Ca 2+ + СО 2 ↑ + H 2 O
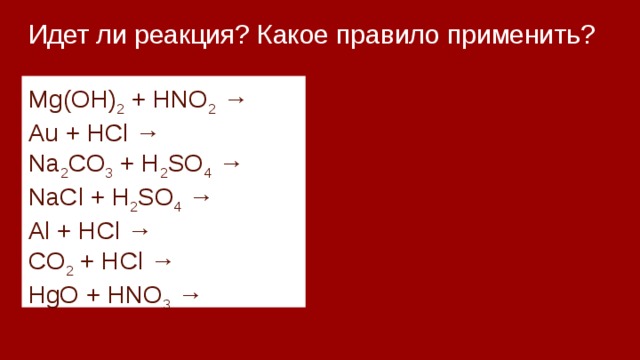
Идет ли реакция? Какое правило применить?
Mg(OH) 2 + HNO 2 →
Au + HCl →
Na 2 CO 3 + H 2 SO 4 →
NaCl + H 2 SO 4 →
Al + HCl →
CO 2 + HCl →
HgO + HNO 3 →

Оцените СВОИ результаты работы
- Теперь я - ас! Могу давать консультации по этой теме
- Славно поработал, но еще есть непонятные нюансы (тонкости)
- Я очень старался, частично понял, но остается еще много сложного. Думаю, в работе найдут много ошибок.
- Ничего не понял! Будто урок проводили на китайском языке!











































