26 октября:
Металлическая связь.
Водородная связь.


Проверочная работа

1. КПС в веществе, формула которого:
1)H 2 O
2)O 2
3)NaCl
4)Mg

2. Химическая связь в бромиде кальция:
1)ИС
2)КПС
3)КНПС

3.Химическая связь, возникающая за счет образования общих электронных пар между атомами с незначительно отличающимися электроотрицательностями:
1)ИС
2)КПС
3)КНПС

4. Химическая связь в хлороводороде:
1)ИС
2)КПС
3)КНПС

5. В каком из веществ имеется и ионная и ковалентная полярная связь одновременно:
1) H 2 SO 4
2) HClO 3
3)NaOH
4)C 2 H 5 OH

6. Вещество хорошо растворимо в воде и его раствор проводит электрический ток. Вещество обладает высокой температурой плавления, очень твёрдое. У этого вещества кристаллическая решётка:
1)Атомная
2)Ионная
3)Молекулярная

7. Кристаллическая решётка льда:
1)Атомная
2)Ионная
3)Молекулярная

8 . На какой схеме приведён донорно-акцепторный механизм образования ковалентной связи:
1)А + В A B
2) А + В A B
3) А + В A B

9.По кратности ковалентную связь можно классифицировать как:
1)Полярную и неполярную
2)Одинарную и двойную
3)Обменная и донорно-акцепторная

10. Верны ли следующие суждения:
А) Электроотрицательность – это способность атомов отдавать свои валентные электроны
Б) Ионная связь образуется между атомами с резко отличающимися электроотрицательностями.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны

Ответы
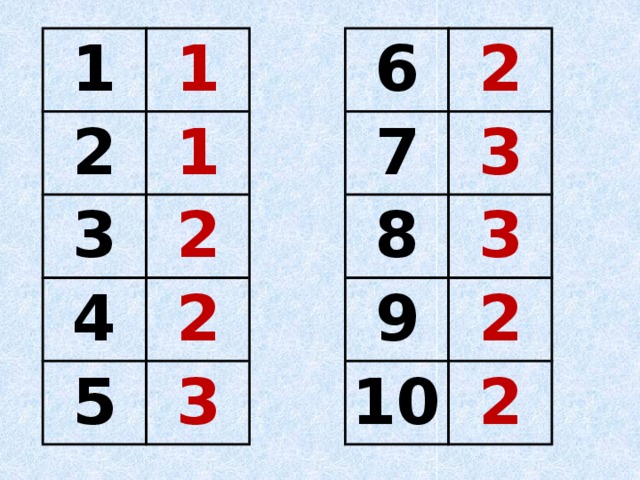
1
6
2
1
7
2
3
1
3
8
2
3
4
9
2
5
2
10
3
2
..
..
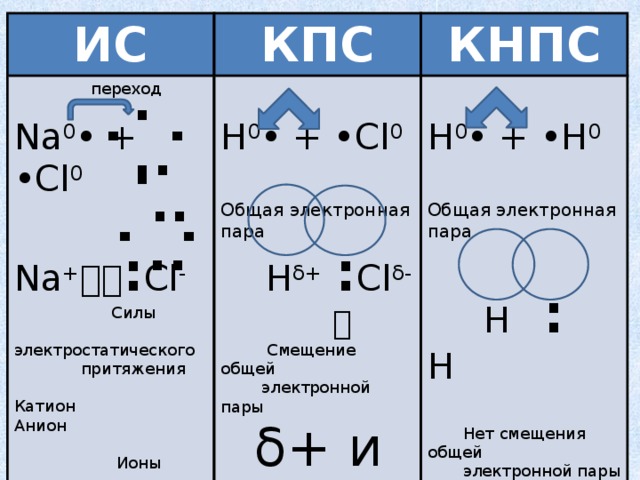
ИС
переход
КПС
Металл-неметалл
КНПС
Неметалл-неметалл
Na 0 • + •Cl 0
H 0 • + •Cl 0
Простые вещества неметаллы
Na + : Cl -
Общая электронная пара
H 0 • + •H 0
H δ+ : Cl δ-
Силы
Общая электронная пара
электростатического
Смещение общей
притяжения
электронной пары
H : H
δ+ и δ-
Катион Анион
Частичные заряды
Нет смещения общей
Ионы
электронной пары
..
..
..
..
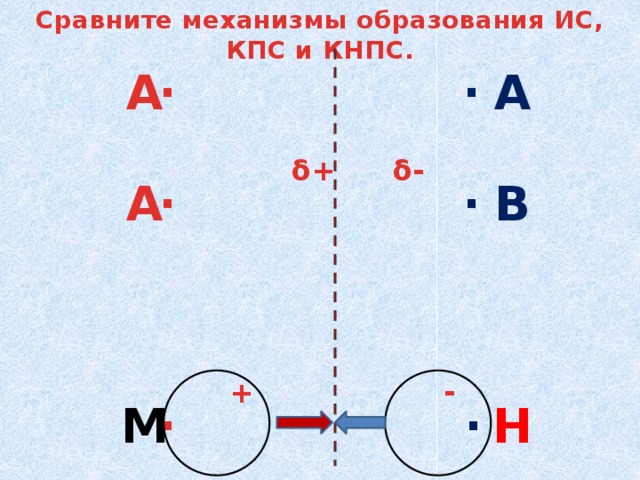
Сравните механизмы образования ИС, КПС и КНПС.
А
А
·
·
δ-
δ+
В
·
А
·
-
+
M
·
H
·

Металлическая связь – это связь в металлах и их сплавах, которая осуществляется относительно свободными валентными электронами между атомами и ионами (атом-ионами) металлов.

Металлическая кристаллическая решётка – это кристалл в узлах которого находятся атомы или ионы металла между которыми перемещаются относительно свободные валентные электроны.



Особенности атомов металлов:
- На внешнем уровне 1-3 электронов.
- Большой радиус атома.
- Большое число свободных орбиталей.
- При сближении атомов металлов свободные орбитали перекрываются и валентные электроны свободно перемещаются по ним.

- Атомы металла превращаются в ионы, а ионы в атомы – постоянный процесс в металлах: Ме 0 – ē Me +
- Совокупность относительно свободных валентных электронов металлов обеспечивают связь между атомами и ионами металлов.


Металлический блеск

Электропроводность

Теплопроводность

Пластичность, ковкость
4. Механическое воздействие на кристалл с металлической связью вызывает смещение слоёв атомов, однако, благодаря перемещению электронов по всему кристаллу, разрыв связей не происходит. Для металлов характерна высокая пластичность. Золото, например, можно прокатывать в листы толщиной не более 0,003 мм, которые используются для позолоты различных предметов.

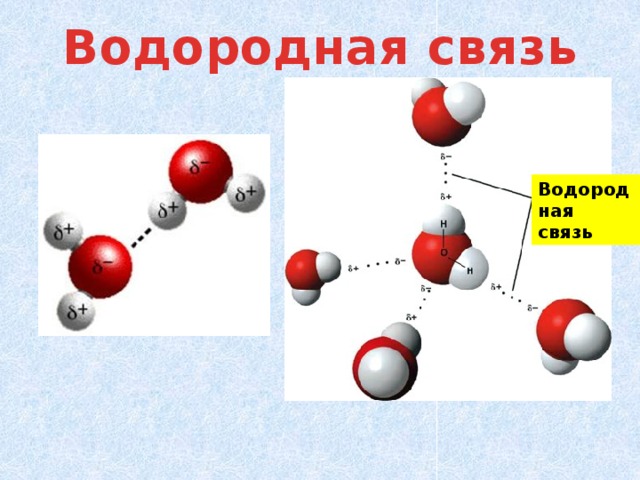
Водородная связь
Водородная связь
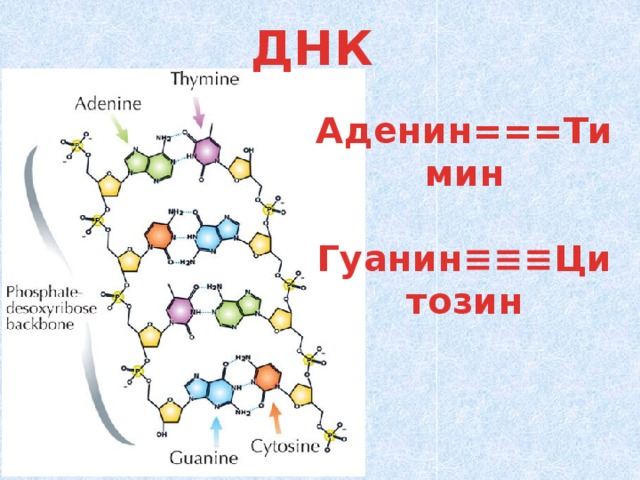
ДНК
Аденин===Тимин
Гуанин≡≡≡Цитозин
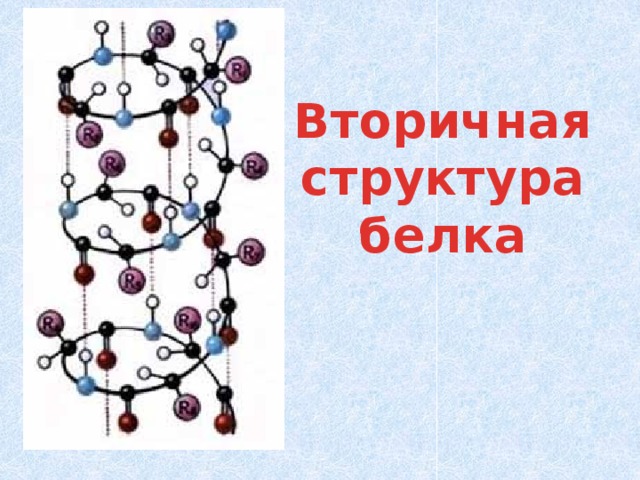
Вторичная структура белка

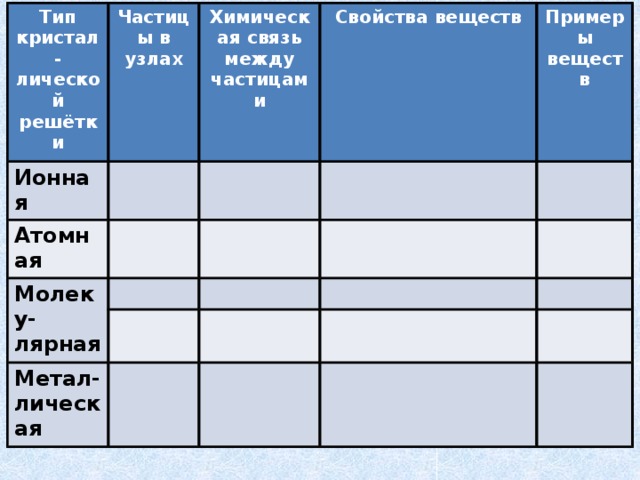
Тип кристал-лической решётки
Частицы в узлах
Ионная
Химическая связь между частицами
Атомная
Свойства веществ
Молеку-лярная
Примеры веществ
Метал-лическая
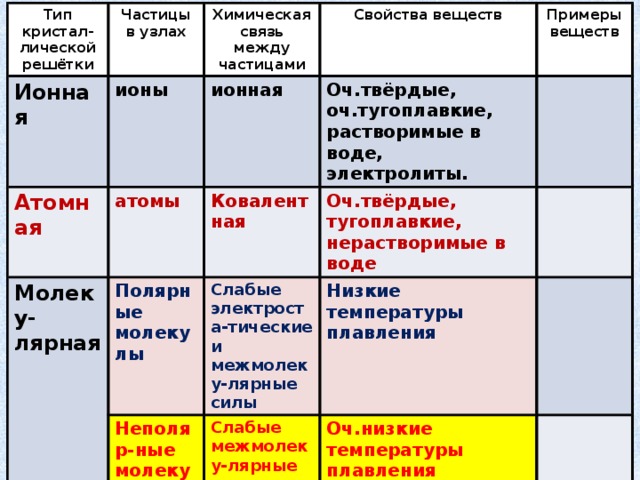
Тип кристал-лической решётки
Ионная
Частицы в узлах
Химическая связь между частицами
Атомная
ионы
Свойства веществ
ионная
атомы
Молеку-лярная
Ковалентная
Полярные молекулы
Примеры веществ
Оч.твёрдые, оч.тугоплавкие, растворимые в воде, электролиты.
Оч.твёрдые, тугоплавкие, нерастворимые в воде
Слабые электроста-тические и межмолеку-лярные силы
Неполяр-ные молекулы
Метал-лическая
Низкие температуры плавления
Слабые межмолеку-лярные силы
Атомы и ионы металла
Оч.низкие температуры плавления
Метал-лическая
Металлический блеск, тепло- и электропроводность, пластичность

Домашнее задание:
Учить § 5-6.
Ответить на вопросы в конце параграфов