План урока
Тэма “Будова атама. Ядро і электронная абалонка. Атамны нумар. Фізічны сэнс атамнага нумара”
Падрыхтавала: Бялько М.А.
Клас: 8
Дыдактычная мэта урока:
Па выніках вывучэння тэмы вучні павінны:
Ведаць ядзерную мадэль будовы атама, сучасную фармуліроўку азначэння атама.
Умець раскрываць фізічны сэнс атамнага нумара хімічнага элемента
Вызначаць колькасць пратонаў і электронаў у атаме.
Задачы асобаснага развіцця:
Садзеянне развіццю агульнаадукацыйных навыкаў самастойнай працы з падручнікас, схемай, аналізу і выкарыстанню вывучаемай інфармацыі
Фарміраванее інфармацыйных і камунікатыўных кампетэнцый праз выкарыстанне прэзентацыі і групавое выкананне заданняў.
Матэрыялы і абсталяванне: кампутар, прэзентацыя ўрока, раздатачныя матэрыялы (тэставае заданне па тэме “Перыядычная сістэма хімічных элементаў”)
Арганізацыйная хвіліна
1.Вітанне.
2.Праверка падрыхтоўкі класа да ўрока.
Этап матывацыі і тэмавызначэння.
Настаўнік: Сення мы з вамі працягваем удасканальваць свае веды прахімічныя элементы, а падрабязней пра атамы хімічных элементаў. Запішыце тэму ўрока ў сшыткі
“Будова атама. Ядро і электронная абалонка. Атамны нумар. Фізічны сэнс атамнага нумара”
Гледзячы на гэтую тэму, паспрабуйце самастойна сфармуляваць мэту ўрока, пачынаючы са слоў:
-Мы сення будзем вывучаць………
-А таксама будзем вучыцца прымяняць атрыманыя …… пры выкананні……
Актуалізацыя ведаў
Самастойнае выкананне тэставага задання па тэме “Перыядычная сістэма хімічных элементаў”
| 1.Гарызантальны рад хімічных элементаў называецца: А) група Б) падгрупа В) паўперыяд Г) перыяд 2.Вертыкальны рад хімічных элементаў у ПС называецца: А) група Б) падгрупа В) паўперыяд Г) перыяд 3.Кожны перыяд пачынаецца: А)высакародным газам Б)шчолачным металам В) вадародам Г)кожны раз па іншаму 4.Малымі перыядамі называюцца ўсе перыяды ў радзе: А) 1,5,7 Б) 1,2,4 В) 1,2,3 Г) 5,6,7 5.Шчолачныя металлы знаходзяцца ў: А) ІА групе Б) ІІА групе В) ІВ групе Г) VII групе | 6.Элементы VII групы называюць: А) шчолачнымі металамі Б) галагенамі В)высакароднымі газамі Г) халькагенамі 7. Укажыце правільнае становішча медзі ў перыядычнай сістэме: А) ІІ В група, 3 перыяд Б) І В група, 4 перыяд В) 11 група, 4 перыяд Г) І А група, 4 перыяд 8.Вышэйшая валентнасць элементу, як правіла роўная: А) нумару перыяда Б) нумару групы В) парадкаваму нумару Г) адноснай масе атама 9.Найбольш выражаныя металічныя ўласцівасці мае: А) Cu Б) Se В) Ca Г) Ti 10.Найбольш выражаныя неметалічныя ўласцівасці мае: А) F Б) Cl В) I Г) Br |
Вывучэнне новага матэрыялу
1.Прадмовы да адкрыцця складанай будовы атаму
Самастойная праца з падручнікам (с.132, 1 і 2 абзацы тэмы)
па заданню №1:
Адкажыце на пытанні:
1.Існаванне чаго ўстанавіў Д.Д. Томсан?
2.Што адкрыў Анры Бекерэль?
3.Дайце азначэнне тэрміну “электроны”
4.Дайце азначэнне тэрміну “радыеактыўнасць”
Абмеркаванне адказаў
Настаўнік: Наступнае пытанне з нашай тэмы—гэта будова атама
2.Ядзерная мадэль будовы атама
Заданне №2:
1.Замалюйце ў сшыткі схему мадэлі будовы атама
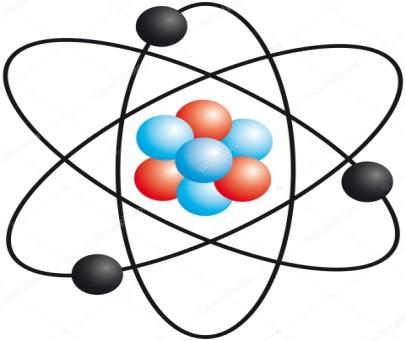
2.Прачытайце матэрыял на старонцы 132 падручніка і папоўніце схему адпаведнымі назвамі часцін




Дадатна зараджанае ядро
Адмоўныя электроны
3.Як вы лічыце, калі скласці дадатны зарад ядра і адмоўны зарад усіх электронаў вакол яго, то які агульны зарад будзе мець атам?
4.Зрабіце вывад аб будове атама, уставіўшы прапушчаныя словы ў выраз:
Атам—гэта …………… часціца, якая складаецца з дадатна зараджанага ….. і адмоўна зараджаных …………….. .
Фізкультхвілінка для спіны і рук
Настаўнік: Як вы даведаліся атам складаецца з ядра і электронаў, якія рухаюцца вакол яго. Але хачу звярнуць вашу ўвагу на малюнак яшчэ раз: паглядзіце на ядро, яно на малюнку складаецца з часцінак 2 тыпаў. Давайце запішам у сшытак:
Ядро складаецца з часціц(яны называюцца ядзернымі часціцамі або нуклонамі). Яны бываюць 2 тыпаў:
-пратоны (р) — маса =1, зарад= +1
-нейтроны (n) — маса =1, зарад= 0
Вынік: маса ядра складаецца з мас усіх ……... і ………, а зарад ядра залежыць толькі ад колькасці ……….. .
3.Атамны нумар і яго фізічны сэнс.
Запіс у сшыткі:
Фізічны сэнс атамнага нумара: атамны нумар элемента ў перыядычнай сістэме роўны зараду ядра яго атамаў.
| Атамны Зарад Лік Лік нумар = ядра = пратонаў = электронаў элемента атама у ядры у атаме |
Сумеснае выкананне задання з настаўнікам:
А) Хімічны элемент Са мае:
атамны нумар 20, значыць яго зарад +20, значыць у яго ядры 20р (пратонаў), а вакол ядра 20е- (электронаў)
Б) Хімічны элемент С (вуглярод) мае………………….
Замацаванне матэрыялу
Настаўнік: Цяпер давайце замацуем нашы веды пра фізічны сэнс атамнага нумару і будову атаму
Самастойнае выкананне задання 2, 3 на старонцы 135падручніка з самаправеркай і абмеркаваннем
С.135, заданне 2
N – зарад ядра +7 і 7 е-
Al - зарад ядра +13 і 13 е-
Fe - зарад ядра +26 і 26 е-
Br - зарад ядра +35 і 35 е-
Au - зарад ядра +79 і 79 е-
C.135 , заданне 3
8р: атамны № 8—гэта О (VI A група, 2 перыяд)
12 р: атамны № 12—гэта С (ІV A група, 2 перыяд)
29 р: атамны № 29—гэта Cu (IВ група, 4 перыяд)
47 р: атамны № 47—гэта Ag (IВ група, 5 перыяд)
80 р: атамны № 80—гэта Hg (II В група, 6 перыяд)
Падвядзенне вынікаў па ўроку:
Адкажыце на пытанні:
-Што мы сення вывучылі?
-Што навучыліся пабіць?
Дамашняе заданне і рэфлесія
§29,заданне 4
Калі матэрыял вам зразумелы, то падыміце ўверх абедзве рукі.
Калі ў вас узніклі пытанні, то адну руку.



























