Постулаты Бора. Модель атома водорода по Бору.

Постулаты Бора
Первый постулат Бора: атомная система может находится только в особых стационарных, или квантовых, состояниях, каждому из которых соответствует определенная энергия E n . В стационарном состоянии атом не излучает.
Нильс Бор
1885-1962
Постулат находится в противоречии с классической механикой (Энергия движущихся электронов может быть любой), с электродинамикой Максвелла, т.к. допускает возможность ускоренного движения без излучения электромагнитных волн.
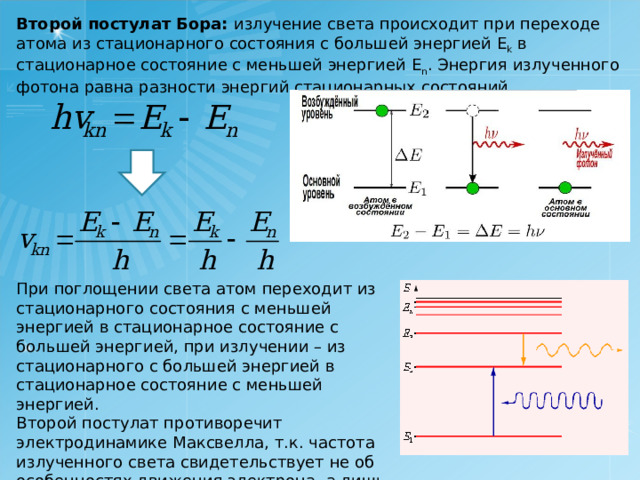
Второй постулат Бора: излучение света происходит при переходе атома из стационарного состояния с большей энергией E k в стационарное состояние с меньшей энергией E n . Энергия излученного фотона равна разности энергий стационарных состояний.
При поглощении света атом переходит из стационарного состояния с меньшей энергией в стационарное состояние с большей энергией, при излучении – из стационарного с большей энергией в стационарное состояние с меньшей энергией.
Второй постулат противоречит электродинамике Максвелла, т.к. частота излученного света свидетельствует не об особенностях движения электрона, а лишь об изменении энергии атома.
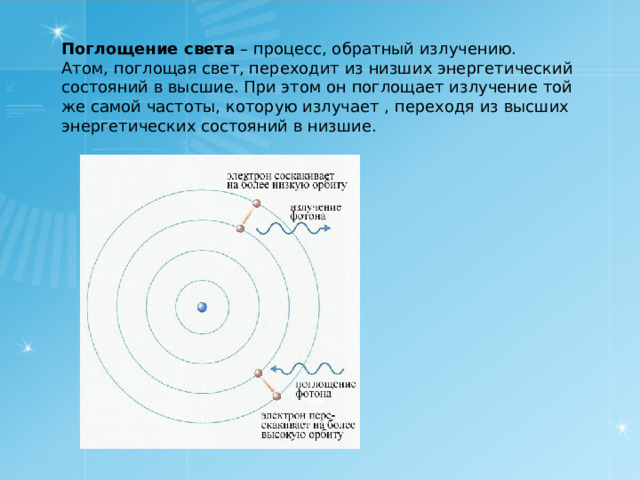
Поглощение света – процесс, обратный излучению.
Атом, поглощая свет, переходит из низших энергетический состояний в высшие. При этом он поглощает излучение той же самой частоты, которую излучает , переходя из высших энергетических состояний в низшие.

Модель атома водорода по Бору
Бор рассматривал простейшие круговые орбиты.
- потенциальная энергия взаимодействия электрона с ядром в абсолютной системе единиц. e – модуль заряда электрона, r – расстояние от электрона до ядра.
Произвольная постоянная, с точностью до которой определяется потенциальная энергия, принята равной нулю.
Wp , так как взаимодействующие частицы имеют заряды противоположных знаков.
E=E кин + W p – полная энергия атома.
- центростремительное ускорение по второму закону Ньютона сообщает электрону на орбите кулоновская сила.
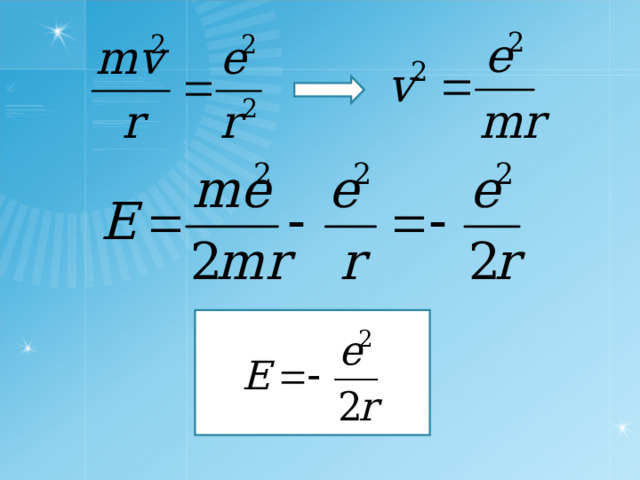

Правило квантования
Из первого постулата Бора энергия может принимать только определенное значение E n .
Электрон движется по круговой орбите, то
mvr – момент импульса в механике
- Постоянная Планка.
Бор предположил, что произведение модуля импульса на радиус орбиты кратно постоянной Планка.

Радиусы орбит
Радиусы боровских орбит меняются дискретно с изменением числа n .
Значения электронных орбит определяют:
Наименьший радиус орбиты:
Размеры атома определяются квантовыми законами (радиус пропорционален квадрату постоянной Планка). Классическая теория не может объяснить, почему атом имеет размеры порядка 10 -8 см.

Энергия стационарных состояний
- дискретные (прерывистые) значения
энергий стационарных состояний атома (энергетические уровни).

Низшее энергетическое состояние
Атом может находится сколь угодно долго.
Чтобы ионизировать атом водорода, ему нужно сообщить энергию 13,53 эВ – энергия ионизации.
Возбуждающий атом: n= 2, 3, 4, …
τ = 10 -8 с – время жизни в возбужденном состоянии. За время τ электрон успевает совершить около ста миллионов оборотов вокруг ядра.
 n . " width="640"
n . " width="640"
Излучение света
Возможные частоты излучения атома водорода:
- постоянная Ридберга R = 109737,316 см -1 .
где
Теория Бора приводит к количественному согласию с экспериментом для значений частот, излучаемых атомом водорода. Все частоты излучений атома водорода образуют ряд серий, каждому из которых соответствует определенное значение числа n и различные значения k n .

Спектральные серии водорода
Серия Лаймана – открыл в 1906 г. Теодор Лайман.
Данная серия образуется при переходах электронов с возбуждённых энергетических уровней на первый в спектре излучения и с первого уровня на все остальные при поглощении.
Серия Бальмера – открыл в 1885 г. Иоганн Бальмер. Данная серия образуется при переходах электронов с возбужденных энергетических уровней на второй в спектре излучения и со второго уровня на все вышележащие уровни при поглощении.
Серия Пашена – открыл в 1908 г. Фридрих Пашен.
Данная серия образуется при переходах электронов с возбужденных энергетических уровней на третий в спектре излучения и с третьего уровня на все вышележащие уровни при поглощении.











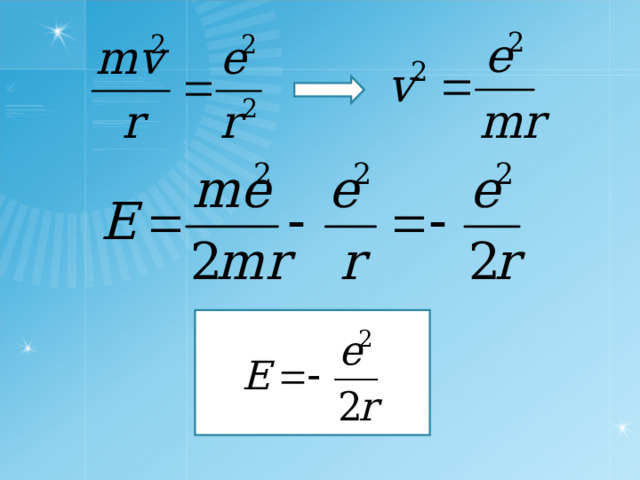




 n . " width="640"
n . " width="640"