
План урока
- Понятие об алкинах.
- Характеристика тройной связи.
- Изомерия и номенклатура алкинов.
- Получение алкинов.
- Физические свойства.
- Химические свойства алкинов.
- Применение алкинов.

Понятие об алкинах
- Алкины – непредельные углеводороды, содержащие в молекуле, помимо одинарных связей, одну тройную связь между атомами углерода, и соответствующие общей формуле
С n Н 2n - 2 , где n ≥ 2 .
- Алкины относятся к непредельным углеводородам, так как их молекулы содержат меньшее число атомов водорода, чем насыщенные.

Характеристика тройной связи
- Вид гибридизации – sp
- Валентный угол – 180
- Длина связи − С ≡ С – 0,12 нм
- Строение ─ линейное
- Вид связи – ковалентная полярная
- По типу перекрывания – δ и 2 π

Схема образования sp -гибридных орбиталей

Схема образования sp -гибридных орбиталей

Гомологический ряд алк ин ов
Эт ин
Проп ин
Бут ин
Пент ин
Гекс ин
Гепт ин
C 2 H 2
C 3 H 4
C 4 H 6
C 5 H 8
C 6 H 10
C 7 H 12

Изомерия алкинов
Структурная изомерия
1. Изомерия положения тройной связи (начиная с С 4 Н 6 ):
СН С СН 2 СН 3 СН 3 С С СН 3
бутин-1 бутин-2
2. Изомерия углеродного скелета (начиная с С 5 Н 8 ):
СН С СН 2 СН 2 СН 3 СН С СН СН 3
СН 3
пентин-1 3-метилбутин-1
3. Межклассовая изомерия с алкадиенами и циклоалкенами, (начиная с С 4 Н 8 ):
СН = СН
СН С–СН 2 –СН 3 СН 2 =СН–СН=СН 2 │
СН 2 –СН 2
бутин-1 бутадиен-1,3 циклобутен
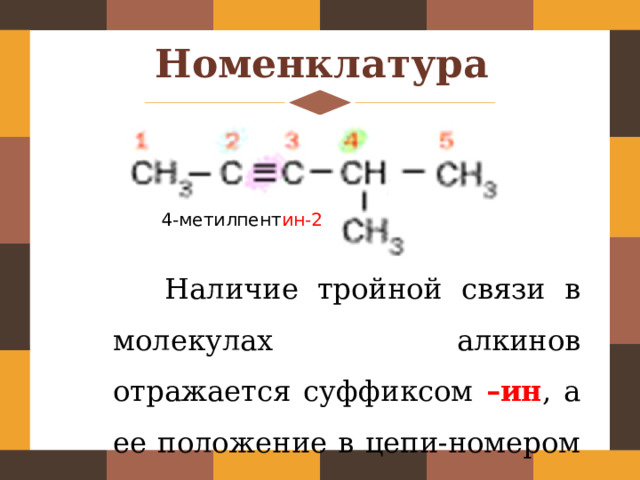
Номенклатура
4-метилпент ин-2
Наличие тройной связи в молекулах алкинов отражается суффиксом –ин , а ее положение в цепи-номером атома углерода.

Физические свойства
Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении молекулярной массы соединений.
Алкины имеют специфический запах. Они лучше растворяются в воде, чем алканы и алкены.

Получение алкинов
Ацетилен получают в промышленности двумя способами:
1. Метановый способ :
1500 С
2СН 4 С 2 Н 2 ↑+ 3Н 2
2. Карбидный способ :
CaC 2 + 2H 2 O C 2 H 2 ↑ + Ca(OH) 2

Химические свойства алкинов
Химические свойства ацетилена и его гомологов в основном определяются наличием в их молекулах тройной связи. Наиболее характерны для алкинов реакции присоединения.

Реакции присоединения
1. Галогенирование
Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды.
CH≡CH+Br 2 →CHBr═CHBr
1,2-дибромэтен
CHBr═CHBr+Br 2 →CHBr 2 -CHBr 2
1,1,2,2-тетрабромэтан

2. Гидрогалогенирование (по правилу Марковникова).
СH 3 -C≡CH + HBr→CH 3 -CBr═CH 2
2-бромпропен
CH 3 -CBr═CH 2 + HBr→CH 3 -CBr 2 -CH 3
2,2 – дибромпропан
3. Гидрирование.
СH 3 -C≡CH +H 2 →CH 3 -CН═CH 2
пропен
CH 3 -CН═CH 2 + H 2 →CH 3 -CН 2 -CH 3
пропан
4. Гидратация (реакция Кучерова)
HgSO 4
Н C C H + H 2 O CH 3 CОH
![Окисление Алкины обесцвечивают раствор KMnO 4 , что используется для их качественного определения. R C C R’ + [O] + H 2 O R COOH + R’ COOH](https://fsd.multiurok.ru/html/2021/11/23/s_619c79a4421ab/img13.jpg)
Окисление
Алкины обесцвечивают раствор KMnO 4 , что используется
для их качественного определения.
R C C R’ + [O] + H 2 O R COOH + R’ COOH

Горение ацетилена
Ацетилен горит коптящим пламенем с выделением большого количества теплоты
2HC CH + 5О 2 4СО 2 +2Н 2 О + 2600 кДж
![Реакции замещения Качественная реакция на концевую тройную связь При взаимодействии ацетилена (или R C C H ) с аммиачными растворами оксида серебра выпадают осадки нерастворимых ацетиленидов: HC CH + 2[Ag(NH 3 ) 2 ]OH AgC CAg + 4NH 3 + 2H 2 O](https://fsd.multiurok.ru/html/2021/11/23/s_619c79a4421ab/img15.jpg)
Реакции замещения
Качественная реакция на
концевую тройную связь
При взаимодействии ацетилена (или R C C H ) с аммиачными
растворами оксида серебра выпадают осадки нерастворимых ацетиленидов:
HC CH + 2[Ag(NH 3 ) 2 ]OH AgC CAg + 4NH 3 + 2H 2 O

Реакции полимеризации
1. Димеризация под действием водного раствора CuCl и NH 4 Cl:
НC CH + НC CH Н 2 C=CH C CH
винилацетилен
2. Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского ):
С, 400 С
3НC CH С 6 H 6
бензол
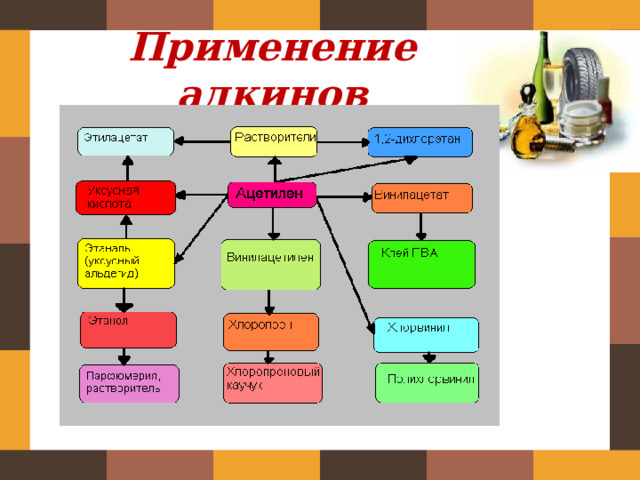
Применение алкинов



















![Окисление Алкины обесцвечивают раствор KMnO 4 , что используется для их качественного определения. R C C R’ + [O] + H 2 O R COOH + R’ COOH](https://fsd.multiurok.ru/html/2021/11/23/s_619c79a4421ab/img13.jpg)

![Реакции замещения Качественная реакция на концевую тройную связь При взаимодействии ацетилена (или R C C H ) с аммиачными растворами оксида серебра выпадают осадки нерастворимых ацетиленидов: HC CH + 2[Ag(NH 3 ) 2 ]OH AgC CAg + 4NH 3 + 2H 2 O](https://fsd.multiurok.ru/html/2021/11/23/s_619c79a4421ab/img15.jpg)



















