Просмотр содержимого документа
«Презентация по химии: соли азотной кислоты»

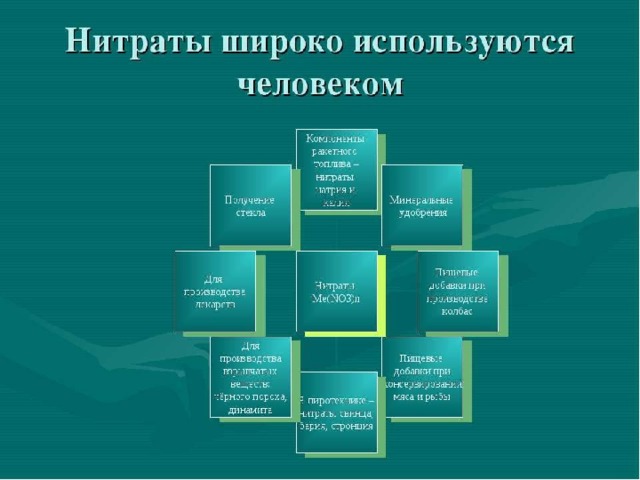
Соли азотной кислоты
- нитраты

Состав нитратов
Me (NO 3 )n или NH 4 NO 3
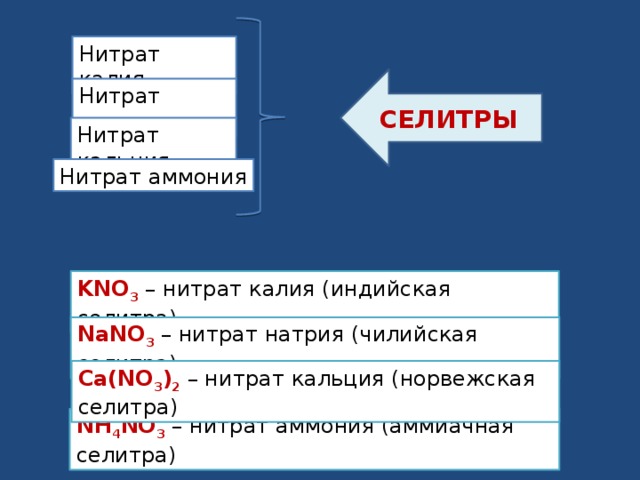
Нитрат калия
Нитрат натрия
СЕЛИТРЫ
Нитрат кальция
Нитрат аммония
KNO 3 – нитрат калия (индийская селитра)
NаNО 3 – нитрат натрия (чилийская селитра)
Са(NО 3 ) 2 – нитрат кальция (норвежская селитра)
NH 4 NO 3 – нитрат аммония (аммиачная селитра)
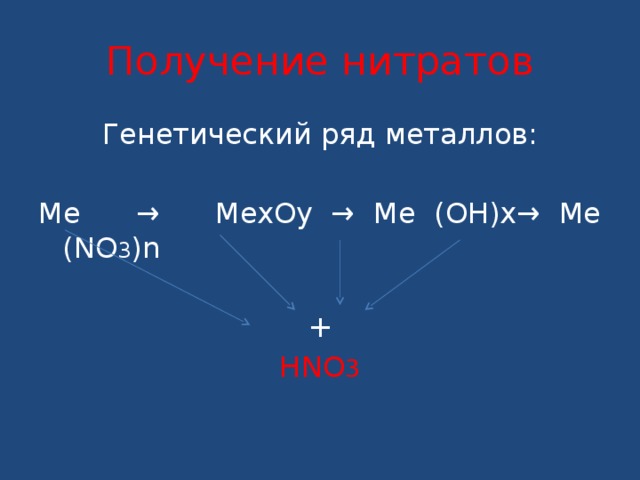
Получение нитратов
Генетический ряд металлов:
Me → MexOy → Me (OH)x→ Me (NO 3 )n
+
HNO 3

Основание + Азотная кислота
Cu(OH) 2 + 2HNO 3 = Cu(NO 3 ) 2 + 2H 2 O
Уравнения реакций
Металл + Азотная кислота
Cu + 4HNO 3 (k) = Cu(NO 3 ) 2 + 2NO 2 ↑ + 2H 2 O
Основный оксид + Азотная кислота
CuO + 2HNO 3 = Cu(NO 3 ) 2 + H 2 O
NH3 + HNO 3 =NH 4 NO 3
Соль слабой кислоты + Азотная кислота
CuCO 3 + 2HNO 3 = Cu(NO 3 ) 2 + CO 2↑ + 2H 2 O

Физические свойства нитратов
при обычных условиях это твёрдые кристаллические вещества
нитраты хорошо растворимы в воде
растворение нитратов – эндотермический процесс

ХИМИЧЕСКИЕ СВОЙСТВА НИТРАТОВ
С кислотами
AgNO 3 + HCl = AgCl↓ + HNO 3
Со щелочами
Cu(NO 3 ) 2 + 2NaOH = Cu(OH) 2 ↓ + 2NaNO 3
С солями
Cu(NO 3 ) 2 + 2NaOH = Cu(OH) 2 ↓ + 2NaNO 3

ХИМИЧЕСКИЕ СВОЙСТВА НИТРАТОВ
Специфические
Все нитраты термически неустойчивы . При нагревании они разлагаются с образованием кислорода.
Другие реакции - от положения металла, образующего нитрат, в электрохимическом ряду напряжений:
левее Mg
Нитрат + O 2
Mg..Сu
НИТРАТ
Оксид металла + NO 2 + O 2
правее Cu
Металл + NO 2 + O 2

Качественная реакция на нитраты