Просмотр содержимого документа
«Презентация по химии "Сероводород. Сульфиды"»

Сероводород.
Сульфиды.

Сероводород представляет собой бесцветный газ с резким запахом.
Он ядовит и вызывает отравление даже при незначительном содержании в воздухе.
H 2 S
В одном объёме воды растворяется 2,5 объёма сероводорода.
Сероводород
Сероводород может накапливаться в организме.
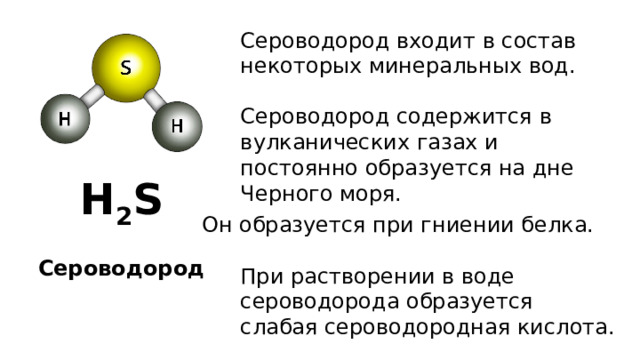
Сероводород входит в состав некоторых минеральных вод.
Сероводород содержится в вулканических газах и постоянно образуется на дне Черного моря.
H 2 S
Он образуется при гниении белка.
Сероводород
При растворении в воде сероводорода образуется слабая сероводородная кислота.

Сероводород также имеет лечебное значение, он является составной частью некоторых минеральных вод (Пятигорск, Серноводск, Мацеста).

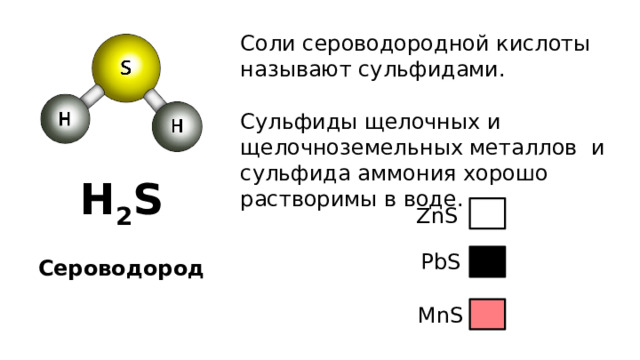
Соли сероводородной кислоты называют сульфидами.
Сульфиды щелочных и щелочноземельных металлов и сульфида аммония хорошо растворимы в воде.
H 2 S
ZnS
PbS
Сероводород
MnS
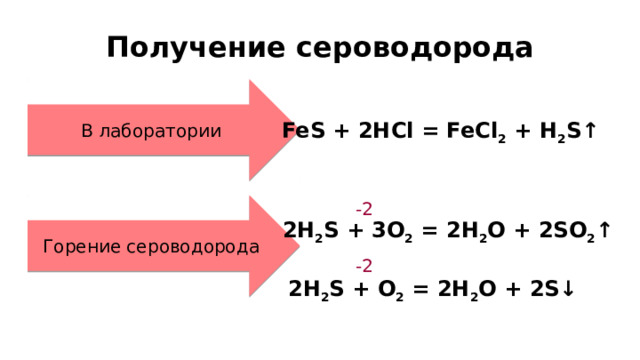
Получение сероводорода
В лаборатории
FeS + 2HCl = FeCl 2 + H 2 S↑
-2
Горение сероводорода
2H 2 S + 3O 2 = 2H 2 O + 2SO 2 ↑
-2
2H 2 S + O 2 = 2H 2 O + 2S↓
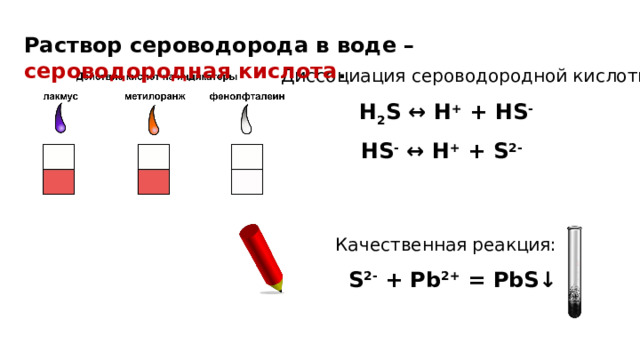
Раствор сероводорода в воде – сероводородная кислота .
Диссоциация сероводородной кислоты:
H 2 S ↔ H + + HS -
HS - ↔ H + + S 2-
Качественная реакция:
S 2- + Pb 2+ = PbS↓







































