Просмотр содержимого документа
«Презентация по химии: "Комплексные соединения алюминия. Алюмосиликаты"»

ГАПОУ СО «Калининский техникум агробизнеса»
Комплексные соединения алюминия. Алюмосиликаты
Подготовила: Данилова Т.В., преподаватель химии высшей квалификационной категории

Соединения алюминия
Соли
Оксид
Гидроксид
Каолинит
Аl 2 O 3 •2SiO 2 •2H 2 O

1. Оксид алюминия Al 2 O 3
Можно получить:
t
2) Al(OH)3 =

Оксид алюминия (Al 2 O 3 ) в природе
Боксит
Корунд
Сапфир
Рубин

Al 2 O 3 – амфотерный оксид
Выбрать с какими веществами будет реагировать оксид алюминия, написать уравнения реакций:
Al 2 O 3 : H 2 O, NaOH, CuSO 4 , HNO 3
file:///C:/Users/ дом/ Downloads/ Единая%20коллекция%20цифровых%20образовательных%20ресурсов/алюминий%20ЕКЦОР/амф%20оксида%20алюм%20интерактив. swf
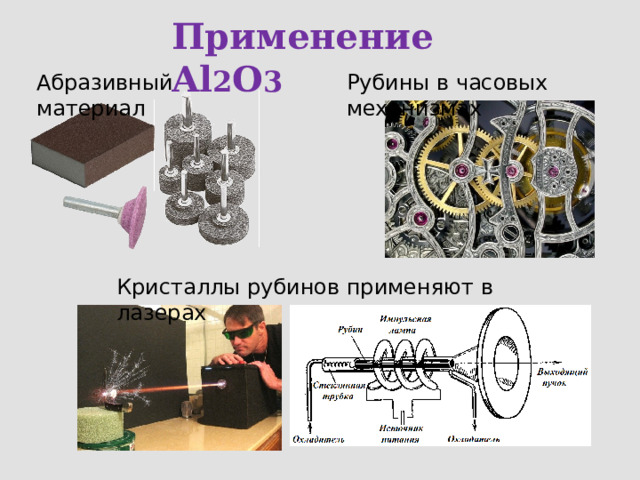
Применение Al 2 O 3
Абразивный материал
Рубины в часовых механизмах
Кристаллы рубинов применяют в лазерах
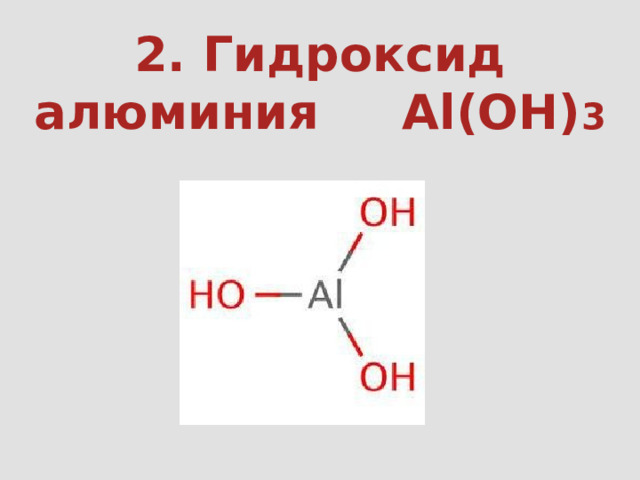
2. Гидроксид алюминия Al(OН) 3

Получение гидроксида алюминия
file:///C:/Users/ дом/ Downloads/ Единая%20коллекция%20цифровых%20образовательных%20ресурсов/алюминий%20ЕКЦОР/получ%20гидроксида%20алюм%20интреактив. swf
Доказательство амфотерности:
Стр.61

Природные алюминаты
Благородная шпинель
Драгоценный хризоберилл
BeAl 2 O 4
MgAl 2 O 4

3. Соли алюминия
Алюмосиликаты
Каолин
Полевой шпат
Глина белого цвета, она же белая глина, состоящая из минерала каолинита
Аl 2 O 3 •2SiO 2 •2H 2 O
К 2 O∙Al 2 О 3 ∙6SiO 2
Na 2 O∙Al 2 O 3 ∙6SiO 2
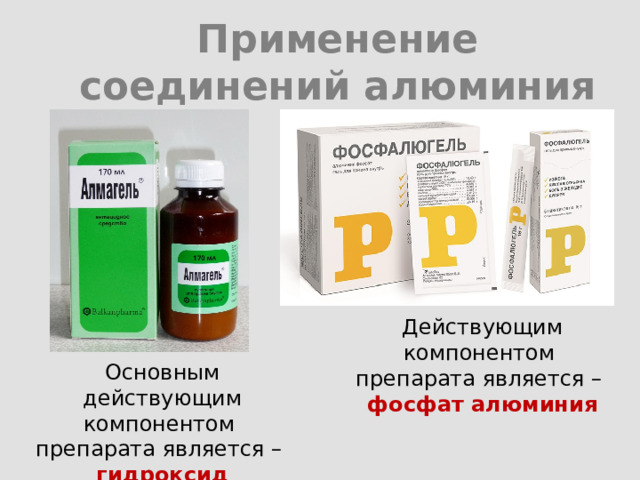
Применение соединений алюминия
Действующим компонентом
препарата является –
фосфат алюминия
Основным действующим компонентом
препарата является –
гидроксид алюминия

Соли алюминия: за или против?..

В 1927 году
получил алюминий
t
AlCl 3 + 3K = 3KCl + Al
(Без доступа воздуха)
Фридрих Вёлер

Будучи студентом Оберлинского колледжа, узнал, что можно разбогатеть и получить благодарность человечества, если изобрести способ получения алюминия в промышленных масштабах.
Как одержимый, Чарльз проводил эксперименты по выделению алюминия.
23.02.1886 г. , спустя почти год после окончания колледжа, Чарльз Холл получил с помощью электролиза первый алюминий.
Немного позже Ч. М. Холл получил патент на электролитический способ получения алюминия.
Чарльз Мартин Холл
1863-1914
эл. ток
2Al 2 O 3 = 4Al + 3O 2 – 3352 кДж







































