
Классы неорганических соединений

Классификация неорганических веществ
Основания
Оксиды
Кислоты
Соли
Генетическая связь
![Неорганические вещества (неорганические соединения) — это химические соединения, не являющиеся органическими, то есть, не содержащие углерода (кроме карбидов, цианидов, карбонатов, оксидов углерода и некоторых других соединений[⇨], которые традиционно относят к неорганическим). Неорганические соединения не имеют характерного для органических углеродного скелета. Простые вещества — состоят из атомов одного элемента; Сложные вещества — состоят из атомов двух или более элементов.](https://fsd.multiurok.ru/html/2020/10/26/s_5f96d920531f2/img2.jpg)
Неорганические вещества (неорганические соединения) — это химические соединения, не являющиеся органическими, то есть, не содержащие углерода (кроме карбидов, цианидов, карбонатов, оксидов углерода и некоторых других соединений[⇨], которые традиционно относят к неорганическим). Неорганические соединения не имеют характерного для органических углеродного скелета.
- Простые вещества — состоят из атомов одного элемента;
- Сложные вещества — состоят из атомов двух или более элементов.
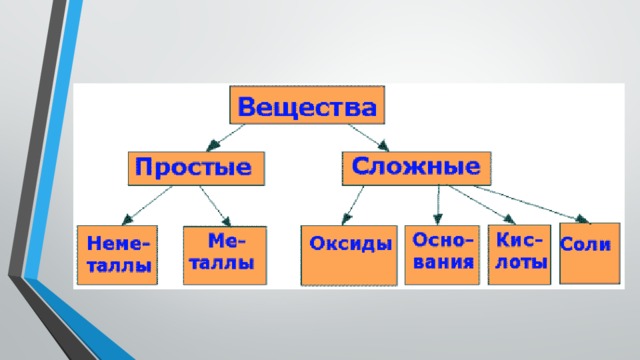

Простые вещества по химическим свойствам делятся на: металлы (Li, Na, K, Mg, Ca и др.); неметаллы (F2, Cl2, O2, S, P и др.); амфотерные простые вещества (Zn, Al, Fe, Mn и др.); благородные газы (He, Ne, Ar, Kr, Xe, Rn).
Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.

оксиды: осно́вные оксиды (CaO, Na2O и др.); кислотные оксиды (CO2, SO3 и др.); амфотерные оксиды (ZnO, Al2O3 и др.); двойные оксиды (Fe3O4 и др.); несолеобразующие оксиды (CO, NO и др.);

Гидроксиды; основания (NaOH, Ca(OH)2 и др.); кислоты (H2SO4, HNO3 и др.); амфотерные гидроксиды (Zn(OH)2, Al(OH)3 и др.);
![соли: средние соли (Na2SO4, Ca3(PO4)2 и др.); кислые соли (NaHSO3, CaHPO4 и др.); осно́вные соли (Cu2CO3(OH)2 и др.); двойные и/или комплексные соли (CaMg(CO3)2, K3[Fe(CN)6], KFeIII[FeII(CN)6] и др.);](https://fsd.multiurok.ru/html/2020/10/26/s_5f96d920531f2/img7.jpg)
соли: средние соли (Na2SO4, Ca3(PO4)2 и др.); кислые соли (NaHSO3, CaHPO4 и др.); осно́вные соли (Cu2CO3(OH)2 и др.); двойные и/или комплексные соли (CaMg(CO3)2, K3[Fe(CN)6], KFeIII[FeII(CN)6] и др.);

бинарные соединения: бескислородные кислоты (HCl, H2S и др.); бескислородные соли (NaCl, CaF2 и др.); прочие бинарные соединения (AlH3, CaC2, CS2 и др.).

Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.

Оксиды — весьма распространённый тип соединений, содержащихся в земной коре и во Вселенной вообще. Примерами таких соединений являются ржавчина, вода, песок, углекислый газ, ряд красителей. Оксидами также является класс минералов, представляющих собой соединения металла с кислородом

Кисло́ты — химические соединения, способные отдавать катион водорода (кислоты Брёнстеда) либо соединения, способные принимать электронную пару с образованием ковалентной связи (кислоты Льюиса)

Со́ли — это сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды. Кроме катионов металлов в солях могут находиться катионы аммония NH4+, фосфония PH4+ и их органические производные, а также комплексные катионы и т. д. Анионами в солях выступают анионы кислотного остатка различных кислот Брёнстеда — как неорганических, так и органических, включая карбанионы и комплексные анионы.

Генетические связи - это связи между разными классами, основанные на их взаимопревращениях. Зная классы неорганических веществ, можно составить генетические ряды металлов и неметаллов. В основу этих рядов положен один и тот же элемент.

Учите химию!








![Неорганические вещества (неорганические соединения) — это химические соединения, не являющиеся органическими, то есть, не содержащие углерода (кроме карбидов, цианидов, карбонатов, оксидов углерода и некоторых других соединений[⇨], которые традиционно относят к неорганическим). Неорганические соединения не имеют характерного для органических углеродного скелета. Простые вещества — состоят из атомов одного элемента; Сложные вещества — состоят из атомов двух или более элементов.](https://fsd.multiurok.ru/html/2020/10/26/s_5f96d920531f2/img2.jpg)




![соли: средние соли (Na2SO4, Ca3(PO4)2 и др.); кислые соли (NaHSO3, CaHPO4 и др.); осно́вные соли (Cu2CO3(OH)2 и др.); двойные и/или комплексные соли (CaMg(CO3)2, K3[Fe(CN)6], KFeIII[FeII(CN)6] и др.);](https://fsd.multiurok.ru/html/2020/10/26/s_5f96d920531f2/img7.jpg)
























