
Чадыр-Лунгский лицей №2
Бозаджи Н.,
учитель химии,
высшая дид.категория
13 апреля 2016 г.


«Мышление начинается с проблемной ситуации» С. Л. Рубинштейн

Жил один кристалл ионный,
Для ионов дом огромный,
Был красивый он и ровный,
Но случилась с ним беда.
Капля на него упала,
И кристалла вмиг не стало:
На ионы распластала
Его ловкая вода.
Все семейство удивилось:
«Что снаружи приключилось?»

...04.2017
Тема урока :

В результате изучения темы, вы будете способны:
- Давать определение понятиям:
- Давать определение понятиям:
электролит, неэлектролит, ЭД,
степень ЭД катион и анион.
- электролит, неэлектролит, ЭД, степень ЭД катион и анион.
2.Сравнивать вещества по электропроводимости.
3.Различать сильные и слабые электролиты.
4.Рассматривать механизм ЭД .
5.Рассматривать ЭД кислот, солей и оснований
6.Определять роль электролитов в процессах жизнедеятельности
7.Осуществлять рефлексию своей деятельности
- 7.Осуществлять рефлексию своей деятельности

Задание №1.
Что такое электрический ток ?
Электрический ток – направленное движение
заряженных частиц
Задание № 2.
Все ли вещества могут проводить электрический ток ?

Задание № 3.
Видео вопрос: Какие вещества проводят ток , а какие нет? в каком состоянии находятся вещества?
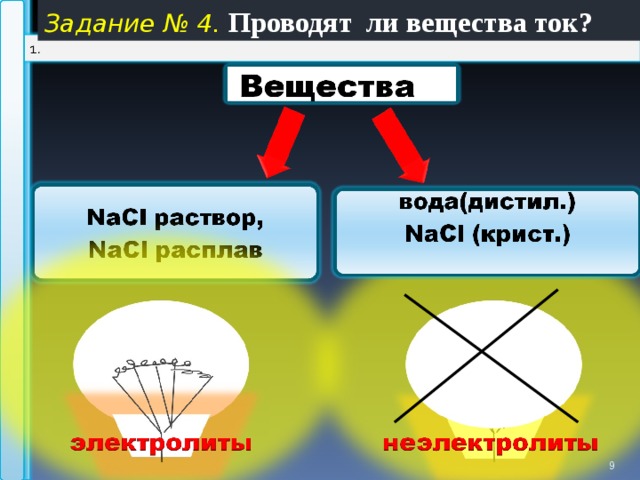
Задание № 4. Проводят ли вещества ток?

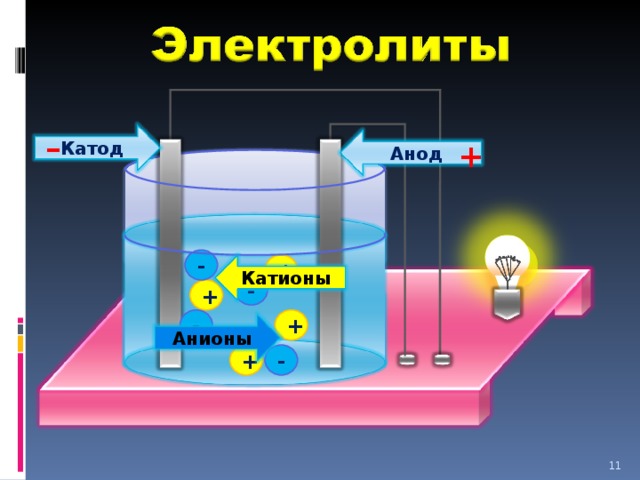
-
Катод
Анод
+
-
+
Катионы
-
+
-
+
Анионы
+
-
11

Задание № 6. Используя таблицу растворимости приведите примеры электролитов (по одной формуле).
11
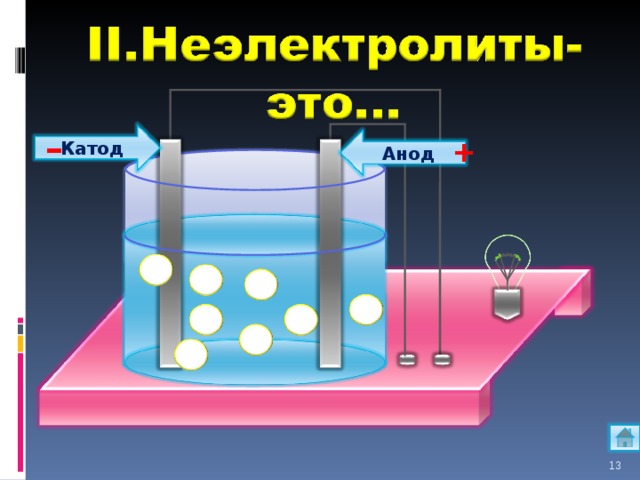
-
Катод
+
Анод
13

Задание № 7. «Дай мне название»
13

Задание № 8. Используя таблицу растворимости приведите примеры 2 неэлектролитов.
14
14
16

III .Электролитическая диссоциация. ЭД
17

Задание № 9 . Какие заряженные частицы - ионы вы знаете?
КАТИОНЫ
АНИОНЫ
-
+
Для двух подруг подарков груз
Взвалил c ебе Ион на плечи
Для Кати он несет свой плюс( + )
Для Ани он несет свой минус( - )
+
-
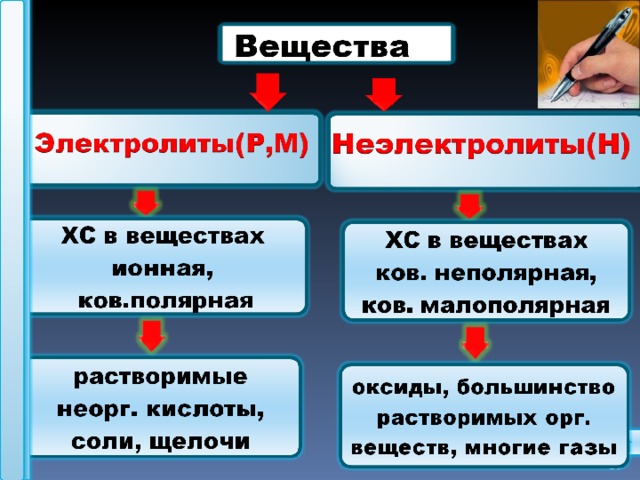
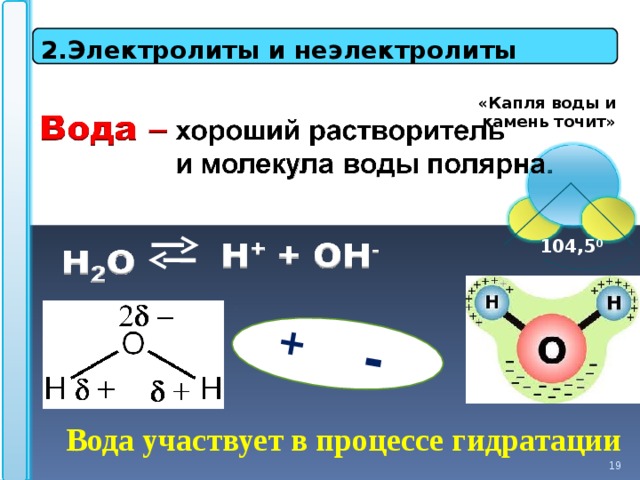
2 .Электролиты и неэлектролиты
«Капля воды и камень точит»
104,5 0
Вода участвует в процессе гидратации
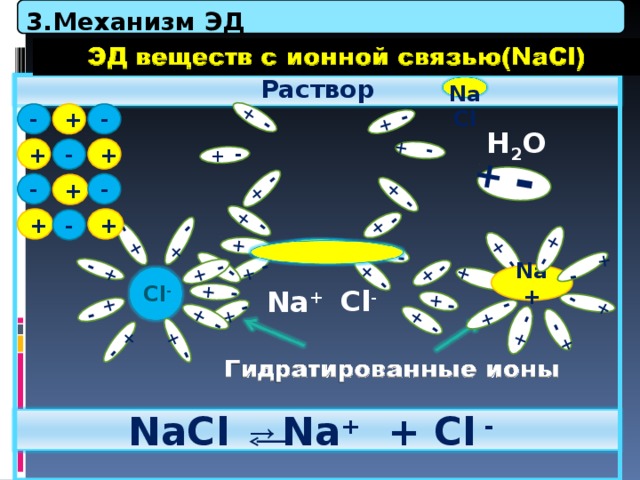
3.Механизм ЭД
+
-
+
-
+
-
+
+
-
-
+
+
-
+
-
+
-
-
+
+
-
-
+
-
+
+
+
+
+
+
-
-
-
+
-
+
-
-
-
-
+
-
+
-
+
+
+
-
-
+
-
+
-
+
-
+
-
+
-
-
-
+
-
+
-
+
-
+
Раствор
NaCl
+
-
-
H 2 O
+
+
-
-
+
-
-
+
+
+
-
+
-
Na+
С l -
Cl -
Na +
Рисунок 1.
NaCl → Na + + Cl -
20
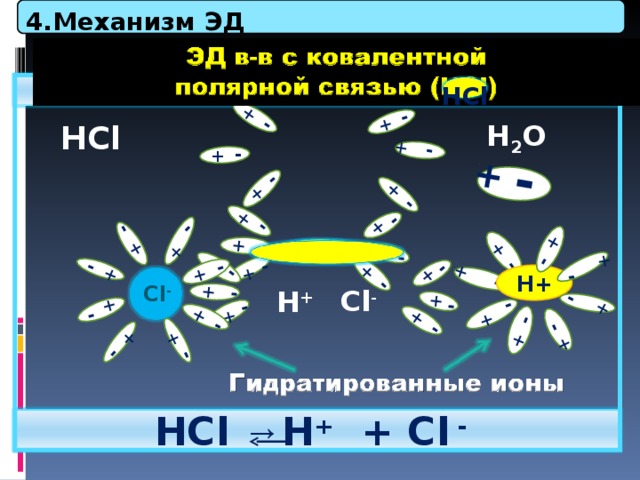
4 .Механизм ЭД
+
-
+
-
+
-
+
+
-
-
+
-
+
+
-
+
-
-
+
+
-
-
+
-
+
+
+
+
+
-
-
+
-
+
+
-
-
-
-
+
-
-
+
-
+
+
-
+
-
+
-
+
-
+
-
+
-
+
-
+
-
-
-
-
+
+
-
+
Раствор
HCl
HCl
H 2 O
-
+
+
-
Н +
С l -
Cl -
H +
Рисунок 1.
HCl → H + + Cl -
21

Задание № 10. Укажите процессы описанные в этом стихотворении и назовите тип ХС вещества .
Жил один кристалл ионный, Для ионов дом огромный, Был красивый он и ровный. Но случилась с ним беда. Капля на него упала, И кристалла вмиг не стало: На ионы распластала Его ловкая вода. Все семейство удивилось: «Что снаружи приключилось?»
Это рядом появилась вдруг молекул череда, Подбежали шумным роем, Окружили плотным строем: «Предложить хотим героям нашу дружбу навсегда…» Водородом к анионам, Гидроксидом к катионам, Не уйти от них ионам Ни туда и ни сюда.
Гидратация
Диссоциация
Ионная связь
21


+
+
+
IV .Сильные и слабые электролиты
+
+
+
+
+
+
+
+
+
От чего зависит сила электролита?
21
 30% NB! Слабые электролиты n α = N α 30% 25 " width="640"
30% NB! Слабые электролиты n α = N α 30% 25 " width="640"
NB! Сильные электролиты
α 30%
NB! Слабые электролиты
n
α =
N
α 30%
25
 30% ) (Р) Соли Слабые ( α 30% ) Все растворимые Основания (М) Hg 2 Cl 2 , c оли тяжелых металлов МеОН р МеОН н МеОН р I и II групп гл.подгрупп - водный раствор аммиака –нашатырь NH 4 OH Кислоты бескислород все HI, HBr, HCl кислородосодержащие HF (8,5%) , H 2 S HClO 4 H 2 SO 4 (50%) , HNO 3 H 2 SO 3 , H 2 CO 3 (0,17%) , H 2 SiO 3 , Н 3 Р O 4 , CH 3 COOH и др. " width="640"
30% ) (Р) Соли Слабые ( α 30% ) Все растворимые Основания (М) Hg 2 Cl 2 , c оли тяжелых металлов МеОН р МеОН н МеОН р I и II групп гл.подгрупп - водный раствор аммиака –нашатырь NH 4 OH Кислоты бескислород все HI, HBr, HCl кислородосодержащие HF (8,5%) , H 2 S HClO 4 H 2 SO 4 (50%) , HNO 3 H 2 SO 3 , H 2 CO 3 (0,17%) , H 2 SiO 3 , Н 3 Р O 4 , CH 3 COOH и др. " width="640"
1 .Сильные и слабые электролиты ( !!!ТР )
Сильные
( α 30% ) (Р)
Соли
Слабые ( α 30% )
Все растворимые
Основания
(М)
Hg 2 Cl 2 , c оли тяжелых металлов
МеОН р
МеОН н
МеОН р
I и II групп гл.подгрупп
-
водный раствор
аммиака –нашатырь
NH 4 OH
Кислоты
бескислород
все
HI, HBr, HCl
кислородосодержащие
HF (8,5%) , H 2 S
HClO 4 H 2 SO 4 (50%) , HNO 3
H 2 SO 3 ,
H 2 CO 3 (0,17%) , H 2 SiO 3 , Н 3 Р O 4 , CH 3 COOH и др.
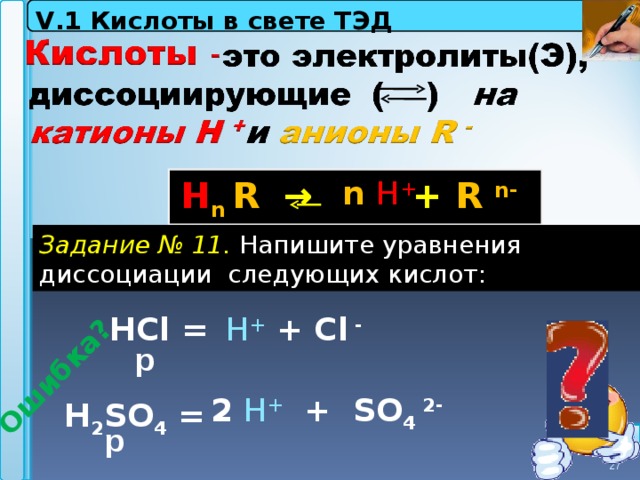
V . 1 Кислоты в свете ТЭД
Ошибка?
n H +
Н n R → + R n-
Задание № 11. Напишите уравнения диссоциации следующих кислот:
Н Cl =
H + + Cl -
р
2 H + + SO 4 2-
Н 2 SO 4 =
р
27
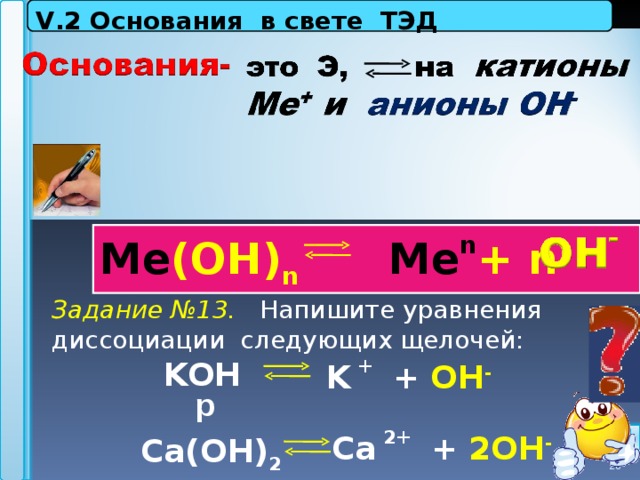
V . 2 Основания в свете ТЭД
М e (OH) n Me n + n
Задание №13. Напишите уравнения диссоциации следующих щелочей:
KOH
Ca(OH) 2
K + + OH -
р
Ca 2+ + 2OH -
28
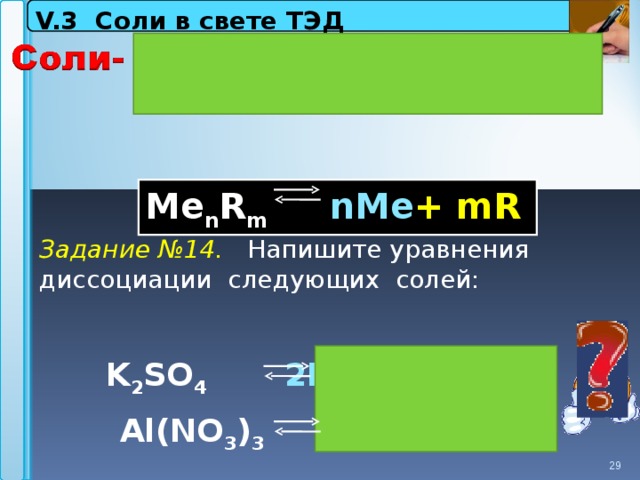
V.3 Соли в свете ТЭД
М e n R m nMe + mR
Задание №14. Напишите уравнения диссоциации следующих солей:
K 2 SO 4 2 К + +
SO 2- 4
Al 3+
+
3 NO 3 -
Al(NO 3 ) 3
29

VI .Значение электролитов
Э

Ионы
Типичный симптом
Са 2+
Замедление роста скелета
Mg 2+
Fe 2+
Мускульные судороги
Анемия, нарушение иммун -
ной системы
Zn 2+
Повреждение кожи, замедление полового созревания
Mn 2+
Учащение депрессий, дерматиты
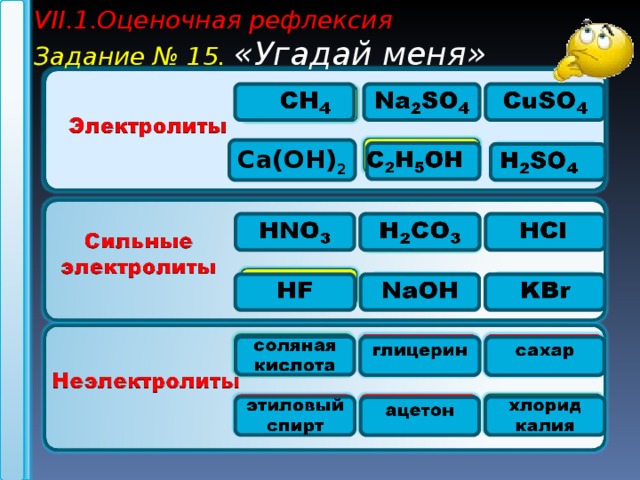
VII. 1.Оценочная рефлексия
Задание № 15. «Угадай меня»
Ca(OH) 2

VII. 2.Оценочная рефлексия
Задание № 16. Тест
«Незаконченное предложение»
(Отметьте букву правильного ответа)
B A D A B
Слабым электролитом является _______ .
Электролитическая диссоциация
в растворах – это процесс распада электролита на __________ .
Электролитами не являются ________ .
Электролитическая диссоциация электролитов в растворах протекает под действием __________ .
Основные положения электролитической диссоциации сформулировал ученый ______.
Д.И.Менделеев
кислоты
HNO 3
оксиды
KCl
ионы
атомы
электрического
тока
катализатора
С.Аррениус
щелочи
температуры
молекул растворителя
NaOH
М.Фарадей
М.В.Ломоносов
H 2 S
электроны
соли
молекулы
33
33
33
33

«Острова»
о. Грусти
О. Удовольствия
о. Воодушевления
о.Неопределенности
о. Недоумения
о.Радости
о.Тревоги
о.Просветления
о.Бермудский
треугольник

1. § 5.6.1 - 2 стр. 119-123
2. конспект, знать определения
3.Написать уравнения диссоциации 2-4 * кислот, щелочей и солей
33

Хоть выйди ты не в белый свет
А в поле за околицей,-
Пока идешь за кем-то вслед,
Дорога не запомнится.
Зато, куда б ты ни попал
И по какой распутице,
Дорога та, что сам искал,
Вовек не позабудется.
Н.Рыленков
Благодарю за
за сотрудничество





























 30% NB! Слабые электролиты n α = N α 30% 25 " width="640"
30% NB! Слабые электролиты n α = N α 30% 25 " width="640"
 30% ) (Р) Соли Слабые ( α 30% ) Все растворимые Основания (М) Hg 2 Cl 2 , c оли тяжелых металлов МеОН р МеОН н МеОН р I и II групп гл.подгрупп - водный раствор аммиака –нашатырь NH 4 OH Кислоты бескислород все HI, HBr, HCl кислородосодержащие HF (8,5%) , H 2 S HClO 4 H 2 SO 4 (50%) , HNO 3 H 2 SO 3 , H 2 CO 3 (0,17%) , H 2 SiO 3 , Н 3 Р O 4 , CH 3 COOH и др. " width="640"
30% ) (Р) Соли Слабые ( α 30% ) Все растворимые Основания (М) Hg 2 Cl 2 , c оли тяжелых металлов МеОН р МеОН н МеОН р I и II групп гл.подгрупп - водный раствор аммиака –нашатырь NH 4 OH Кислоты бескислород все HI, HBr, HCl кислородосодержащие HF (8,5%) , H 2 S HClO 4 H 2 SO 4 (50%) , HNO 3 H 2 SO 3 , H 2 CO 3 (0,17%) , H 2 SiO 3 , Н 3 Р O 4 , CH 3 COOH и др. " width="640"



























