Здравствуйте, меня зовут Константин Анатольевич Барковец.
Я работаю учителем физики с 2000 года. Преподаю предмет как в базовых, так и в профильных классах. В своей работе я стараюсь быть инновационным и активно использовать современные технологии. Я часто записываю свои "рабочие" уроки в школе и публикую их в социальных сетях. Я верю, что такой подход позволяет не только помочь моим ученикам, но и поделиться полезной информацией с другими учителями.
В данной презентации, которую я предоставляю, рассматривается тема молекулярной физики и термодинамики. Она может быть использована на уроках физики в качестве повторения уже пройденного материала. Я уверен, что такой подход поможет ученикам лучше усвоить и закрепить полученные знания. Конечно, каждый учитель имеет свой собственный стиль преподавания и предпочтения. Поэтому, если вы решите использовать мою презентацию, я настоятельно рекомендую вносить в нее свои изменения и адаптировать ее под свои потребности. Я сам часто скачиваю презентации и изменяю их "под себя", чтобы они лучше соответствовали моему стилю преподавания и уровню понимания моих учеников.
В заключение, я хотел бы подчеркнуть, что обмен опытом и знаниями - важная часть нашей профессии. Я всегда готов делиться своими материалами и учиться у других учителей. Пусть наши уроки станут еще более интересными.
www.youtube.com /@BARKOVEZ
https ://vk.com/barkovez

Молекулярная физика — наука, которая изучает макротела, их физические свойства на основе рассмотрения их молекулярного строения, движения и сил взаимодействия микрочастиц.

Самое главное знание-знание о молекулах»
Ричард Фейнман

Теория атомов
«Атомы суть всевозможных малых тел, не имеющие качеств, пустота же - место, в котором все эти тела, в течении всей вечности, носясь вверх и вниз, или сплетаются между собой, или наталкиваются друг на друга, отскакивают, расходятся и снова сходятся в такие соединения, и таким образом они производят и все прочие сложные тела и наши тела, и их состояния и ощущения.»
Демокрит Абдерский 460 г.до н.э.

Количественно оценивает тепловые процессы
Термометр
Изобретателем термометра принято считать Галилея: в его собственных сочинениях нет описания этого прибора, но его ученики, Нелли и Вивиани, засвидетельствовали, что уже в 1597 году он сделал нечто вроде термо баро скопа (термоскоп)
Что измеряет?
?
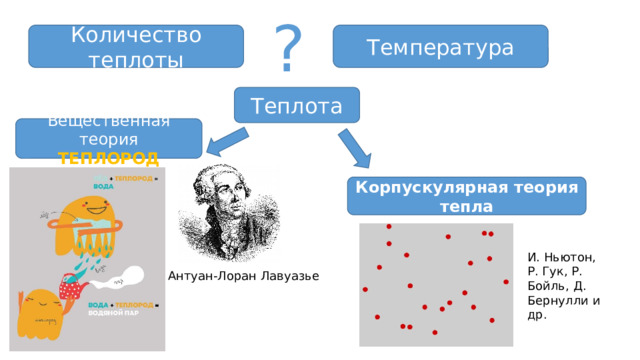
Количество теплоты
Температура
Теплота
Вещественная теория
ТЕПЛОРОД
Корпускулярная теория тепла
И. Ньютон,
Р. Гук, Р. Бойль, Д. Бернулли и др.
Антуан-Лоран Лавуазье
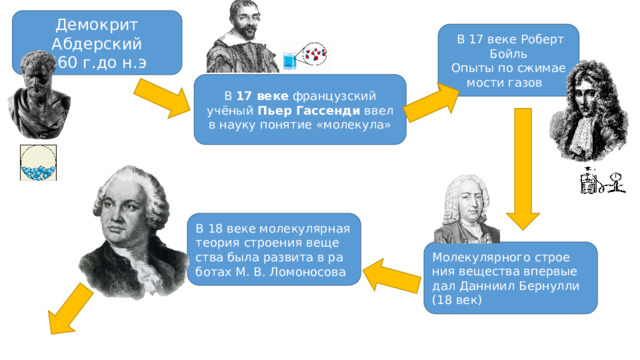
Демокрит Абдерский 460 г.до н.э
В 17 веке Роберт Бойль
Опыты по сжимаемости газов
В 17 веке французский учёный Пьер Гассенди ввел в науку понятие «молекула»
В 18 веке молекулярная теория строения вещества была развита в работах М. В. Ломоносова
Молекулярного строения вещества впервые дал Данниил Бернулли (18 век)

В 1741 г. в одной из своих первых работ «Элементы математической химии» М. В. Ломоносов сформулировал важнейшие положения атомно-молекулярной теории.
В основе МКТ лежат три утверждения:
- Все тела состоят из малых частиц, между которыми есть промежутки
- Частицы всех тел постоянно и беспорядочно движутся
- Частицы тел взаимодействуют друг с другом: притягиваются и отталкиваются
?

Теоретические основы
броуновского движения
были даны
Альбертом Эйнштейном и
Марианом Смолуховским.
Открыл
Обосновали
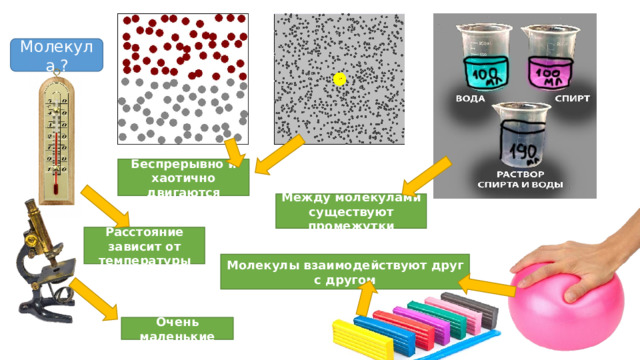
Молекула ?
Беспрерывно и хаотично двигаются
Между молекулами существуют промежутки
Расстояние зависит от температуры
Молекулы взаимодействуют друг с другом
Очень маленькие

Демокрит Абдерский 460 г.до н.э .
Герд Бинниг и Генрих Рорер являются изобретателями сканирующего туннельного микроскопа (1981г)
Эрнст Август Руска
Создатель электронного микроскопа, лауреат
Нобелевской премии по физике за 1986 год

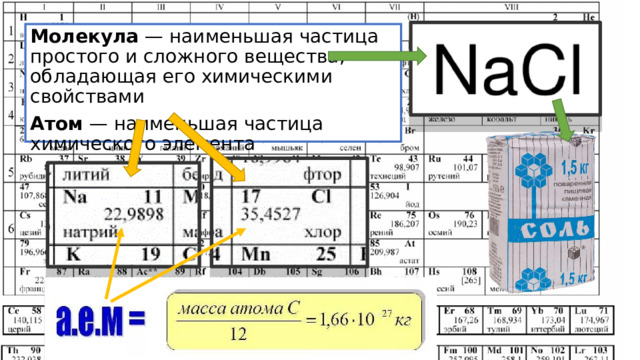
Молекула — наименьшая частица простого и сложного вещества, обладающая его химическими свойствами
Атом — наименьшая частица химического элемента
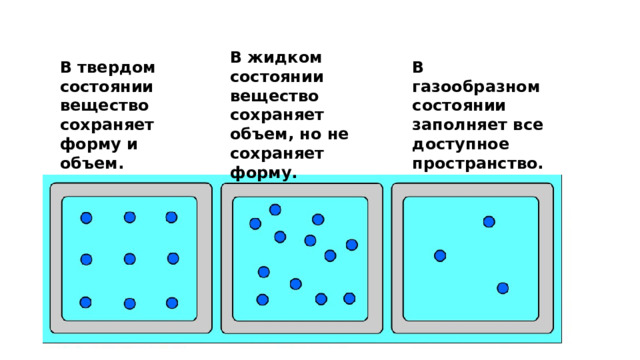
В жидком состоянии вещество сохраняет объем, но не сохраняет форму.
В твердом состоянии вещество сохраняет форму и объем.
В газообразном состоянии заполняет все доступное пространство.
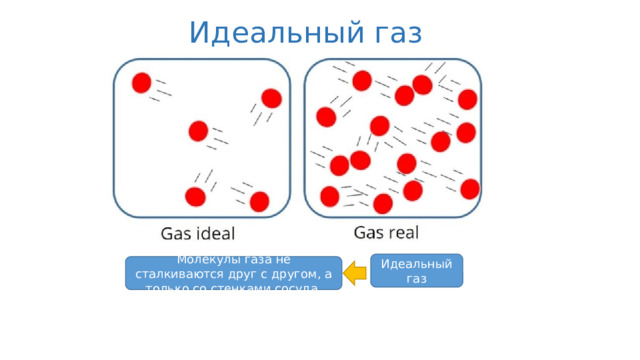
Идеальный газ
Идеальный газ
Молекулы газа не сталкиваются друг с другом, а только со стенками сосуда.

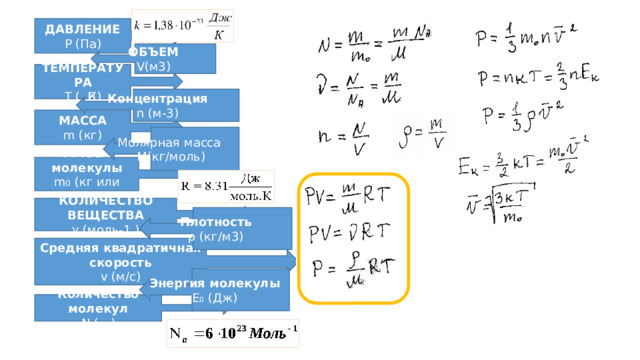
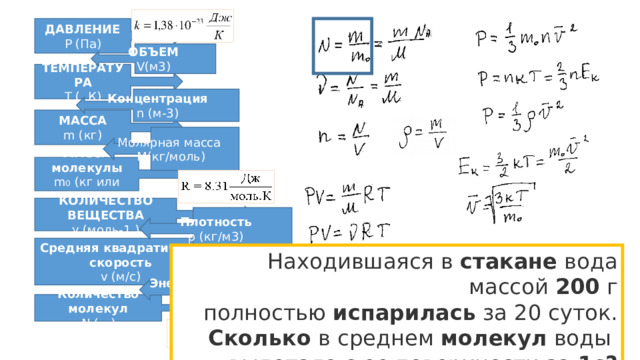
ДАВЛЕНИЕ
Р (Па)
ТЕМПЕРАТУРА
Т ( ͦК)
МАССА
m (кг)
МАССА молекулы
m 0 (кг или а.е.м.)
ОБЪЕМ
V(м3)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
Концентрация
n (м-3)
Средняя квадратичная скорость
Молярная масса
v (м/с)
Плотность
M(кг/моль)
Энергия молекулы
ρ (кг/м3)
Е 0 (Дж)
Количество молекул
N (…)
ДАВЛЕНИЕ
Р (Па)
ОБЪЕМ
V(м3)
ТЕМПЕРАТУРА
Т ( ͦК)
Концентрация
n (м-3)
МАССА
m (кг)
Молярная масса
M(кг/моль)
МАССА молекулы
m 0 (кг или а.е.м.)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
Плотность
ρ (кг/м3)
Средняя квадратичная скорость
v (м/с)
Энергия молекулы
Е 0 (Дж)
Количество молекул
N (…)
ДАВЛЕНИЕ
Р (Па)
ОБЪЕМ
V(м3)
ТЕМПЕРАТУРА
Т ( ͦК)
Концентрация
n (м-3)
МАССА
m (кг)
Молярная масса
M(кг/моль)
МАССА молекулы
m 0 (кг или а.е.м.)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
Плотность
ρ (кг/м3)
Средняя квадратичная скорость
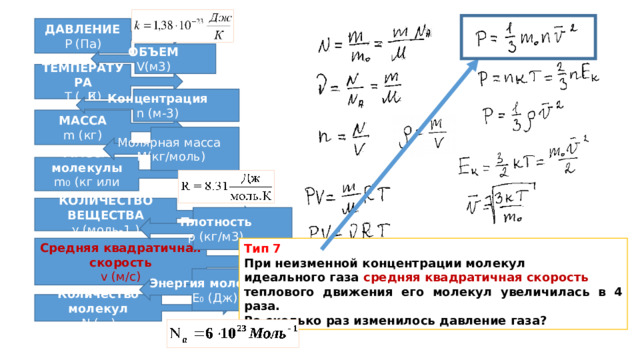
Тип 7
v (м/с)
При неизменной концентрации молекул
идеального газа средняя квадратичная скорость
теплового движения его молекул увеличилась в 4 раза.
Во сколько раз изменилось давление газа?
Энергия молекулы
Е 0 (Дж)
Количество молекул
N (…)
ДАВЛЕНИЕ
Р (Па)
ОБЪЕМ
V(м3)
ТЕМПЕРАТУРА
Т ( ͦК)
Концентрация
n (м-3)
МАССА
m (кг)
Молярная масса
M(кг/моль)
МАССА молекулы
m 0 (кг или а.е.м.)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
Плотность
ρ (кг/м3)
Средняя квадратичная скорость
v (м/с)
Энергия молекулы
Е 0 (Дж)
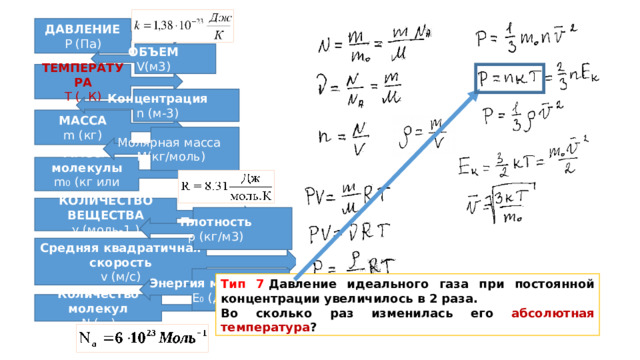
Тип 7 Давление идеального газа при постоянной концентрации увеличилось в 2 раза.
Во сколько раз изменилась его абсолютная температура ?
Количество молекул
N (…)
ДАВЛЕНИЕ
Р (Па)
ОБЪЕМ
V(м3)
ТЕМПЕРАТУРА
Т ( ͦК)
Концентрация
n (м-3)
МАССА
m (кг)
Молярная масса
M(кг/моль)
МАССА молекулы
m 0 (кг или а.е.м.)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
Плотность
ρ (кг/м3)
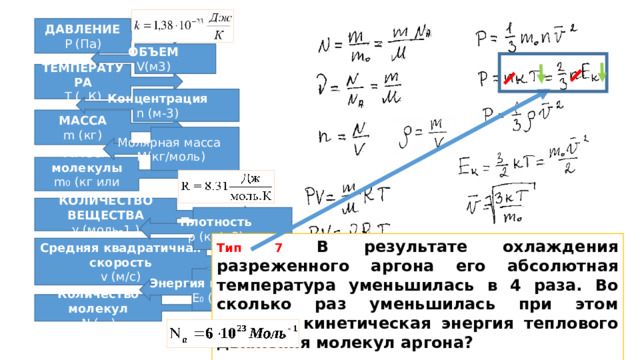
Тип 7 В результате охлаждения разреженного аргона его абсолютная температура уменьшилась в 4 раза. Во сколько раз уменьшилась при этом средняя кинетическая энергия теплового движения молекул аргона?
Средняя квадратичная скорость
v (м/с)
Энергия молекулы
Е 0 (Дж)
Количество молекул
N (…)
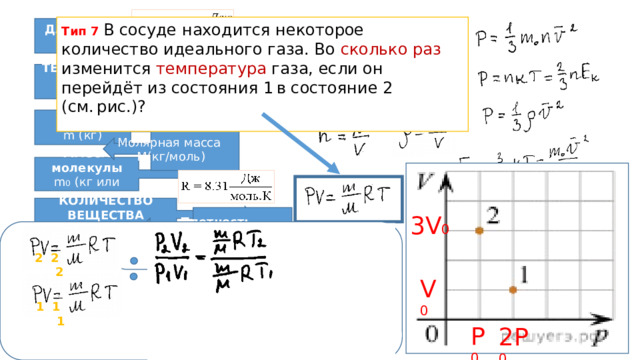
Тип 7 В сосуде находится некоторое количество идеального газа. Во сколько раз изменится температура газа, если он перейдёт из состояния 1 в состояние 2 (см. рис.)?
ДАВЛЕНИЕ
Р (Па)
ОБЪЕМ
V(м3)
ТЕМПЕРАТУРА
Т ( ͦК)
Концентрация
n (м-3)
МАССА
m (кг)
Молярная масса
M(кг/моль)
МАССА молекулы
m 0 (кг или а.е.м.)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
3V 0
Плотность
ρ (кг/м3)
Средняя квадратичная скорость
v (м/с)
2 2 2
Энергия молекулы
Е 0 (Дж)
V 0
Количество молекул
N (…)
1 1 1
P 0
2P 0
ДАВЛЕНИЕ
Р (Па)
ОБЪЕМ
V(м3)
ТЕМПЕРАТУРА
Т ( ͦК)
Концентрация
n (м-3)
МАССА
m (кг)
Молярная масса
M(кг/моль)
МАССА молекулы
m 0 (кг или а.е.м.)
КОЛИЧЕСТВО ВЕЩЕСТВА
γ (моль-1.)
Плотность
ρ (кг/м3)
Средняя квадратичная скорость
v (м/с)
Находившаяся в стакане вода массой 200 г полностью испарилась за 20 суток.
Сколько в среднем молекул воды
вылетало с ее поверхности за 1с?
Энергия молекулы
Е 0 (Дж)
Количество молекул
N (…)
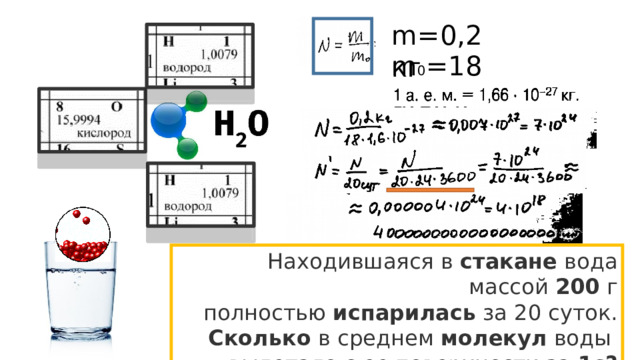
m=0,2кг
m 0 =18 а.е.м.
Находившаяся в стакане вода массой 200 г полностью испарилась за 20 суток.
Сколько в среднем молекул воды
вылетало с ее поверхности за 1с?

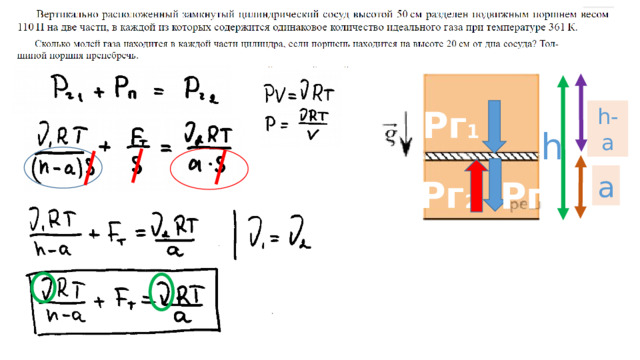
Рг 1
h-a
h
a
Рг 2
Рп
СОХРАНЕНИЕ ТЕПЛОРОДА?
?
В 19 веке принцип сохранения теплорода был заменен более общим и глубоким принципом — законом сохранения энергии.
Количество теплоты -мера изменения энергии
– это раздел физики, изучающий тепловые свойства макроскопических тел и систем тел, находящихся в состоянии теплового равновесия, на основе закона сохранения энергии, без учета внутреннего строения тел , составляющих систему.
Термодинамика
Тепловые явления описываются с помощью величин, регистрируемых приборами
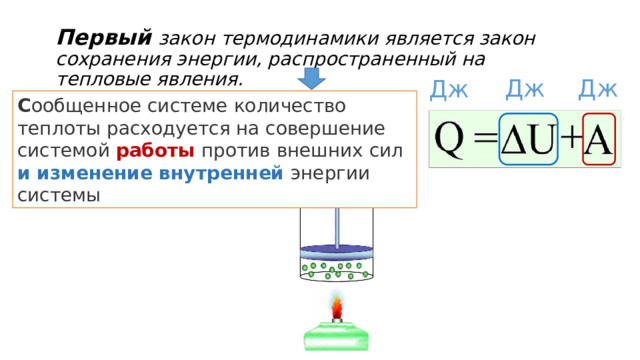
Первый закон термодинамики является закон сохранения энергии, распространенный на тепловые явления.
Дж
Дж
Дж
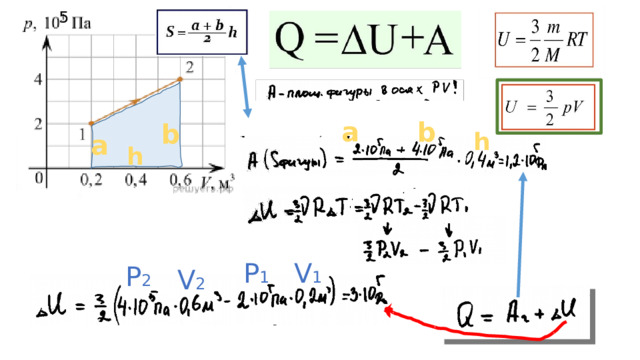
С ообщенное системе количество теплоты расходуется на совершение системой работы против внешних сил и изменение внутренней энергии системы

Внутренняя энергия
Внутренняя энергия — кинетическая энергия всех молекул, из которых состоят тела, и потенциальная энергия их взаимодействия.
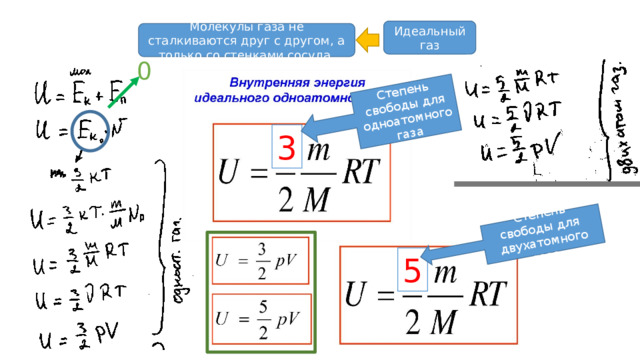
Степень свободы для одноатомного газа
Степень свободы для двухатомного газа
Идеальный газ
Молекулы газа не сталкиваются друг с другом, а только со стенками сосуда.
0
3
5
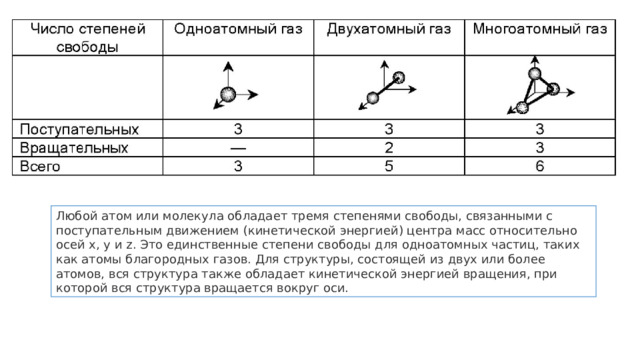
Любой атом или молекула обладает тремя степенями свободы, связанными с поступательным движением (кинетической энергией) центра масс относительно осей x, y и z. Это единственные степени свободы для одноатомных частиц, таких как атомы благородных газов. Для структуры, состоящей из двух или более атомов, вся структура также обладает кинетической энергией вращения, при которой вся структура вращается вокруг оси.
5
а
b
b
h
а
h
Р 1
V 1
Р 2
V 2
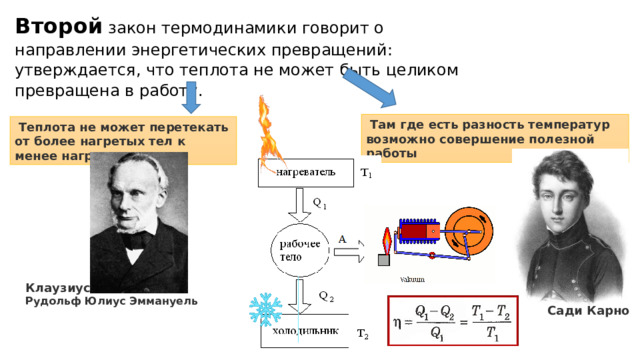
Второй закон термодинамики говорит о направлении энергетических превращений: утверждается, что теплота не может быть целиком превращена в работу.
Там где есть разность температур возможно совершение полезной работы
Теплота не может перетекать от более нагретых тел к менее нагретым .
Клаузиус
Рудольф Юлиус Эммануель
Сади Карно

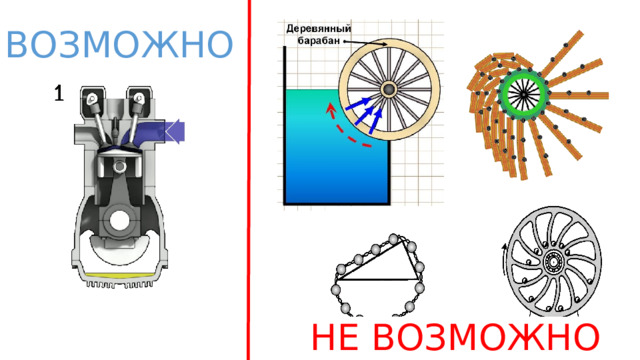
ВОЗМОЖНО
НЕ ВОЗМОЖНО

Заключение: …





























































