
Алкадиены: строение, номенклатура,
гомологи, изомерия

ЦЕЛИ УРОКА
- Познакомить учащихся с понятием «алкадиены», их номенклатурой, изомерией, химическими свойствами и способами получения.
- Совершенствовать умения учащихся составлять структурные формулы органических веществ и их изомеров, записывать уравнения реакций.

Актуализация ранее полученных знаний
Вопросы:
1. С какими классами углеводородов вы познакомились к настоящему времени?
2. Какие вещества называются алканами, алкенами, алкинами?
3. Общая химическая формула алканов, алкенов, алкинов?
4. Какие виды изомерии характерны для этих классов углеводородов?
5. Какие реакции характерны для веществ имеющих кратную связь?
6. Согласно какому правилу происходит присоединение галогеноводородов и воды в молекулах с кратными связями?

- Алкадиены - ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода и соответствующие общей формуле: C n H 2n-2

Алкадиены с кумулированным расположением двойных связей (аллены)
- Углеводороды содержащие две двойные связи ,находящиеся возле соседних атомов углерода.
1 2 3 4
СН 2 =С=СН-СН 3
бутадиен -1, 2

Сопряженные алкадиены
- Углеводороды содержащие две двойные связи ,между которыми находится одна одинарная связь.
1 2 3 4 5 6
СН 3 -СН=СН-СН=СН-СН 3
гексадиен-2, 4
1 2 3 4
СН 2 =СН-СН=СН 2
бутадиен -1, 3 (дивинил)

Алкадиены с изолированными двойными связями
- Углеводороды содержащие две двойные связи ,между которыми находится несколько одинарных связей.
8 7 6 5 4 3 2 1
СН 3 –СН 2 -СН=СН-СН 2 -СН 2 -СН=СН 2
октадиен-1, 5

Номенклатура алкадиенов
Правила:
1. Главная цепь должна содержать обе двойные связи.
2. Нумерацию ведут с того конца где ближе кратная связь.
3. Называют заместители и указывают атомы углерода от которого они отходят.
4. Указывают название алкадиена и атомы углерода от которых образована двойная связь.
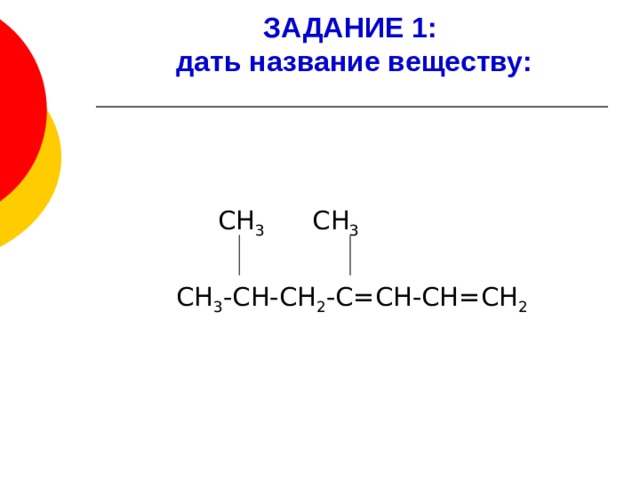
ЗАДАНИЕ 1: дать название веществу:
СН 3 СН 3
СН 3 -СН-СН 2 -С=СН-СН=СН 2
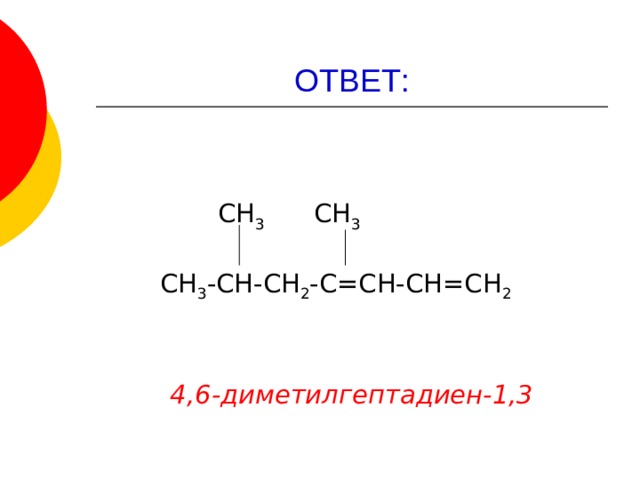
ОТВЕТ:
СН 3 СН 3
СН 3 -СН-СН 2 -С=СН-СН=СН 2
4,6-диметилгептадиен-1,3

ИЗОМЕРИЯ АЛКАДИЕНОВ
1. Структурная:
а) изомерия углеродного скелета
б) изомерия положения двойных связей.
2. Пространственная:
а)цис-транс изомерия
3. Межклассовая изомерия
(алкины)
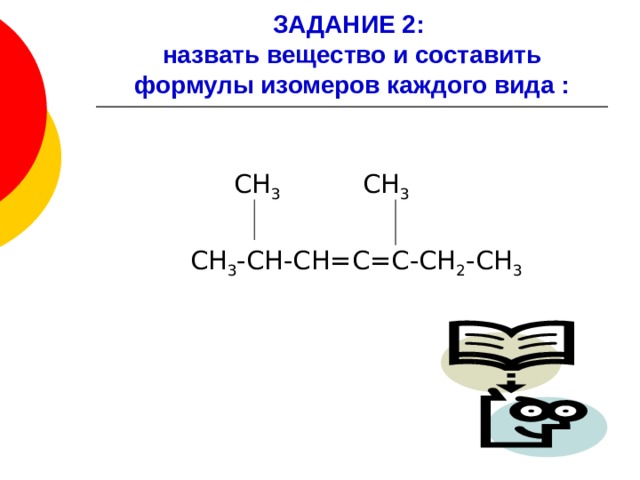
ЗАДАНИЕ 2: назвать вещество и составить формулы изомеров каждого вида :
СН 3 СН 3
СН 3 -СН-СН=С=С-СН 2 -СН 3
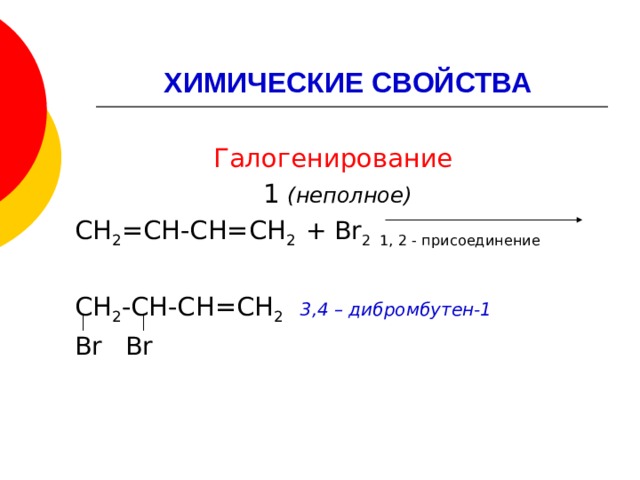
ХИМИЧЕСКИЕ СВОЙСТВА
Галогенирование
1 (неполное)
СН 2 =СН-СН=СН 2 + Br 2 1, 2 - присоединение
СН 2 -СН-СН=СН 2 3,4 – дибромбутен-1
Br Br
ХИМИЧЕСКИЕ СВОЙСТВА
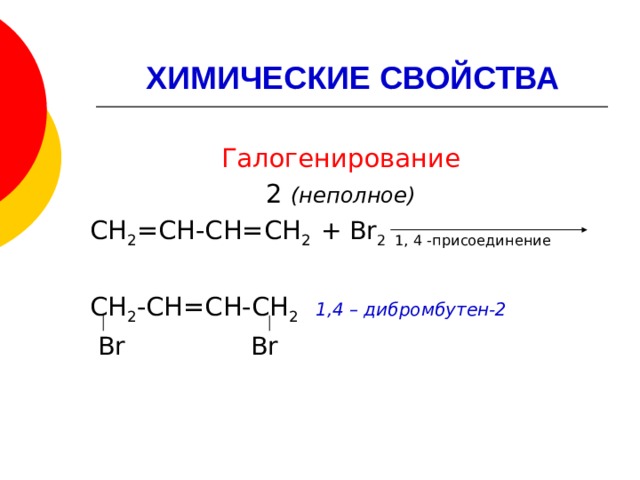
Галогенирование
2 (неполное)
СН 2 =СН-СН=СН 2 + Br 2 1, 4 -присоединение
СН 2 -СН=СН-СН 2 1,4 – дибромбутен-2
Br Br
ХИМИЧЕСКИЕ СВОЙСТВА
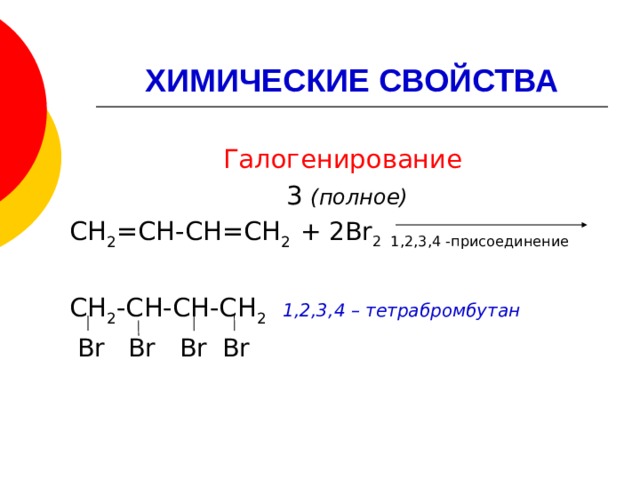
Галогенирование
3 (полное)
СН 2 =СН-СН=СН 2 + 2Br 2 1,2,3,4 -присоединение
СН 2 -СН-СН-СН 2 1,2,3,4 – тетрабромбутан
Br Br Br Br

ЗАДАНИЕ 3: записать уравнения реакций гидрирования бутадиена-1,3 возможными способами:
ОТВЕТ:
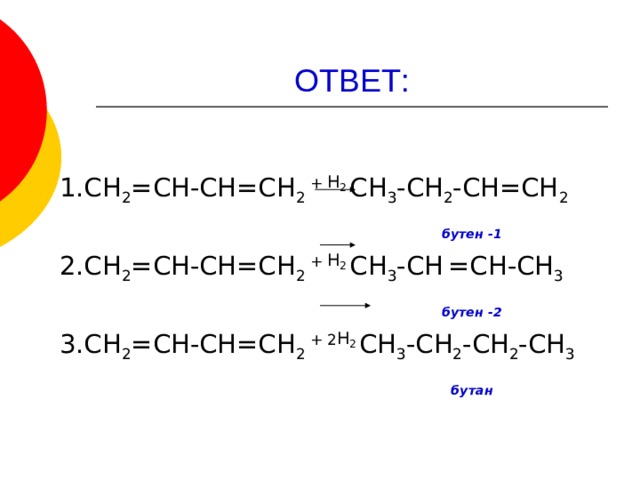
1.СН 2 =СН-СН=СН 2 + Н 2 СН 3 -СН 2 -СН=СН 2
бутен -1
2.СН 2 =СН-СН=СН 2 + Н 2 СН 3 -СН =СН-СН 3
бутен -2
3.СН 2 =СН-СН=СН 2 + 2 Н 2 СН 3 -СН 2 -СН 2 -СН 3
бутан
ХИМИЧЕСКИЕ СВОЙСТВА
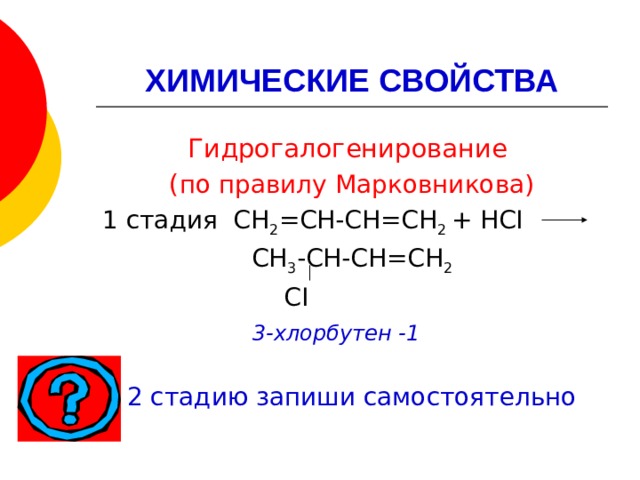
Гидрогалогенирование
( по правилу Марковникова)
1 стадия СН 2 =СН-СН=СН 2 + НСI
СН 3 -СН-СН=СН 2
СI
3-хлорбутен -1
2 стадию запиши самостоятельно
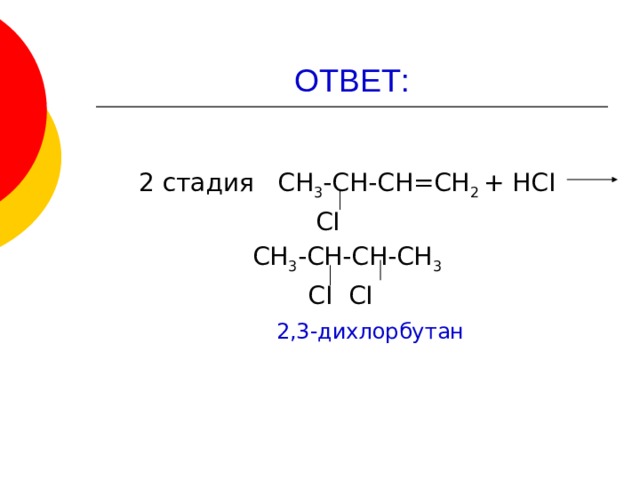
ОТВЕТ:
2 стадия СН 3 -СН-СН=СН 2 + НСI
СI
СН 3 -СН-СН-СН 3
СI СI
2,3-дихлорбутан

ХИМИЧЕСКИЕ СВОЙСТВА
Горение
ЗАДАНИЕ 4: записать уравнение реакции горения бутадиена-1,3
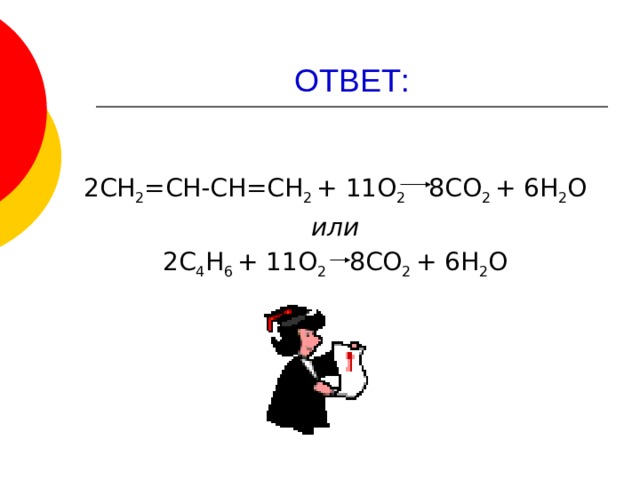
ОТВЕТ:
2СН 2 =СН-СН=СН 2 + 11О 2 8СО 2 + 6Н 2 О
или
2С 4 Н 6 + 11О 2 8СО 2 + 6Н 2 О

ХИМИЧЕСКИЕ СВОЙСТВА
Полимеризация
Полимеризация диеновых УВ приводит
к образованию каучуков – полимеров, обладающих высокой эластичностью.
бутадиеновый каучук
бутадиен -1, 3
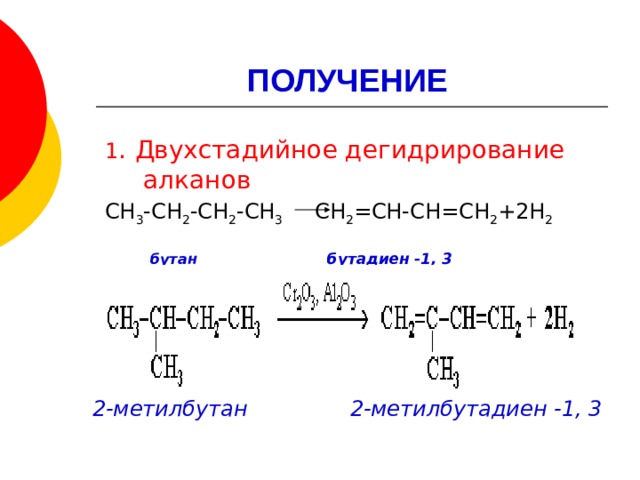
ПОЛУЧЕНИЕ
1 . Двухстадийное дегидрирование алканов
СН 3 -СН 2 -СН 2 -СН 3 СН 2 =СН-СН=СН 2 +2Н 2
бутан бутадиен -1, 3
2-метилбутан 2-метилбутадиен -1, 3

ПОЛУЧЕНИЕ
2. Синтез дивинила по методу
С. В. Лебедева

ДОМАШНЕЕ ЗАДАНИЕ
- учебник стр. 49 стр. задания № 4, 8

СПАСИБО
ЗА
УРОК

















































