|
Историческая справка Открытие Д.И. Менделеевым в 1869 г закона периодической повторяемости свойств химических элементов Опыты Фарадея по электролизу указывали на то, что в состав атомов входят электрически заряженные частицы, заряды кратны заряду электрона, 1879 г Круксом были открыты катодные лучи в опытах по изучению электрического разряда 1897 г Дж. Томсон установил, что катодные лучи являются потоком одинаковых частиц (электроны),1897 г считается открытием электрона. 1909 г Милликен измерил заряд электрона Открытие рентгеновского излучения и радиоактивности Существование линейчатых спектров испускания Опыт Резерфорда 1.Модель атома Томсона – атом однородный шар из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электрона равен положительному заряду атома. Поэтому атом в целом электрически нейтрален. https://www.youtube.com/watch?v=v0j6Gg8_EEY
2. Опыт Резерфорда Просмотр видеоролика https://www.youtube.com/watch?v=0T7DNFbB6tY
3. Модель атома Резерфорда - в центре находится массивное + заряженное ядро, вокруг ядра движутся электроны. Почти вся масса сосредоточена в центре ядра. Работа с учебником стр 73 Недостаток планетарной модели атома: Нельзя объяснить устойчивость атома. Спектр должен быть непрерывным. А он линейчатый Планетарная модель атома, предложенная Резерфордом, – это попытка применения классических представлений о движении тел к явлениям атомных масштабов. Она оказалась несостоятельной. Классический атом неустойчив. Электроны, движущиеся по орбите с ускорением, должны неизбежно упасть на ядро, растратив всю энергию на излучение электромагнитных волн. Заряд атомного ядра впервые точно измерил Г.Мозли в 1913г. В 1920 г. Чедвиг осуществил непосредственные измерения атомного ядра. 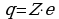 произведение порядкового номера химического элемента в таблице Менделеева на заряд электрона. Порядковый номер химического элемента определяется числом положительных зарядов ядра атома этого химического элемента. Поэтому порядковый номер элемента называют зарядовым числом. произведение порядкового номера химического элемента в таблице Менделеева на заряд электрона. Порядковый номер химического элемента определяется числом положительных зарядов ядра атома этого химического элемента. Поэтому порядковый номер элемента называют зарядовым числом.
Следующий шаг в развитии представлений об устройстве атома в 1913 году сделал выдающийся датский физик Н. Бор. Он сформулировал постулаты, которым должна удовлетворять новая теория о строении атомов. https://www.youtube.com/watch?v=eqO-QnHVRMs Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не излучает. Т.е. атом характеризуется системой энергетических уровней. Механическая энергия электрона, движущегося по замкнутой траектории вокруг положительно заряженного ядра, отрицательна. Поэтому всем стационарным состояниям соответствуют значения энергии En En ≥ 0 электрон удаляется от ядра, становится свободным, т. е. происходит ионизация. Величина |E1| называется энергией ионизации. Состояние с энергией E1называется основным состоянием атома. Частота излучения определяется только изменением энергии атома и никак не зависит от характера движения электрона.
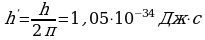 постоянная Планка постоянная Планка
Состав атомного ядра: протоны + нейтроны = нуклоны Z – число протонов в ядре, порядковый номер, зарядовое число A- число нуклонов или массовое число ядра (p+n) N- число нейтронов N=A-Z Изотопы – различные виды одного и того же элемента, отличающиеся числом нейтронов в ядре. Изотоп водорода 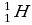 назван протоном назван протоном Работа в паре. Определить состав атомного ядра:
| 






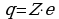 произведение порядкового номера химического элемента в таблице Менделеева на заряд электрона. Порядковый номер химического элемента определяется числом положительных зарядов ядра атома этого химического элемента. Поэтому порядковый номер элемента называют зарядовым числом.
произведение порядкового номера химического элемента в таблице Менделеева на заряд электрона. Порядковый номер химического элемента определяется числом положительных зарядов ядра атома этого химического элемента. Поэтому порядковый номер элемента называют зарядовым числом.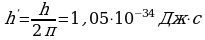 постоянная Планка
постоянная Планка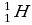 назван протоном
назван протоном

















