
Урок по химии в 10 классе: «Общие способы получения металлов»

Знакомство человека с металлами началось с золота , серебра и меди , то есть с металлов, встречающихся в свободном состоянии на земной поверхности. Впоследствии к ним присоединились металлы, значительно распространенные в природе и легко выделяемые из их соединений: олово , свинец , железо и ртуть . Эти 7 металлов были знакомы человечеству в глубокой древности.

К семи известным металлам уже только в средние века прибавились цинк , висмут , сурьма. В начале XVIII столетия - мышьяк . С середины XVIII века число открытых металлов быстро возрастает и к началу XX столетия доходит до 65, а к началу XXI века — до 96.

В окружающей нас среде химические элементы металлы встречаются как в виде простых веществ (или в свободном виде), так и в виде соединений.

Форма нахождения элементов металлов в естественных условиях зависит от их химической активности. Химически малоактивные металлы (например, медь, золото, серебро, платина, палладий и др.), в природе могут находится в виде простых веществ, так и в виде соединений. Металлы с высокой химической активностью (например, натрий, калий, кальций, алюминий, магний и др.) встречаются в природных условиях только в виде соединений.

Если металл в природных условиях находится в свободном состоянии, то его получение сводится лишь к разделению соответствующих смесей (например, с пустой породой, другими металлами и т.д.). При этом преимущественно используются известные физические методы разделения смесей.

Однако большинство металлов получают в результате химических реакций из руд. Руда – природное минеральное образование, в котором атомы химических элементов (в частности, металлов) находятся в окисленном состоянии.

Чтобы получить металлы из руды в свободном состоянии, необходимо провести процесс восстановления: Me n+ + ne - = Me . Для этого используют различные восстановители (например, водород, более активные металлы, углерод (в виде кокса), СО, постоянный электрический ток).

Технологические процессы, лежащие в основе промышленных способов получения металлов из руд, можно разделить на: - пирометаллургические, - гидрометаллургические, - электрометаллургические. В пирометаллургии для преобразования руды в металлическое сырьё используются высокие температуры и различные восстановители. В гидрометаллургических методах процесс восстановления протекает в водном растворе. В электрометаллургических процессах восстановителем является постоянный электрический ток.

Восстановление с помощью водорода
Водород как восстановитель может использоваться для получения металлов со средней и малой активностью из их соединений (чаще всего оксидов), например меди, вольфрама, молибдена. Восстановление протекает при нагревании соответствующего оксида в токе газообразного водорода:
WO 3 +3H 2 =W+3H 2 O
CuO+H 2 =Cu+H 2 O
Восстановить до металла оксиды активных ( Na, Ca, Al, Mg ) металлов с помощью водорода невозможно.

Восстановление металлами (металлотермия)
Металлы используются в качестве восстановителей для получения других металлов из самых различных соединений. Метод получения металлов из их соединений с помощью алюминия называется алюмотермией. Например, алюминий используется в промышленности для получения кальция из его оксида, а металлический кальций используют для получения цезия:
4 CaO+2Al=Ca(AlO 2 ) 2 +3Ca
Ca+2CsCl=CaCl 2 +2Cs

При высокой температуре углерод и оксид углерода( II ) являются сильными восстановителями: CuO+CO=Cu+CO 2 PbO+C=Pb+CO

Свободный углерод (в виде кокса) и оксид углерода (II) служат восстановителями при промышленном производстве железа в доменном процессе. Для этого смесь железной руды (магнетита Fe 3 O 4 , красного или бурого железняков Fe 2 O 3 ) с коксом нагревают до высокой температуры. Протекающие при этом процессы можно выразить суммарно следующими схемами: C+CO 2 →2CO Fe 2 O 3 +C( или CO)→Fe 3 O 4 +CO 2 В результате в металле остается как примесь продукт его взаимодействия с углеродом – карбид железа Fe 3 C.

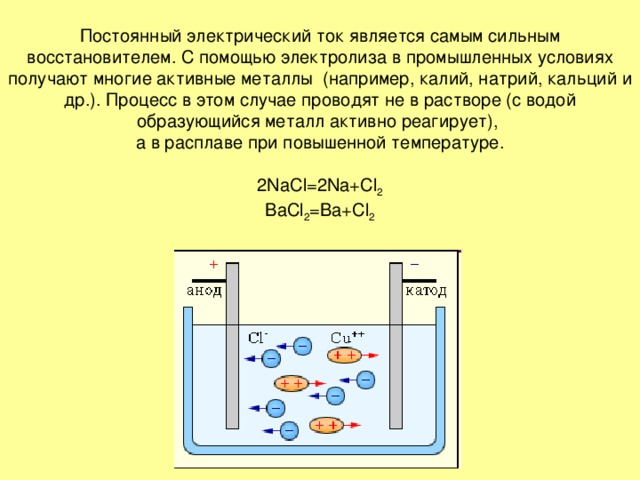
Постоянный электрический ток является самым сильным восстановителем. С помощью электролиза в промышленных условиях получают многие активные металлы (например, калий, натрий, кальций и др.). Процесс в этом случае проводят не в растворе (с водой образующийся металл активно реагирует), а в расплаве при повышенной температуре. 2NaCl=2Na+Cl 2 BaCl 2 =Ba+Cl 2

Весь производимый в промышленных масштабах алюминий получают путем электролиза раствора оксида алюминия в расплавленном криолите Na 3 AlF 6 . Протекающий при этом процесс упрощенно можно выразить суммарным уравнением: 2 Al 2 O 3 =4Al+3O 2

Домашнее задание:

Список используемых источников
- http://ru.wikipedia.org/wiki/Каменноугольный_кокс
- http://ru.wikipedia.org/wiki/Серебро
- http://www.vostok-met.ru/wp-content/uploads/2011/02/image014.jpg
- http://www.dekatop.com/wp-content/uploads/2011/07/gold_01.jpg
- http://files.school-collection.edu.ru/dlrstore/5ca811f4-7aea-42ca-b5da-534dfd445e6c/IMG_0861.JPG
- http://www.asia.ru/images/target/img/product/11/90/18/11901863.jpg
- http://www.rmms.ru/userFiles/image/Металлургия.jpg
- http://inventions.ru/i/photo/aluminium1.jpg
- http://artdesign21.narod.ru/image/1/4951011bc5f764b6ef74e651154_prev.jpg











































