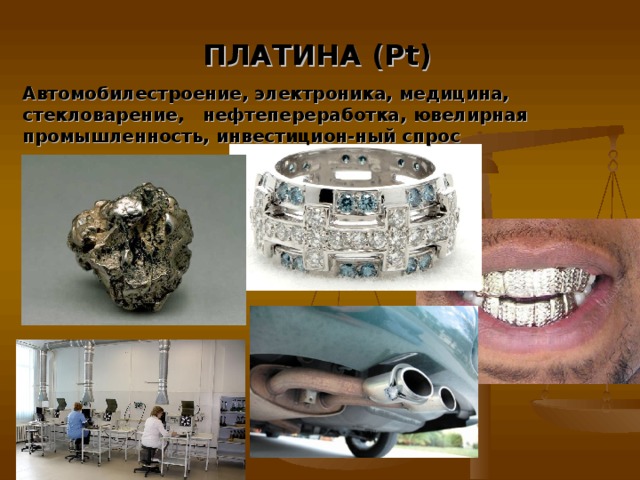
МЕТАЛЛЫ
обобщающий урок с использованием интерактивной технологии кооперативного обучения «Карусель»
Металлы отверзают недро земное к плодородию; металлы
служат нам в ловлении земных и морских животных для
пропитания нашего; металлы облегчают купечество
удобную к сему монетою… И кратко сказать, ни едино
художество, ни едино ремесло простое употребления
металлов миновать не сможет.
М.Ломоносов.
Цель урока: обобщить, систематизировать знания учащихся о расположении металлов в периодический системе, их строении и свойствах; развивать умение критически мыслить, реализовывать полученные знания на практике, способность к сотрудничеству и ответственному поведению; воспитывать чувство солидарности, стремление постичь сущность, такие социальные качества как дисциплинированность, способность высказывать свое мнение, слушать других.
1. Организационный этап урока.
2. Мотивация учебно-познавательной деятельности учащихся.
Сейчас мы не представляем своей жизни без металлов и их сплавов. И куда бы не бросил взгляд – металлы всегда рядом. Они помогают человеку обрабатывать землю, строить, готовить еду, лететь в космос, обогревать и освещать жилища, добывать полезные ископаемые. Изучив данную тему, мы выяснили суть многих физических и химических процессов, происходящих с металлами. Сегодня нам нужно повторить и обобщить, привести знания в стройную систему и научиться применить их в практической деятельности, а возможно, и в нестандартных ситуациях.
3. Объявление темы и ожидания результатов.
На уроке мы обобщим знания по теме «Общая характеристика металлов» на уровне их применения в повседневной жизни, продолжим формирование таких общечеловеческих ценностей, как способность к сотрудничеству, ответственному поведению, способность не только выражать свое мнение, но и слушать других. Тест в конце урока оценит степень сформированности ваших компетентностей по теме.
4. Предоставление необходимой информации.
«Необычное в обычном»
Демонстрируются образцы металлов, продолжается обсуждение областей их применения, звучит много интересных фактов о металлах, которые свидетельствуют, что рядом много необычного.
Мg – в 1,5 раза легче «крылатого» алюминия, широко используется в пиротехнике. Нагретый на воздухе до 550 С, он вспыхивает и мгновенно сгорает ослепительным ярким пламенем.
Легкость могла бы сделать этот металл прекрасным конструкционным материалом, но чистый магний мягкий и непрочный. Применяется в виде сплавов с Al, Zn, Mn. Участвует в фотосинтезе, так как входит в состав хлорофилла.
Биологи Франции установили интересное влияние Са и Мg на пол потомства: если пища матери богата этими элементами, то в потомстве преобладал женский пол.
Li – самый легкий из легких.
Аналитическим путем установлено, что вместе со стаканом горячего чая мы выпиваем около 10-15 мг стекла. Если при извлечении стекла к нему добавить Li, его растворимость уменьшится в 100 раз. Используется в металлургии, входит в состав электролита аккумуляторов, является ракетным топливом.
Cs – металл, который можно расплавить на ладони – t пл. = 28,5 С (второй после ртути). От воздуха он легко загорается, при действии воды – со взрывом воспламеняется, бурно реагирует даже со льдом.
Используется для получения вакуума при изготовлении радиоламп.
Соли цезия применяются в медицине для лечения некоторых язвенных процессов.
Ba – помощник врачей.
Мягкий, легко загорается в воздухе от удара. Барий – замечательный поглотитель рентгеновских лучей, поэтому защитные стенки медицинского рентгеновского оборудования делают из кирпича, содержащий соединения Ва. Бариева «каша» (BaSO4) применяют при рентгеновских исследованиях желудка, потому BaSO4 задерживает рентгеновские лучи больше, чем мягкие ткани организма; это дает возможность найти анатомические изменения. Смесь BaSO4 та ZnSO4 называют белилами, применяют в малярном деле. Ва(NO3)2 окрашивает пламя в зеленый цвет, что придает феєрверкам зеленых огней.
Fe – строитель Вселенной, основа всей металлургии, машиностроения, железнодорожного транспорта, судостроения, грандиозных инженерных сооружений. Fe входит в состав гемоглобина крови, ним богата печень и селезенка. Участвует в окислительных процессах растительных организмов.
Tl (тантал) – металл высокой чистоты, незаменимый в хирургии, так как имеет превосходное свойство: не раздражает живых тканей, хорошо обрабатывается, на него не действует ни один медикамент.
«Картинная галерея»
Взгляните на эту картину и запишите в тетрадь 3-4 слова, обозначающие предметы, изображенные на этой картине. Найдите в периодический системе элементы, которые начинаются с такой же буквы, что и выписанные слова. Это элементы металлические или неметаллические? Как определили? Где именно размещены металлические элементы в периодической системе?
Особое строение атомов обусловливает характерные особенности строения вещества. Таким образом:
Что общего в строении атомов металлических элементов?
2. За счет чего образуются металлическая связь? (слайд № 1)
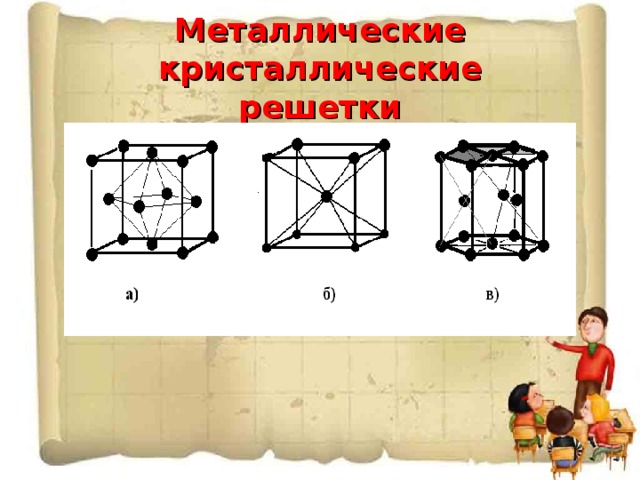
3. Виды и строение металлических кристаллических решеток (слайд № 2)
4. Характерные физические свойства металлов (слайд № 3)
«Химическое домино»
Эта игра позволит обобщить знания химических свойств металлов. У вас в руках карточки с изображением второй части уравнений химических реакций, характерных для металлов. Первая – на флип-чарте. Соединим их для образования схем реакций и превратим их в химические уравнения.
C →
 u + НCl
u + НCl
C → CuCl2 + Au
u + Au Cl3
B → Ba O
a + O2
B → Ba (OН)2 +Н2
a + Н2O
Z → Zn Cl2 + Cu
n + Cu Cl2
F → Fe Cl2 + Н2
e + НCl
Так с какими же веществами вступают в реакцию металлы? (слайд № 4)
5. Интерактивное упражнение «Карусель» (технология кооперативного обучения)
Упражнение одновременно включает в активную работу по общению для обсуждения вопросов всех учащихся класса. Оно проверяет глубину имеющихся знаний и развивает умение аргументировать собственную позицию и способность к сотрудничеству.
Каждый ученик, который сидит во внешнем круге, имеет лист с конкретным вопросом и во время перемещения собирает максимум информации, взглядов по указанному вопросу. В конце ответы заслушиваются, определяются вопросы особенно сложные, продуктивные, те, которые быстро иссякли, а также анализируется работа партнеров.
Вопросы для интерактивного упражнения:
1. Почему медь более пластична, чем цинк?
2. В электрохимическом ряду напряжений металлов алюминий занимает позицию достаточно активного металла. Жизненный опыт говорит о химическую пассивность металла (посуда). Опровергните это несоответствие.
3. Почему металлы в отличие от большинства твердых неметаллических веществ проводят электрический ток?
4. Почему натрий хранят под слоем керосина или парафина?
5. Чем обусловлена непрозрачность и металлический блеск металлов?
6. Почему в 1912 году погибла экспедиция английского исследователя Роберта Скотта, которая направлялась к Южному полюсу?
Слайд-ответы:
№ 1


медь цинк
(кубическая гранецентрированная) (гексагональная плотноупакованная)
№ 2 4 Al + 3O2 → 2 Al2O3
Поверхность (неполированная) алюминия покрыта защитной оксидной пленкой, на которую не действуют вода, кислоты.
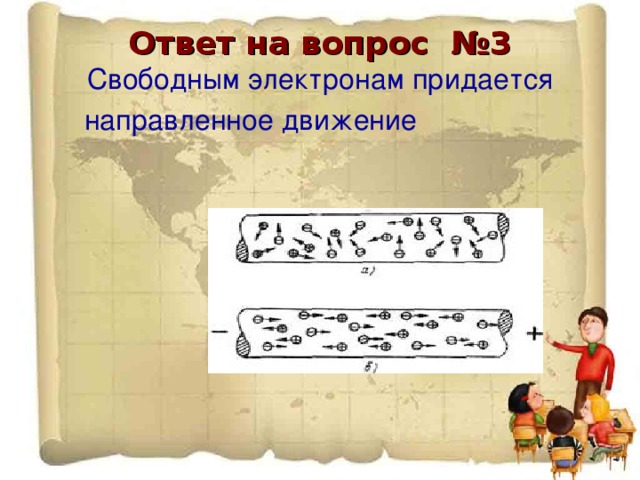
№ 3
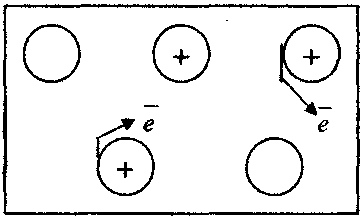
Свободным электронам придается
направленное движение
№ 4 4Na + O2 → 2 Na2O
№5 «Электронный газ» часть лучей солнечного света может поглощать (непрозрачность) а часть отражать (металлический блеск)

№ 6 Посуда с горючим экспедиции была запаяна оловом, которое при низких температурах стало хрупким и рассыпалось в порошок. Горючее вытекло.
Переход пластичного белого олова в порошковидное серое олово при низких температурах получил название «оловянная чума».
6. Подведение итогов урока.
Подводим черту под знаниями, которые повторены, оглянемся на события, произошедшие на уроке, составив Ретро-план и воссоздав последовательность эффективных и продуктивных форм работы (флип-чарт).
7. Оценивание результатов урока.
......, ......., ........, ........, ......... умело в течение урока подбирали необходимую информацию, логически обосновали утверждения, отделяли факты от субъективного мнения, выделяли причинно-следственные связи, делали выводы и поэтому получают за работу на уроке оценку «5». Это оценка навыков мышления.
Оценка же знаний состоится с помощью теста, задание которого заключается в выборе одного правильного ответа.
Вариант 1 Вариант 2
1. Металл, имеющий наиболее 1. Металл, имеющий наивысшую
выраженный металлический блеск температуру плавления
А Na А Zn
Б Al Б W
В Ag В Co
2. Металл, имеющий самую низкую 2. Металл,имеющий наибольшую
температуру плавлення: плотность:
А K А Os
Б Ag Б Fe
В Hg В Ca
3. Самый твердый металл: 3. Самый легкий металл:
А Co А Cu
Б Ni Б Al
В Cr В Zn
4. Наиболее электропроводный 4. Самый мягкий металл:
металл:
А Cu А Na
Б Al Б Al
В Ag В Ba
5. Что общего в строении атомов 5. Що общего в строении атомов елементов с порядковыми элементов с порядковыми номерами
номерами 11 и 19: 12 и 20:
А заряд ядра атома А заряд ядра атома
Б количество электронных уровней Б количество электронных уровней
В количество электронов на В количество электронов на на внешнем уровне внешнем уровне
6. С водой не взаимодействует: 6. С соляной кислотой не взаимодействует:
А Cu А Cu
Б Fe Б Fe
В Zn В Zn
7. Название химического 7. Название химического
соединения CaH2 соединения Al2S3
А гидрат кальция А сульфид алюминия
Б гидроксид кальция Б сульфит алюминия
В гидрид кальция В сульфат алюминия
8. Установите соответствие между металлами и их физическими свойствами:
А K 1. Тугоплавкий металл А Na 1.В обычных условиях – жидкость Б W 2. Красный металл Б Au 2. Плавится в горячей воде
В Cu 3. Мягкий, легко режется В Ag 3. Желтый металл
ножем Г Hg 4. Металл с высокой
Г Fe 4. Серебристо-серый металл электропроводностью
с высокой пластичностью
8. Информация о домашнем задании.
Предлагается специальное домашнее задание, что подлежит оцениванию «Если бы когда-то...» Это эссе, в котором нужно подать идеи относительно проблемного вопроса: что было бы, если бы человек не научился добывать металлы из руд?





 u
u