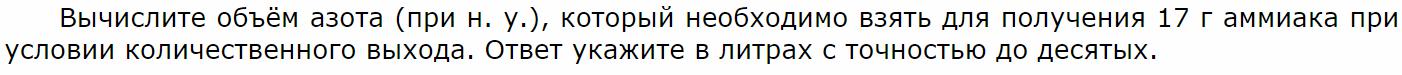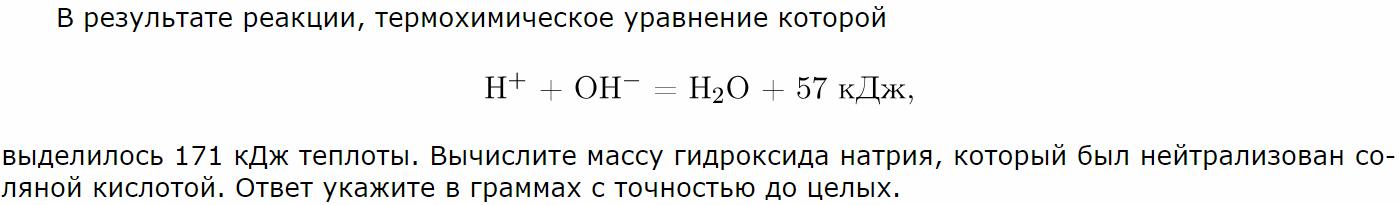Подготовка учащихся к ЕГЭ по химии в рамках ФГОС
Решение задач по общей химии.


Моль - количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 12 г. При применении моля структурные элементы должны быть специфицированы и могут быть атомами, молекулами, ионами, электронами и другими частицами или специфицированными группами частиц.
Примерное определение моль
Моль - единица количества вещества, в котором содержится число Авогадро (NA=6,022140857(74)⋅1023 моль−1) структурных элементов.
Моль является одной из основных единиц измерения СИ.
Формулы для решения задач по химии
n – количество вещества, [моль]
m – масса вещества, [г]
M – молярная масса, [г/моль]
N – число атомов, молекул, ионов и пр., [безразмерная величина]
NA – число Авогадро, NA = 6,02∙1023 [1/моль]
T – температура, [К]
P – давление газа, [атм], [Па], [мм. рт. ст.]
– объем, [л], [м3]
Vm – молярный объем, при н. у. для газов Vm = 22,4 [л/моль]
– концентрация вещества, [моль/л]
R – универсальная газовая постоянная, R = 8,31 [Дж/(моль∙К)], если давление в Па, а объем в м3; R = 0,082, если давление в атм, а объем в л.
– плотность вещества, [г/мл]
Dy(x) – относительная плотность газа X по газу Y, [безразмерная величина]
ω – массовая доля, [%] χ – мольная доля, [%] φ – объемная доля, [%]
– выход продукта реакции, [%]
Q – количество теплоты, [кДж]
Qобр – теплота образования вещества, [кДж/моль]
Qобр – количество теплоты выделяющейся при образовании 1 моль вещества из простых веществ, находящихся в устойчивых состояниях при стандартных условиях.
Qобр=Q/n
Количество вещества через массу:
| n | т | т n M |
| т |
|
|
|
|
|
|
| M | M n |
|
|
|
|
|
Количество вещества через объем:
Количество вещества через число частиц:
Массовая доля вещества в растворе (смеси, руде и т.д.):

т(вещества )
т( раствора) 100%

т(вещества ) m( раствора) (вещества )

100%
Массовая доля элемента в соединении:

Мольная доля вещества в смеси

n(вещества )
n(смеси) 100%

n(смеси) (вещества )
n(вещества )

100%
Объемная доля вещества в смеси

V (вещества )
V (смеси) 100%

(вещества ) V (смеси) (вещества ) 100%

Концентрация вещества
n(вещества )
С(вещества )

V ( раствора)
n(вещества) V ( раствора) C(вещества)
n(вещества )
V ( раствора)

C(вещества )
Связь массы, объема и плотности
Vт V т т V


9. Относительная плотность газа X по газу Y

Выход продукта реакции
| | m(практическая) | 100% | n(практическое) | 100% |
| V (практический) | 100% |
|
| m(теоретическая) | n(теоретическое) | V (теоретический) |
|
|
|
|
|
|
|
Уравнение состояния идеального газа:
P∙V=n∙R∙T
1 л = 1 дм3 = 1000 мл = 0,001 м3
1 атм = 101 325 Па = 760 мм рт ст; 1 бар=100000 Па=100 кПа
0° C = 273 К, 100° C = 373 К
Нормальные условия (н. у.): P = 1 атм, T = 273 К
Стандартные условия: P = 1 бар, T = 298 К
Типы задач ЕГЭ.
Расчеты массы вещества или объема газа по известному количеству вещества, массе или объему одного из участвующих в реакции веществ.

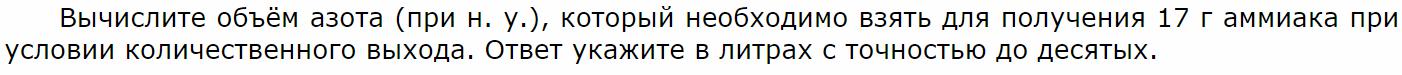
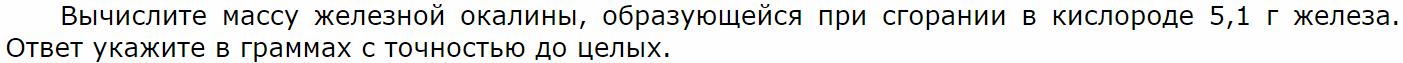



Расчеты объемных отношений газов при химических реакциях.

Расчеты по химическим уравнениям, если одно из веществ дано в избытке.

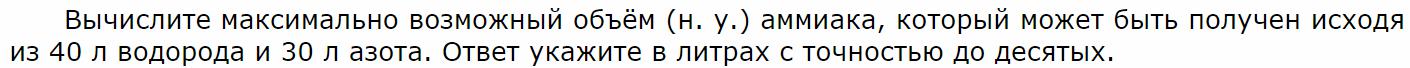

Задачи на выход продукта реакции.



Расчеты по термохимическим уравнениям.

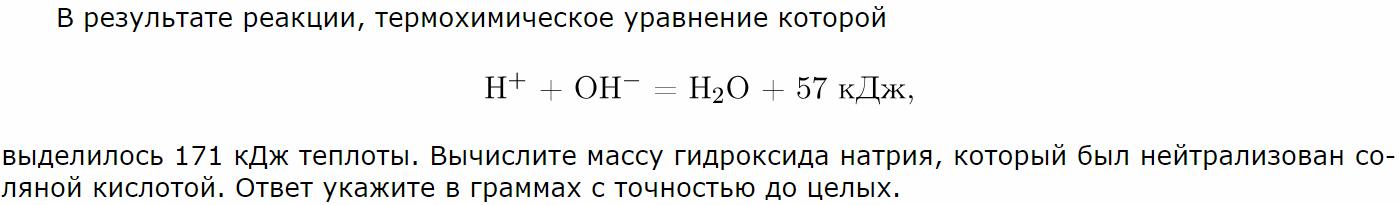

Задачи на примеси.

Чтобы верно решить задачи №34 нужно:
•Верно составлять уравнения реакций (особенно ОВР, электролиз, кислые и основные соли, реакции разложения…), не забывать про коэффициенты.
•При расчете массы раствора помнить, что массы осадков и газов не входят в массу
раствора.
•Уметь определять избыток/недостаток.
•иметь представление о кристаллогидратах , уметь находить их молярные массы и учитывать кристаллизационную воду в расчетах.
•Обладать базовыми знаниями математики и уметь считать на калькуляторе.
•Знать формулы для расчета физических величин, применяемых в химии.





Установление формулы вещества по уравнению реакции и определении молярной массы.
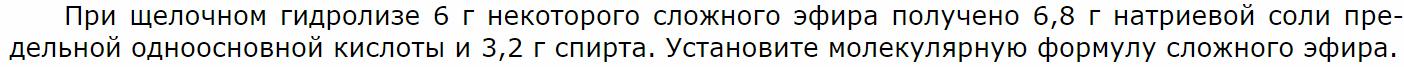






Установление формулы вещества по уравнению реакции сгорания. Обычно в таких задачах используют относительную плотность паров вещества.




Задачи на нахождение молекулярной формулы вещества через массовые доли элементов.