
©Хасанов Дилшод Наимович
©Тобольский медицинский колледж им. В.Солдатова

ЭТАН, ПРОПАН И БУТАН входят в состав природного и попутного нефтяного газов.
АЛКАНЫ содержатся в нефти.

Крупнейшие месторождения природного газа в России:
Уренгой Ямбург Штокмановское
Ленинградское Русановское Заполярное
Медвежье Астраханское
Западно-Камчатский шельф Сахалин-3

Проблемный вопрос: Почему алканы называются «предельными углеводородами»?
АЛКАНЫ ( предельные, насыщенные, парафины) - это углеводороды с общей формулой С п Н 2п + 2 в молекулах которых между атомами углерода имеются только одинарные (сигма) связи , не способные на реакции присоединения.
В молекулах алканов имеются только одинарные - связи. Все четыре валентности атома углерода в молекулах алканов полностью, т.е. до предела, насыщены атомами углерода и водорода. Между атомами углерода отсутствуют кратные связи. Отсюда происходят другие названия этих углеводородов - насыщенные или предельные.

Вспомните, какие вещества мы называем гомологами?
ГОМОЛОГИ – это вещества со схожими строением и свойствами, но различающиеся по составу на одну или несколько групп CH 2 ( гомологическая разность).
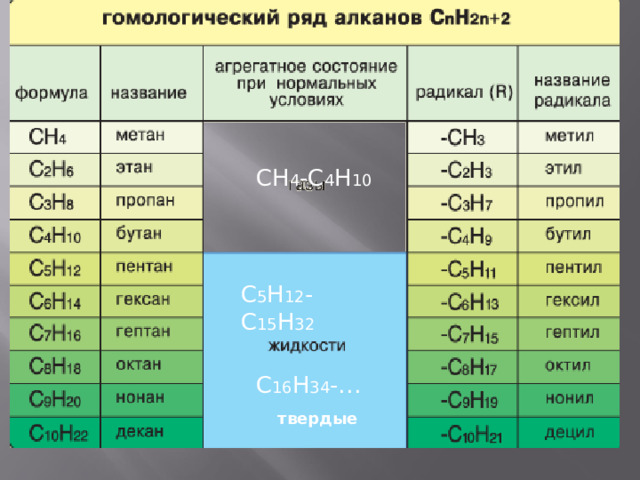
СН 4 -С 4 Н 10
С 5 Н 12 -С 15 Н 32
С 16 Н 34 -…
твердые
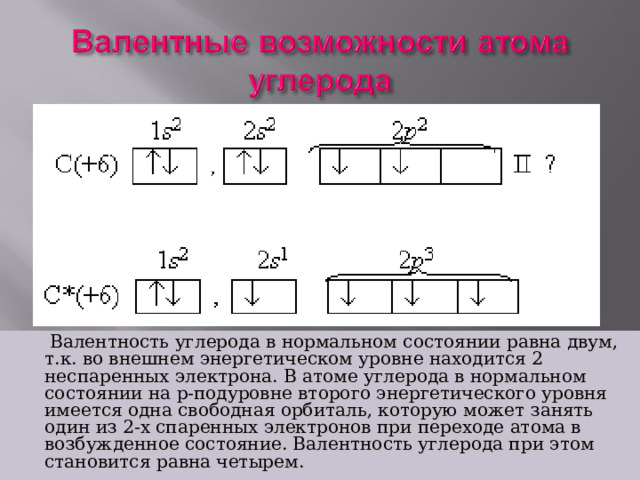
Валентность углерода в нормальном состоянии равна двум, т.к. во внешнем энергетическом уровне находится 2 неспаренных электрона. В атоме углерода в нормальном состоянии на р-подуровне второго энергетического уровня имеется одна свободная орбиталь, которую может занять один из 2-х спаренных электронов при переходе атома в возбужденное состояние. Валентность углерода при этом становится равна четырем.
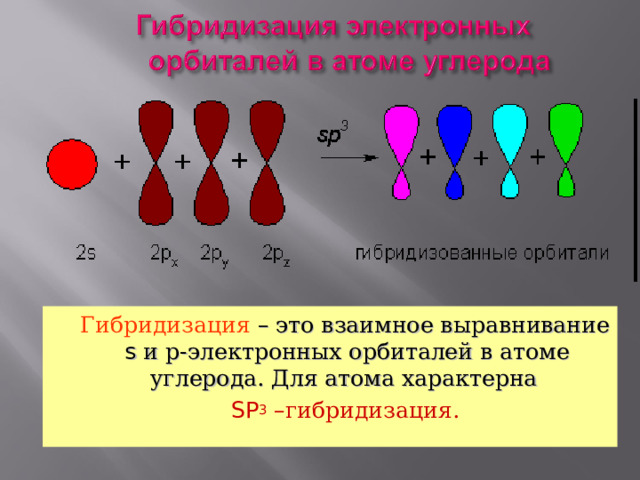
Гибридизация – это взаимное выравнивание s и р-электронных орбиталей в атоме углерода. Для атома характерна
SP 3 –гибридизация.

В алканах все четыре неспаренных электрона у углеродных атомов участвуют в процессе гибридизации. Такой процесс называется
SP 3 – гибридизация

- Какие вещества входят в состав природного и попутного нефтяного газов?
- Что такое алканы?
- Что такое гомологи?
- Назовите общую формулу гамологов
- Перечислите первые 3 вещества гомологического ряда алканов

- 1)Этан, пропан и бутан
- 2) Алканы - углеводороды с общей формулой Сп Н2п + 2 в молекулах которых между атомами углерода имеются только одинарные (сигма) связи, не способные на реакции присоединения.
- 3) ГОМОЛОГИ – это вещества со схожими строением и свойствами, но различающиеся по составу на одну или несколько групп CH2 (гомологическая разность).
- 4) CnH2n+2
- 5) Метан, этан, пропан
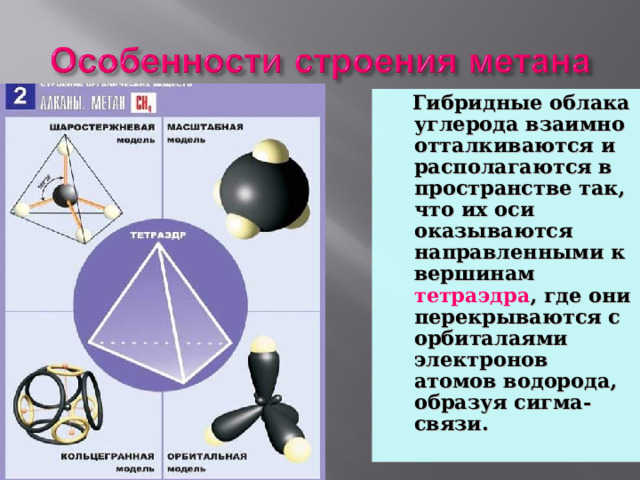
Гибридные облака углерода взаимно отталкиваются и располагаются в пространстве так, что их оси оказываются направленными к вершинам тетраэдра , где они перекрываются с орбиталаями электронов атомов водорода, образуя сигма-связи.
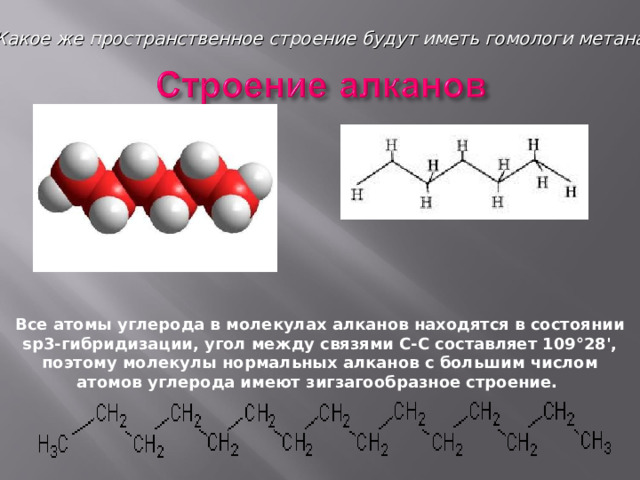
Какое же пространственное строение будут иметь гомологи метана?
Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации, угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение.

Тип гибридизации углерода в алканах определяет направление гибридных электронных облаков в пространстве к вершинам тетраэдра . Такое же пространственное строение имеет и пакет молока.
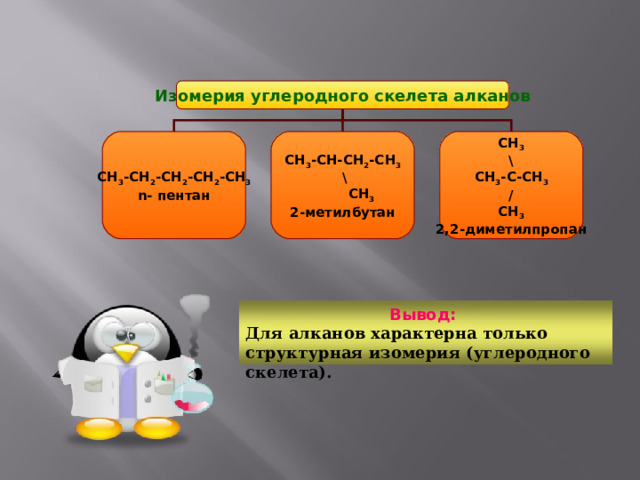
Изомерия углеродного скелета алканов
СН 3 -СН 2 -СН 2 -СН 2 -СН 3
n- пентан
СН 3 -СН-СН 2 -СН 3
\
СН 3
2-метилбутан
СН 3
\
СН 3 -С-СН 3
/
СН 3
2,2-диметилпропан
Вывод:
Для алканов характерна только структурная изомерия (углеродного скелета).
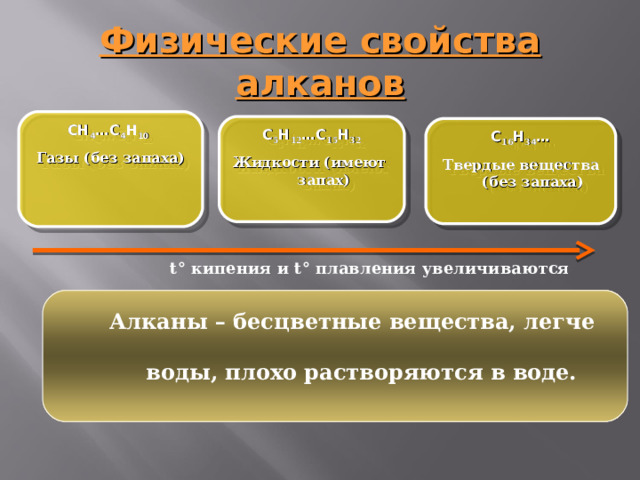
Физические свойства алканов
CH 4 …C 4 H 10
Газы (без запаха)
C 5 H 12 …C 15 H 32
Жидкости (имеют запах)
C 16 H 3 4 …
Твердые вещества (без запаха)
t ° кипения и t ° плавления увеличиваются
Алканы – бесцветные вещества, легче воды, плохо растворяются в воде.

Алгоритм составления названий органических соединений
(3) (4) (5) (6) (7)
СН 3 – СН – СН 2 – СН 2 – СН 2 – СН – СН 2 – СН 3
! !
(2) СН 2 СН 2 – СН 2 – СН 3
! ( 8) (9) (10 )
(1) СН 3
Данное вещество называется: 3-метил, 7-этил дек ан
- Данное вещество называется: 3-метил, 7-этил дек ан
1. Выбирают наиболее длинную (главную) цепь и нумеруют ее ближе к тому концу, к которому стоит радикал ( заместитель, обозначен желтым цветом).
2. Название строится в следующей последовательности:
А) ПРЕФИКС: состоит из цифры, указывающей на номер углеродного атома, возле которого стоит радикал. Например: 3- и пишется название самого радикала. Например: 3-метил,7-этил……. Если молекула содержит несколько одинаковых радикалов, то после перечисления всех цифр, указывающих их местоположение, к радикалу добавляют числовую приставку ( ди –два, три – три, тетра – четыре). Например: 2,3 – диметил………….., или 3,4,5 – триэтил…….
Б) КОРЕНЬ: ставится в соответствии с гомологическим рядом алканов ( смотрите по количеству атомов углерода в главной цепи)
В) СУФФИКС : у алканов суффикс «АН».
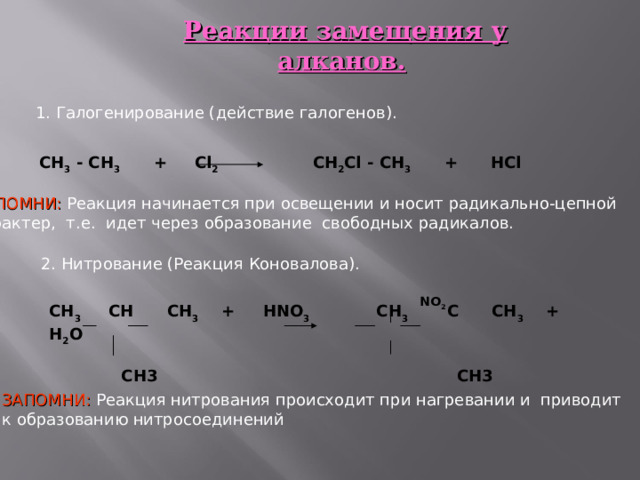
Реакции замещения у алканов.
1. Галогенирование (действие галогенов).
СН 3 - СН 3 + С l 2 CH 2 Cl - CH 3 + HCl
ЗАПОМНИ: Реакция начинается при освещении и носит радикально-цепной
характер, т.е. идет через образование свободных радикалов.
2. Нитрование (Реакция Коновалова).
CH 3 CH CH 3 + HNO 3 CH 3 C CH 3 + H 2 O
CH 3 CH 3
NO 2
ЗАПОМНИ: Реакция нитрования происходит при нагревании и приводит
к образованию нитросоединений

А) Горение
C n H 2 n +2 + O 2 CO 2 + H 2 O

Б) Каталитическое окисление алканов.

1. Пиролиз
При сильном нагревании без доступа воздуха происходит полное разложение алканов на простые вещества.
CH 4 C + 2 H 2
t°C
t°C
C 16 H 34
+
C 8 H 18
C 8 H 16
гексадекан
октан
октен


Запомни!

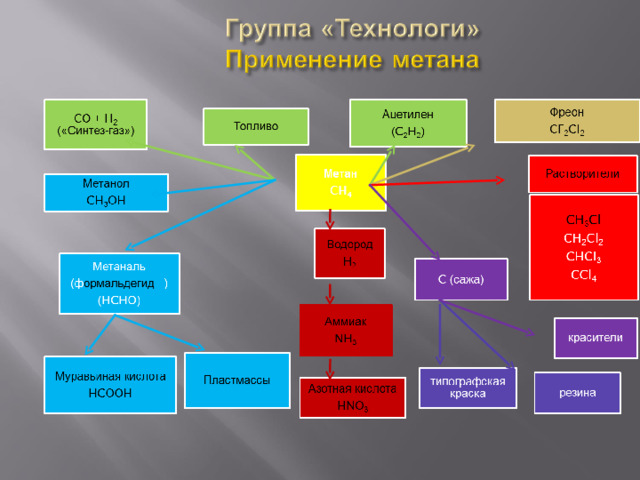
а) из природного газа;
б) синтез из оксида углерода ( II ) и водорода (из синтез-газа):
а) гидролиз карбида алюминия:
б) сплавление солей уксусной кислоты (ацетатов) со щелочами:
Ni, 300°C
H 2 O
+
CH 4 ↑
3
H 2
CO
+
+
Al 4 C 3
H 2 O
+
CH 4 ↑
3
12
Al(OH) 3
4
t°
Na 2 CO 3
+
CH 4 ↑
NaOH
+
CH 3 COONa
(твердый)
ацетат натрия
(твердый)
15
15
15
15

Тест
1.Гомологический ряд алканов
описывается общей формулой
а) С nH 2 n -2
б) CnH 2 n
в) С nH 2 n +2
г) CnH 2 n +1
2. Молекула метана имеет форму
а) пирамиды
б) параллепипеда
в) тетраэдра
г) конуса
3. Для алканов характерна гибридизация:
а) SP
б) SP 2
в) SP 4
г) SP 3
4. Радикал – это
а) группа атомов с неспаренными электронами
б) группа атомов, отличающаяся от метана на СН 2 -
в) группа атомов, имеющая положительный заряд
г) функциональная группа атомов,
5. Формулы только алканов записаны в ряду:
а) С 3 Н 6 , С 2 Н 4 , С 6 Н 14
б) С 4 Н 10 , С 2 Н 6 , С 3 Н 8
в) С 2 Н 2 , С 3 Н 8 , С 6 Н 6
г) С 6 Н 6 , С 4 Н 8 , С 2 Н 6
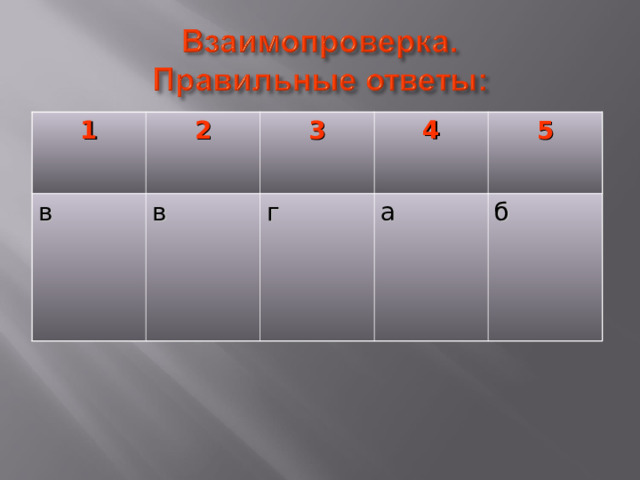
1
2
в
3
в
4
г
5
а
б

а. C 4 H 10 + O 2 =
б. этан + Cl 2 =
в. C 5 H 12 →
t°C
 CH3-CH2Cl + HCl В) с5 h12 = ch3-ch (ch3) - ch2-ch3 " width="640"
CH3-CH2Cl + HCl В) с5 h12 = ch3-ch (ch3) - ch2-ch3 " width="640"
- А) 2 С4Н10 + 13 О2 = 8 СО2 + 10 Н2О
- Б) CH3CH3 + Cl2 ---- CH3-CH2Cl + HCl
- В) с5 h12 = ch3-ch (ch3) - ch2-ch3

В состав органического вещества входит углерод, массовая доля которого – 92,23% и водород массовая доля которого 7,77%. Относительная плотность паров этого вещества по водороду равна 13. Определите молекулярную формулу вещества.

- Проанализируем входит ли в состав органического вещества кислород. Все вещество это 100%, значит 100-92,23-7,77=0, значит кислород отсутствует. Рассчитаем молярную массу органического вещества: M ( СхНу ) = Д (Н2) * М (Н2); M ( СхНу ) = 13*2=26; n(C)=(W(C)*M(CxHy))/M(C)*100 n(C)=(92,23*26)/12*100 = 2; n(Н)=(W(Н)*M(CxHy))/M(Н)*100; n(Н)=(7,77*26)/1*100 = 2; Проверяем подсчитав молярную массу С2Н2. М (С2Н2)=12*2+2=26 г/моль. Ответ: органическое вещество имеет формулу - С2Н2.


































 CH3-CH2Cl + HCl В) с5 h12 = ch3-ch (ch3) - ch2-ch3 " width="640"
CH3-CH2Cl + HCl В) с5 h12 = ch3-ch (ch3) - ch2-ch3 " width="640"




















