Просмотр содержимого документа
«Лабораторная работа №19 «Исследование свойств белков как биологических полимеров»»

Лабораторная работа
«Исследование свойств белков»
«Исследование свойств белков, как биологических полимеров»
Название опыта
Ход работы
Наблюдения
Уравнения реакций
Выводы
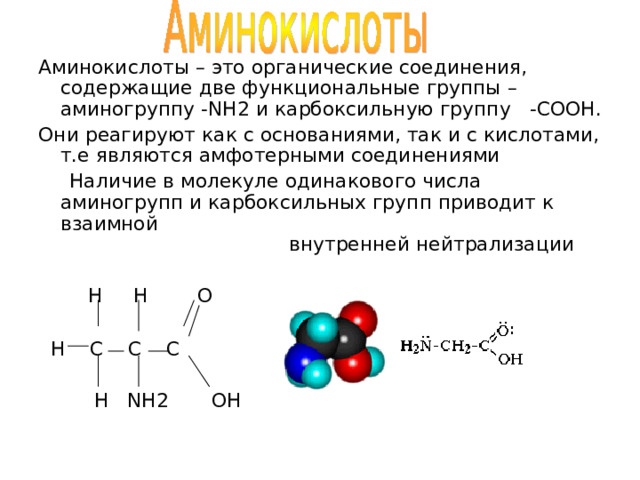
Аминокислоты – это органические соединения, содержащие две функциональные группы – аминогруппу -NH2 и карбоксильную группу -COOH .
Они реагируют как с основаниями, так и с кислотами, т.е являются амфотерными соединениями
Наличие в молекуле одинакового числа аминогрупп и карбоксильных групп приводит к взаимной внутренней нейтрализации
H H O
H C C C
H NH2 OH

- Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом.
- Реагируют со спиртами, образуя сложные эфиры.

- Аминокислоты могут реагировать друг с другом : карбоксильная группа одной аминокислоты реагирует с аминогруппой другой аминокислоты с образованием пептидной связи и молекулы воды-реакция поликонденсации
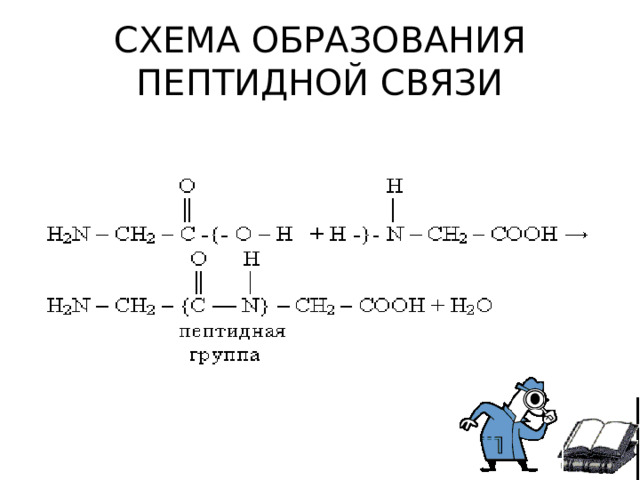
СХЕМА ОБРАЗОВАНИЯ ПЕПТИДНОЙ СВЯЗИ
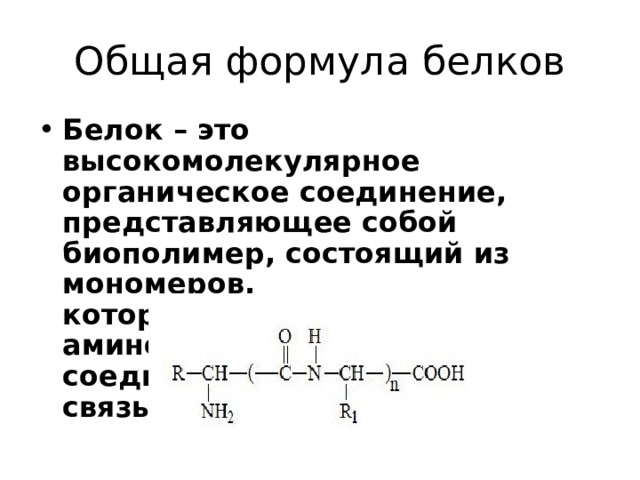
Общая формула белков
- Белок – это высокомолекулярное органическое соединение, представляющее собой биополимер, состоящий из мономеров, которыми являются аминокислоты, соединенные пептидной связью.

По физическим свойствам белки делятся на :
растворимые в воде
нерастворимые в воде

В состав белков входят 20 α - аминокислот, но их остатки могут многократно повторяться в самых различных сочетаниях, поэтому существует огромное число различных белков, каждый из которых имеет свое особенное строение и выполняет свою функцию в жизнедеятельности организма.
Молекула инсулина
Структура белков
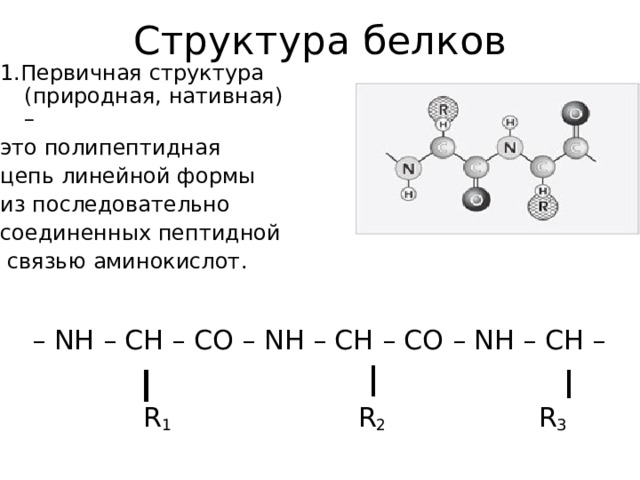
1.Первичная структура (природная, нативная) –
это полипептидная
цепь линейной формы
из последовательно
соединенных пептидной
связью аминокислот .
– NH – CH – CO – NH – CH – CO – NH – CH –
R 1 R 2 R 3
Структура белков
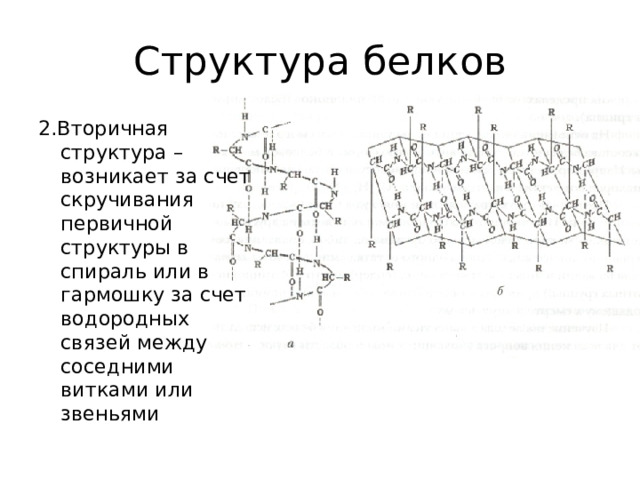
2.Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку за счет водородных связей между соседними витками или звеньями

Структура белка
3.Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот вторичной структуры
Структура белка.
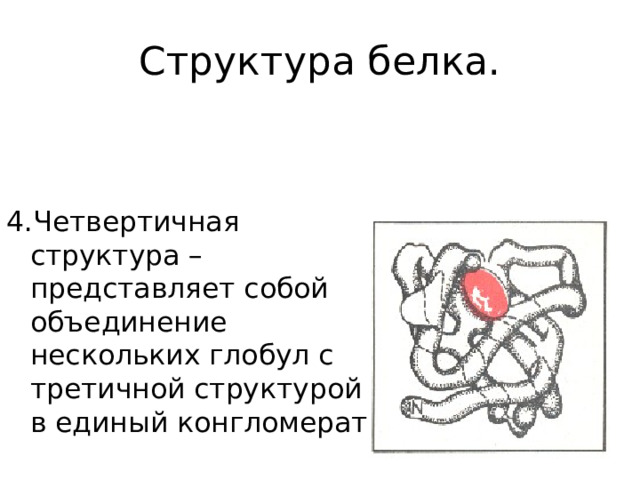
4.Четвертичная структура – представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат
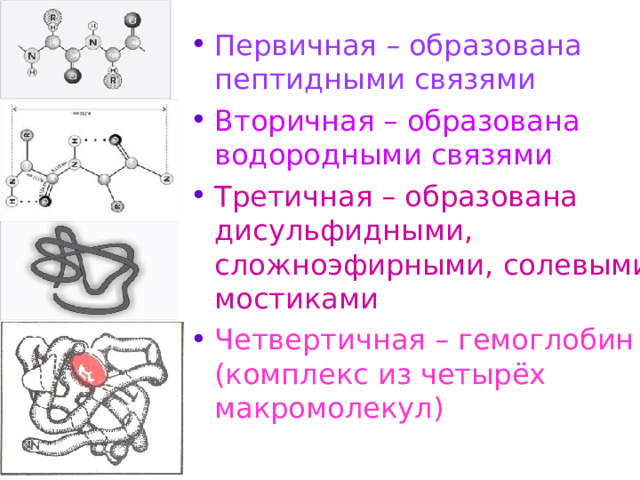
- Первичная – образована пептидными связями
- Вторичная – образована водородными связями
- Третичная – образована дисульфидными, сложноэфирными, солевыми мостиками
- Четвертичная – гемоглобин (комплекс из четырёх макромолекул)

Ксантопротеиновая реакция
В пробирку налейте 2 мл раствора белка и добавьте по каплям 0,5 мл концентрированного раствора азотной кислоты. Осторожно нагревайте пробирку и наблюдайте изменение цвета.
РАСТВОР БЕЛКА + HNO 3 ? Жёлтый цвет указывает на присутствие ароматических аминокислот
Биуретовая реакция
К 2–3 мл раствора белка в пробирке добавьте 2–3 мл 10%-го раствора гидроксида натрия. К полученной смеси прилейте 2–3 мл раствора сульфата меди(II). Пробирку встряхните и
РАСТВОР БЕЛКА + NaOH + CuSO 4 ?
Красно – фиолетовый окрас указывает на присутствие пептидной группы
РАСТВОР БЕЛКА + СН 3 СООР b + NaOH ?
Чёрный цвет указывает на присутствие серы

Лабораторная работа №19 «Исследование свойств белков как биологических полимеров»
- Опыт №1. Денатурация белков:
1.Налить в пробирку №1 раствор белка, нагреть на спиртовке до кипения.
2.Налить в пробирку №2 раствор белка и добавить 1 мл этанола.
3.Налить в пробирку №3 раствор белка и добавить 1 мл сульфата меди.
4.Налить в пробирку №4 раствор белка и добавить 1 мл нитрата свинца.
5.Налить в пробирку №5 раствор белка и добавить 1 мл формалина

Опыт№2 Биуретова ракция
- (используется в медицине для обнаружения белка в моче).
1. Налить в пробирку 1мл раствора белка, добавить 2 мл раствора щёлочи натрия и добавить 0,5 мл раствора медного купороса.
- Уравнение реакции не пишется, описываем наблюдения.

Опыт №3. Ксантопротеиновая реакция
- Налить в пробирку 2мл раствора белка, добавить 0,5 мл концентрированной азотной кислоты, нагреть на спиртовке содержимое пробирки и добавить раствор аммиака. Уравнение реакции не пишется, описываем наблюдения.

эксперимент

Вопросы для самоконтроля
- 1.Какую вы знаете общую формулу белков?
- 2.Из чего состоят белки?
- 3.Особенности структуры белков и её характеристики.
- 4.Что такое денатурация?
- 5.Какие факторы вызывают денатурацию белков?
- 6.Какие вам известны качественные реакции на белок?

Вывод: Белки обладают следующими свойствами














































