
Коррозия металлов
Учитель объявляет тему «Коррозия металлов».
(На экране появляется изображение и звучит музыкальный фрагмент).

Коррозия ( от лат. corrosio – « разъедать » ) - это самопроизвольно протекающий процесс разрушения металлов в результате взаимодействия с окружающей средой.
Конечно же , урок будет посвящен не творчеству одноимённой группы, а самопроизвольному процессу разрушения металлов под действием окружающей среды (на экране появляется определение коррозии).

«Ржа ест железо»
Коррозия металла – необратимый процесс, наносящий большой ущерб экономике.
Ежегодно вследствие коррозии в мире выбывает из фонда годного около 500 млн т проката черных металлов (около 30% годового производства металлов во всём мире)!
В результате коррозии металлы становятся менее прочными, нарушается герметичность труб и аппаратов, что может привести к утечке нефти, бензина, газа и т. д.
Вред, наносимый коррозией огромен. А чтобы победить противника, его нужно хорошо знать.

Ежегодно
1/ 4
всего произведенного
Fe
теряется из-за коррозии

Сущность коррозии
Какие окислители наиболее часто встречаются в природе?
Кислород воздуха, вода с растворёнными в ней примесями солей и кислот, хлор, оксиды серы, азота и др.
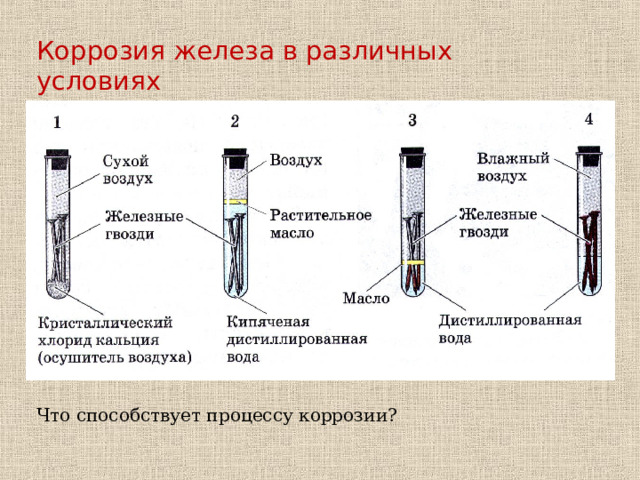
Коррозия железа в различных условиях
Электрохимической коррозии способствуют наличие влаги, кислорода, электролита (морская вода и др.), высокая температура, контакт различных по химической активности металлов.
Что способствует процессу коррозии?
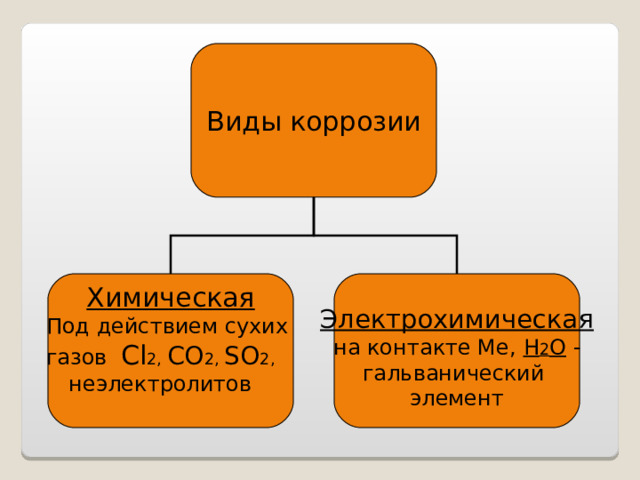
Виды коррозии
Химическая
Под действием сухих
газов С l 2, CO 2, SO 2 ,
неэлектролитов
Электрохимическая
на контакте Ме, H 2 O -
гальванический
элемент
7

Виды коррозии
Химическая (газовая коррозия) происходит в не проводящей электрический ток среде.
… или сернистым газом.

Виды коррозии
Электрохимическая происходит в токопроводящей среде (в электролите).
Следующий вид коррозии – электрохимическая. Как видно из определения, этот вид коррозии происходит в электролитах.

1813 г.
Гемфри Деви
открыл
электрохимическую
коррозию металлов

Электрохимическая коррозия железа
Fe + O 2 + H 2 O Fe(OH) 3
Составить электронный баланс,указать окислитель и восстановитель, расставить коэффициенты

Проверка
Электрохимическая коррозия железа
4 Fe + 3 O 2 + 6 H 2 O 4 Fe(OH) 3
Fe 0 - 3 е → Fe +3 4 - восстановитель
O 2 0 +4 е →2O -2 3 - окислитель

Механизм коррозии
Посмотрите на видео процесс разрушения чистого образца цинка по д действием соляной кислоты.
Что произойдёт, если к реагирующему цинку прикоснуться медной проволокой?
Растворение цинка в соляной кислоте
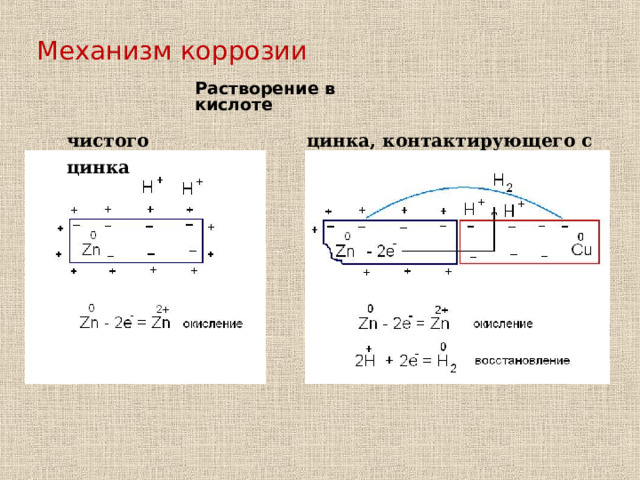
Механизм коррозии
Растворение в кислоте
чистого цинка
цинка, контактирующего с медью
… а затем объясняет тот же процесс, но при контакте цинка с медью.

Контакт железа с менее активным металлом (медью)
Вывод: при контакте железа в токопроводящей среде с менее активными металлами происходит разрушение более активного металла, т. е. железа.

- Коррозия протекающая в токопроводящей среде. Помимо химической реакции, в системе возникает электрический ток. Процесс электрохимической коррозии происходит при контакте двух металлов Разрушается металл с более сильными восстановительными свойствами (выполняет роль анода)

Коррозия на контакте двух металлов
2+
Fe - 2 ē Fe
разрушение
на меди:
+
2Н + 2 ē H 2
2+
Zn - 2 ē Zn
разрушение
на железе:
+
2Н + 2 ē H 2

Уже полтора тысячелетия стоит на одной из площадей Дели железная колонна высотой около 8 метров, диаметром 65 сантиметров, массой 6,5 тонн. И, несмотря на жаркий и влажный климат Индии, не ней нет ни единого ржавого пятнышка.
На экране появляется новая информация и изображение Делийской колонны.

Это объясняется тем, что колонна сделана из чистого железа. А чистое железо не ржавеет.
Сейчас лишь немногие крупнейшие металлургические лаборатории мира могут получить граммы железа такой чистоты.
Как это удалось древним индийским металлургам?!

Знать особенности металлов особенно важно тогда, когда строятся транспортные средства или сложные объекты, от прочности и надёжности которых будут зависеть человеческие жизни.
В начале ХХ века из нью-йоркского порта вышла в открытый океан красавица яхта. Её владелец, американский миллионер, не пожалел денег, чтобы удивить свет: корпус яхты был сделан из очень дорогого в то время алюминия, листы которого скреплялись медными заклёпками. Это было так красиво: сверкающий серебристым блеском корабль, усеянный золотистыми головками заклёпок!

Однако недолго наслаждался владелец новой яхты. Через несколько дней, когда в океане поднялось лёгкое волнение, обшивка корпуса вдруг начала расходиться, и яхта быстро пошла ко дну. Команда едва успела спустить на воду шлюпки, которые… тоже были из алюминия с медью. К счастью, незадачливых мореплавателей подобрало проходившее мимо судно.

Защита от коррозии
- Изоляция металла от окружающей среды нанесением покрытий:
- – неметаллических (покрытие лаками, красками, эмалями);
- – химических (оксидные, фосфатные, нитридные и т. д.) ;
- – металлических покрытий (катодное и анодное покрытие).

Легирование металлов – получение сплавов, которые устойчивы к коррозии (например, нержавеющей стали, содержащей до 18% хрома и до 10% никеля).
Нержавеющая сталь
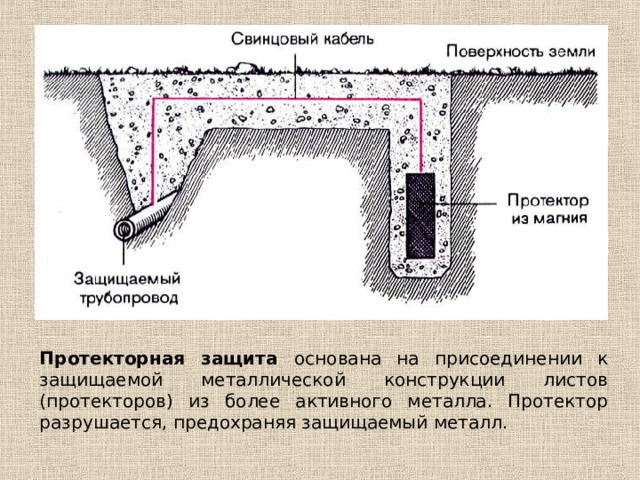
Особый интерес представляет протекторная защита. На чем основано её действие? Каков её недостаток?
Протекторная защита основана на присоединении к защищаемой металлической конструкции листов (протекторов) из более активного металла. Протектор разрушается, предохраняя защищаемый металл.
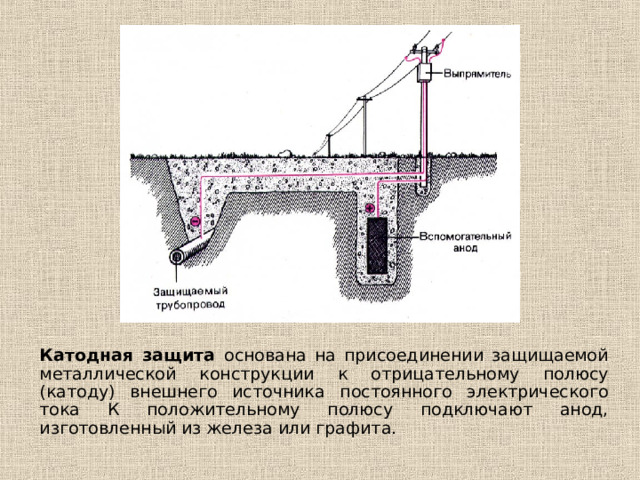
На чем основана катодная защита?
Катодная защита основана на присоединении защищаемой металлической конструкции к отрицательному полюсу (катоду) внешнего источника постоянного электрического тока К положительному полюсу подключают анод, изготовленный из железа или графита.

Защита металлов от коррозии
- Изменение свойств агрессивной среды:
- – удаление из неё веществ, которые усиливают коррозию (например, кислород можно удалить кипячением);
- – добавление веществ, которые замедляют коррозию, – ингибиторов .
Наиболее распространен метод изоляции от окружающей среды нанесение м на поверхность металла защитных пленок из неметаллов, химическими методами и др.

Домашнее задание
- § 13, в. 2
- В тетрадь выписать из презентации химические реакции, протекающие при химической и электрохимической коррозии. Составьте электронный баланс для реакций,



















































