Контрольная работа №1: “Углеводороды”
Задания к контрольной работе:
Для вопросов 1-7 выберите вариант ответа (верный - только один ответ из четырех). Каждый правильный ответ: 1 балл, максимально 7 баллов.
Для вопросов 5-7 объясните выбор ответа, записав или уравнение реакции; или определение. Назовите вещества по систематической номенклатуре или составьте их структурную формулу. Каждый правильный дополнительный ответ: 1 балл, максимально 3 балла.
Решите задачу 8, запишите ход решения. Оценивается каждый элемент решения, максимально: 3 балла.
12-13 баллов – оценка “5”, 10-11 баллов – оценка “4”, 7-9 баллов – оценка “3”, менее 7 баллов – оценка “2”.
Вариант 1
1 Общей формуле алкенов соответствует:
а) СnH2n
б) (СH3)n
в) СnH2n -2
г) СnH2n+2
2 Молекулы алкадиенов содержат:
а) только  связи
связи
б) одну 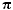 связь
связь
в) две 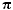 связи
связи
г) бензольное кольцо
3 Ацетилен:
а) летучая жидкость, применяется при сварке металлов
б) вязкая жидкость, применяется для получения резины
в) взрывоопасный газ, применяется при сварке металлов
г) газ, применяется для получения резины
4 Вещество, формула которого
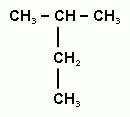
называется:
а) 3-метилбутан
б) 2-метилбутан
в) 2-этилпропан
г) пентан
5 Изомером циклобутана является:
а) бутен
б) бутин
в) бутан
г) бутанол
С, 450-500°С
6 В схеме превращений 3 С2Н2 ----------- Х неизвестным веществом Х является:
а) пропан
б) гексан
в) циклогексан
г) бензол
7 Сумма коэффициентов в реакции горения этана равна:
а) 4
б) 16
в) 19
г) 21
8 Массовая доля углерода в углеводороде составляет 81,82%, относительная плотность паров этого вещества по кислороду равна 1,375. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу.
Ответы и критерии оценивания к Варианту 1
1 Ответы на вопросы с выбором ответа:
| № вопроса | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Ответ | а | в | в | б | а | г | в |
| Балл | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
2 Ответы на дополнительный вопрос (для вопросов 5-7):
| № вопроса | Содержание возможного ответа | Балл |
| 5 | Структурная формула циклобутана или бутена 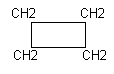 СН2=СН–СН2–СН3 СН2=СН–СН2–СН3
| 1 |
| 6 | Структурная формула бензола: 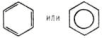
| 1 |
| 7 | Уравнение реакции горения этана: 2С2Н6 +7О2 - 4СО2 +6Н2О | 1 |
3 Решение задачи:
| Содержание верного ответа и указания по оцениванию (возможен другой тип решения) | Баллы |
| Элементы ответа Рассчитана относительная молекулярная масса вещества: Мr(вещесва)= 1,375х32=44 Рассчитано молярное соотношение атомов и выведена молекулярная формула: 44х0,8182/12 : 44х0,1818/1 = 3 : 8 Молекулярная формула С3Н8 Дано название составлена структурная формула вещества: Пропан, СН3–СН2–СН3 | |
| Ответ правильный и полный, включает все вышеназванные элементы | 3 |
| Правильно записаны первый и второй элементы ответов | 2 |
| Правильно записан только первый элемент ответа | 1 |
| Все элементы ответа записаны неверно (в первом элементе допущена ошибка, повлекшая за собой неправильное решение) | 0 |
Максимальное число баллов: 7+3+3=13 баллов.
Вариант 2
1 Общей формуле алканов соответствует:
а) СnH2n+2
б) СnH2n
в) С6H6
г) СnH2n+1
2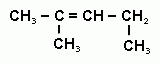 Вещество, формула которого
Вещество, формула которого
называется:
а) гексен
б) 4 - метилпентен-3
в) 2 -метилпентен-2
г) 2,2-диметилбутен -3
3 Для алкинов не характерны реакции
а) горения
б) замещения
в) присоединения
г) гидрирования
4 Природный каучук – это изомер:
а) дивинила
б) изопрена
в) бутадиена-1,3
г) хлоропрена
5 При гидратации вещества бутен-1 образуется:
а) бутанол 1
б) бутанол-2
в) бутан
г) бутин и водород
6 Гомологом этилена является:
а) бензол
б) бутен
в) бутадиен
г) бутанол
7 В схеме превращений С2Н4 +Сl2→ Х неизвестным веществом Х является:
а) хлорэтан
б) дихлорэтан
в) хлорпропан
г) дихлорметан
8 Массовая доля углерода в углеводороде составляет 85,7%, относительная плотность паров этого вещества по водороду равна 42. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу.
Вариант 3
1 Вещество, формула которого С4H6 относится к классу:
а) алкены
б) алканы
в) циклоалканы
г) алкины
2 Бензол:
а) бесцветный, легко сжижающийся газ
б) бесцветная жидкость, нерастворим в воде, ядовит
в) жидкость, растворим в воде, с неприятным запахом
г) желто-зеленый газ, ядовит
3 Вещество, формула которого
Вещество, формула которого
называется:
а) гексан
б) 3- метилпентен-3
в) 2-метилпентан
г) 2-этилбутен 2
катализатор
4 Реакция СH2=СH2 → [-СH2-СH2-]n относится к типу:
а) замещения
б) пиролиза
в) полимеризации
г) обмена
5 При дегидрировании этана образуется:
а) этанол
б) этилен
в) этановая кислота
г) этандиол
6 Сумма коэффициентов в реакции горения ацетилена равна:
а) 3
б) 10
в) 13
г) 20
7 Число изомеров вещества бутан:
а) 1
б) 2
в) 3
г) 4
8 Массовая доля водорода в углеводороде составляет 20,0%, относительная плотность паров этого вещества по воздуху равна 1,034. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу
Вариант 4
1 Вещество, формула которого СН2=СН –СН =СН2 называется
а) дивинил
б) бутин
в) бензол
г) ацетилен
2 Общей формуле алкинов соответствует:
а) СnH2n
б) (СH3)n
в) СnH2n–2
г) СnH2n+2
3 Вещество, формула которого СН3– СН2–СН3 является гомологом:
а) С3H8
б) С4H8
в) С4H10
г) С4H6
4 Этилен:
а) жидкость, нерастворим в воде
б) жидкость, растворим в воде
в) газ, нерастворим в воде
г) газ, растворим в воде
t°С
5 В схеме превращений С3Н6 +Н2О → Х неизвестным веществом Х является:
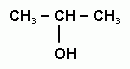
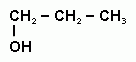

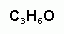
а) ; б) ; в) ; г)
6 Бензол нельзя получить:
а) дегидрированием циклоалканов
б) дегидрированием алканов
в) полимеризацией этилена
г) тримеризацией ацетилена
7 Сумма коэффициентов в реакции горения циклобутана равна:
а) 13
б) 14
в) 15
г) 16
8 Массовая доля углерода в углеводороде 92,3%. Относительная плотность паров этого вещества по водороду равна 39. Найти молекулярную формулу углеводорода. Написать его название и структурную формулу.
Вариант 5
1 Общая формула алкадиенов:
а) СnH2n+2
б) (СH3)n
в) СnH2n-2
г) СnH2n

2 Вещество, формула которого
называется:
а) 3-метилгексен-3
б) 3-этилгексан
в) 3-этилгексен-3
г) 1,2-диэтилбутен-2
3 Обязательное условие реакции хлорирования алканов:
а) газообразное агрегатное состояние продуктов реакции
б) свет
в) низкая температура
г) жидкое агрегатное состояние продуктов реакции
4 Метан:
а) бесцветный газ, без запаха;
б) бесцветная жидкость, с резким запахом;
в) бесцветная жидкость, без запаха
г) бесцветный газ, с резким запахом.
5 Изомером бутадиена является:
а) бутен
б) бутин
в) бутан
г) циклобутан
t°С, Н2SO4
6 В схеме превращений С2Н5ОН - ---→ Х +Y
неизвестными веществами Х и Y являются:
а) этилен и вода
б) этен и водород
в) углекислый газ и вода
г) ацетилен и водород
7 При гидратации ацетилена (в присутствии HdSO4 - реакция Кучерова) образуется
а) этанол
б) этандиол
в) уксусный альдегид
г) уксусная кислота
8 Массовая доля углерода в углеводороде 82,75%. Относительная плотность паров этого вещества по воздуху равна 2. Найти молекулярную формулу углеводорода. Написать его название и структурную формулу.
Вариант 6
1 Вещество, формула которого С4H8 относится к классу:
а) алкены
б) алканы
в) алкадиены
г) алкины
2 Молекулы алкинов содержат:
а) только одинарные связи
б) одну двойную связь
в) две двойные связи
г) одну тройную связь

3 Вещество, формула которого
называется:
а) 3,3-диметилбутан
б) 2,2-диметилбутан
в) 2-этилбутан
г) 2-метил-2-этилпропан
4 Дивинил:
а) бесцветный, легко сжижающийся газ
б) бесцветная жидкость
в) огнеопасная жидкость, с неприятным запахом
г) желто-зеленый газ, ядовит
5 При гидрировании бензола получают
а) циклогексан
б) гексан
в) гексен
г) гексин
6 Число всех изомеров вещества бутен
а) 3
б) 4
в) 5
г) 6
t°С, катализатор
7 В схеме превращений С2Н4 +Н2О → Х
неизвестным веществом Х является
а) этанол
б) этен
в) этилен
г) этан
8 Массовая доля углерода в углеводороде составляет 83,3%, относительная плотность паров этого вещества по водороду равна 36. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу.
Ответы к заданиям 1-8: Варианты 2-6
|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Вариант 2 | а | в | в | б | б | б | б | С6Н12 |
| Вариант 3 | г | б | б | в | б | в | б | С2Н6 |
| Вариант 4 | а | в | в | в | а | в | в | С6Н6 |
| Вариант 5 | в | в | б | а | б | а | в | С4Н10 |
| Вариант 6 | а | г | б | а | а | в | а | С5Н12 |
КАРБОНОВЫЕ КИСЛОТЫ. СЛОЖНЫЕ ЭФИРЫ. ЖИРЫ.
1 ВАРИАНТ.
1. Соотнесите термины, используемые для классификации кислот:
Признак классификации: 1) число карбоксильных групп
2) природа углеродного скелета
Тип кислоты: а) предельная, б) одноосновная, в) ароматическая, г) непредельная, д) двухосновная
2. Формула стеариновой кислоты
а) С15Н31СООН б) С16Н33СООН в) С17Н35СООН г)С17Н33СООН
3. Название кислоты с формулой СН3-СН-СН2-СООН:
СН3
а) 3-метилбутановая б) 2-метилбутановая в) 3-метилбутеновая г) 3,3-диметилпропановая
4. Соотнесите названия и формулы:
Тривиальное название: систематическое название: формула:
I) уксусная 1) пропеновая а) СН2=СН-СООН
II) муравьиная 2) гексановая б) НООС-СООН
III) масляная 3) этановая в) СН3-СН2-СН2-СН2-СН2 -СООН
IV) акриловая 4) этандиовая г) СН3-СН2-СН2-СООН
V) щавелевая 5) метановая д) СН3-СООН
VI) капроновая 6) бутановая е) НСООН
5. Какие признаки, верно, отражают физические свойства уксусной кислоты: 1) при комнатной температуре бесцветная жидкость, 2) газообразное вещество, 3) не имеет запаха, 4) имеет характерный запах, 5) плохо растворима в воде, 6) неограниченно растворима в воде, 7) слабый электролит, 8) сильный электролит?
а) 1,4,6,7 б) 2,4,5,6,7 в) 1,3,6,8 г) 1,4,5,7
6. Относительная молекулярная масса предельной одноосновной карбоновой кислоты равна 256. число атомов углерода в этой кислоте равно:
а) 15 б) 16 в) 17 г) 18
Назовите эту кислоту.
7. Какой из металлов реагирует с уксусной кислотой с максимальной скоростью?
а) железо б) олово в) цинк г) кальций
Напишите уравнение реакции.
8. Суммы коэффициентов в молекулярном, полном и сокращенном ионных уравнениях реакции муравьиной кислоты с карбонатом натрия соответственно равны:
а) 7,11,7 б) 7,13,7 в) 5,9,5 г) 7,11,5
9. Взаимодействие пропионовой кислоты с этиловым спиртом называется реакцией:
а) гидратации б) этерификации в) гидрирования г) нейтрализации
Напишите уравнение реакции
10. Дана цепочка превращений
СН3-СН2-С …1 …2 …3 …4
Укажите формулы веществ 1 – 4: а) СН3-СН2-СООК б) СН3-СН2-СООН в) СН3-СН2-СООСН3
Напишите уравнения реакций.
11. Укажите формулу сложного эфира:
а) СН3-О-СН2-СН3 б) СН3-СН2-С – ОН в) СН3-С – СН3 г) СН3-СН2-С –О – С2Н5
12. Соотнесите: вещество: 1) сложный эфир 2) воск 3) жир 4) мыло
Формула: а) СН2-О-СО-С17Н35 б) С15Н31СООС18Н37 в) С17Н35СООNa г) СН3СООСН3
СН –О-СО-С17Н35
СН2-О-СО-С17Н35
13. Соотнесите:
исходные вещества:
1) С17Н33СООН + Н2 3) СН2-О-СО-С17Н35
2) СН3-СН2 –СООН + СН3-ОН СН –О-СО-С17Н35 + 3NaОН
4) СН3 СООС4Н9 + Н2О СН2-О-СО-С17Н35
название реакции: а) омыление б) гидролиз в) этерификации г) гидрирование
14. В состав природных жиров не входит кислота:
а) щавелевая б) стеариновая в) масляная г) олеиновая
15. С какими из перечисленных веществ в соответствующих условиях реагирует уксусная кислота: 1) медь, 2) оксид кальция, 3) оксид серы (IV), 4) метанол, 5) хлор, 6) этаналь, 7) фенолятнатрия?
а) 2,4,5,7 б) 1,2,5,6 в) 2,3,4,5 г) 4,5,6
Напишите уравнения реакций.
КАРБОНОВЫЕ КИСЛОТЫ. СЛОЖНЫЕ ЭФИРЫ. ЖИРЫ.
2 ВАРИАНТ.
1. Соотнесите:
Тип кислоты: формула:
1) предельная а) СН3-СН=СН-СООН б)
2) непредельная
3) ароматическая в) СН3-СН2-СН2-СООН
2. Пальмитиновая кислота имеет формулу:
а) С15Н31СООН б) С16Н33СООН в) С17Н35СООН г) С17Н33СООН
3. Назовите кислоту формула которой СН3-СН2-ССl2-СООН :
а) 2-дихлорбутановая б) 2,2-дихлорбутановая в) 1,1- дихлорпропановая г) 3-дихлорбутановая
4. Соотнесите названия и формулы:
Тривиальное название: систематическое название: формула:
I) муравьиная 1) пропановая а) НООС-СН2 –СН2 – СООН
II) пропионовая 2) этановая б) СН3-СН2-СН2-СН2-СООН
III) янтарная 3) метановая в) СН3-СООН
IV) валериановая 4) бутандиовая г) НСООН
V) уксусная 5) гексановая д) СН3-СН2 -СООН
VI) капроновая 6) пентановая е) СН3-СН2-СН2-СН2-СН2 –СООН
5. Относительная молекулярная масса предельной одноосновной карбоновой кислоты равна 284. число атомов углерода в этой кислоте равно:
а) 15 б) 16 в) 17 г) 18
Назовите эту кислоту.
6. С каким из веществ муравьиная кислота вступает в реакцию замещения:
а) Mg б) CaO в) Ba(OH)2 г) Na2SiO3
Напишите уравнение реакции.
7. Суммы коэффициентов в молекулярном, полном и сокращенном ионных уравнениях реакции уксусной кислоты с гидроксидом меди (II) соответственно равны:
а) 6,8,8 б) 4,10,4 в) 6,9,7 г) 6,8,4
8. Реакцией этерификации называется взаимодействие кислоты:
а) со щелочью б) со спиртом в) с галогенами г) с металлами
9. Дана цепочка превращений: НС СН …1 …2 …3 …4
Укажите формулы веществ 1 – 4:
а) СН3-СООН б) СН2Cl-СООН в) СН3-С г) СН2С1-СООNa
10. Какие признаки, верно, отражают физические свойства уксусной кислоты: 1) при комнатной температуре бесцветная жидкость, 2) газообразное вещество, 3) не имеет запаха, 4) имеет характерный запах, 5) плохо растворима в воде, 6) неограниченно растворима в воде, 7) слабый электролит, 8) сильный электролит?
а) 1,4,6,7 б) 2,4,5,6,7 в) 1,3,6,8 г) 1,4,5,7
11. С какими из перечисленных веществ в соответствующих условиях реагирует уксусная кислота: 1) медь, 2) оксид кальция, 3) оксид серы (IV), 4) метанол, 5) хлор, 6) этаналь, 7) фенолятнатрия?
а) 2,4,5,7 б) 1,2,5,6 в) 2,3,4,5 г) 4,5,6
Напишите уравнения реакций.
12. Укажите формулу сложного эфира:
а) СН3-СООН б) СН3- СН2-С – СН3 в) Н-С –О – С3Н7 г) СН3-СН2-О-СН3
13.Соотнесите: группа веществ: 1) воски 2) жиры 3) мыла 4) сложные эфиры
Природа веществ:
а) сложные эфиры глицерина и высших карбоновых кислот
б) сложные эфиры высших карбоновых кислот и высших спиртов
в) натриевые и калиевые соли высших карбоновых кислот
г) производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал.
14. Соотнесите:
исходные вещества: название реакции:
СН3-СН2-СООСН3 + Н2О а) омыление
СН2-О-СО-С17Н35 б) гидрирование
СН –О-СО-С17Н35 + 3КОН в) этерификации
СН2-О-СО-С17Н35 г) гидролиз
СН2-О-СО-С17Н33
СН –О-СО-С17Н33 + 3Н2
СН2-О-СО-С17Н33
4) СН3-СООН + С2Н5ОН
Напишите уравнения реакций.
15. Какое из веществ выпадает из общего ряда?
а) триолеат глицерина б) тринитрат глицерина в) тристеарат глицерина г) трипальмитат глицерина
Часть 1
При выполнении заданий этой части в бланке ответов № 1 под номером выполняемого вами задания (А1–А30) поставьте знак « × » в клеточку, номер которой соответствует номеру выбранного вами ответа.
А1. Молекулярная формула клетчатки
1. С6Н12О6
2. (С5Н8О4)n
3. (С5Н10О5)n
4. (С6Н10О5)n
А2. Какой связью соединены остатки двух моносахаридов в молекуле дисахарида
1. Пептидной
2. Гликозидной
3. Водородной
4. Макроэргической
А3. Для моносахаридов характерны свойства
1. Хорошая растворимость в воде
2. Высокие температуры плавления
3. Сладкий вкус
4. Все верно
5. Все неверно
А4. К восстанавливающим дисахаридам не относится
1. Сахароза
2. Мальтоза
3. Целлюлоза
4. Лактоза
А5. Заболевание сахарным диабетом вызвано повышением содержанием в крови
1. Сахарозы
2. Рибозы
3. Глюкозы
4. Фруктозы
А6. Чем можно отличить глюкозу от фруктозы
1. Хлоридом железа (III)
2. Раскаленной медной проволокой
3. Бромной водой
4. Реакцией серебряного зеркала
А7. Из указанных углеводов не окисляется аммиачным раствором оксида серебра
1. Глюкоза
2. Мальтоза
3. Лактоза
4. Сахароза
Часть 2
Ответом к заданиям этой части (В1–В2) является набор цифр или число, которые следует записать в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждую цифру и запятую в записи десятичной дроби пишите в отдельной клеточке в соответствии с приведенными в бланке образцами.
В заданиях В2 на установление соответствия запишите в таблицу цифры выбранных вами ответов под соответствующими буквами, а затем получившуюся последовательность цифр перенесите в бланк ответов № 1 без пробелов и других символов. (Цифры в ответе могут повторяться.)
В1. Вещества Х в схемах превращений соответственно являются
| А. С6Н12О6 дрожжи Х + СО2 Б. С6Н12О6 + Н2 Ni Х
В. (С6Н10О5)n + 3n НNO3 H2SO4 3nН2O + H2SO4
Г. С6Н12О6 ферменты Х + СО2 + Н2
| 1. Мальтоза 2. Триацетат целлюлоза 3. Масляная кислота 4. Тринитрат целлюлозы 5. Сорбит 6. Этиловый спирт |
В2. Соотнесите реакцию и ее характерный признак.
1. Сахароза + Cu(OH)2 А. Фиолетовое окрашивание крахмала
2. Крахмал + I2 Б. Блестящий налет на стенках
3. Глюкоза [Ag(NH3)2]OH(t°) В. Комплексное соединение синего цвета
Не забудьте перенести все ответы в бланк ответов № 1.
Часть 3
Для записи ответов к заданиям этой части (С1) используйте бланк ответов № 2. Запишите сначала номер задания (С1), а затем полное решение. Ответы записывайте четко и разборчиво.
С1. Найдите массу футболки из триацетатного волокна, образовавшегося из 243г целлюлозы.
Инструкция по проверке и оценке работ учащихся по химии
ЧАСТЬ 1
Задание с выбором ответа считается выполненным верно, если учащийся указал код правильного ответа. Во всех остальных случаях (выбран другой ответ; выбрано два или больше ответов, среди которых может быть и правильный; ответ на вопрос отсутствует) задание считается невыполненным.
ЧАСТЬ 2
Задание с кратким свободным ответом считается выполненным верно, если правильно указана последовательность цифр (число).
За полный правильный ответ на задания В1 – В2 ставится 2 балла, за правильный неполный – 1 балл, за неверный ответ (или при его отсутствии) – 0 баллов.
ЧАСТЬ 3
КРИТЕРИИ ПРОВЕРКИ И ОЦЕНКИ ВЫПОЛНЕНИЯ
ЗАДАНИЙ С РАЗВЁРНУТЫМ ОТВЕТОМ
C1
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
| Элементы ответа: Написаны уравнения реакций, соответствующие схеме превращений: 243г Хг (С6Н10О5)n + 3n(CН3CО)2 → (С6Н7О5(CН3CО)3)n + 3nCН3CОOH 162г 288г
1. Найдём относительную молярную массу структурного звена молекулы целлюлозы Мr(C6H10O5)=6*12+10*1+5*16=162 г/моль 2. Найдём относительную молярную массу структурного звена молекулы триацетата целлюлозы Мr(С6Н7О5(CН3CО)3)=6*12+7*1+5*16+3*(12+3+12+16)=159+3*43= =159+129=288 г/моль 3. Через пропорцию найдем массу триацетатного волокна, образовавшегося из 243г целлюлозы 243г – Хг 162г – 288г Следовательно, Х=(243*288)/162=432(г)
Ответ: 432 грамма. |
| Ответ правильный и полный, включает все названные выше элементы | 4 |
| Правильно выполнено и рассчитано действие 3 | 3 |
| Правильно выполнены и рассчитаны действия 1 и 2 | 2 |
| Правильно написано уравнение реакции | 1 |
| Все элементы ответа записаны неверно | 0 |
Перевод баллов в пятибалльную шкалу
| Процент верно выполненных заданий | Кол-во набранных баллов | Отметка по пятибалльной системе |
| Менее 50% | 0-7 | Неудовлетворительно |
| 50-69% | 8-10 | Удовлетворительно |
Вариант №1
1. Общая формула циклоалканов:
а) СnH2n;
б) СnH2n+2;
в) СnH2n-6.
2. Тип гибридизации атома углерода в алкенах:
а) sp3;
б) sp;
в) sp2.
3. Длина связи (C=C) в углеводородах:
а) 0,154нм;
б) 0,14нм;
в) 0,134нм.
4. Выбрать изомер для вещества, имеющего строение: CH2=CH-CH2-CH=CH2:
а) CH2=C=CH-CH2-CH3;
б) 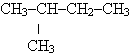 ;
;
в) CH2=CH-CH2-CH2-CH=CH2.
5. Валентный угол при sp2 гибридизации:
а) 180°;
б) 120°;
в) 109°29'.
6. Назовите по международной номенклатуре: 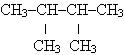 :
:
а) 2,4-диметилбутан;
б) диметилпентан;
в) гексан.
7. Выберите название вещества, из которого получают ацетилен в лаборатории:
а) этан;
б) карбонат кальция;
в) карбид кальция.
8. Углеводород имеет состав: С-92,3%, H-7,7%. Плотность его пара по воздуху равна 2,69. Определите молекулярную формулу вещества.
а) С8H18;
б) С3H4;
в) С6H6.
9. Обесцвечивает раствор KMnO4:
а) пропан;
б) этан;
в) циклобутан.
10. Структурное звено в макромолекуле полиэтилена:
а) СH2=СH2;
б) -СH2-;
в) -СH2-СH2-.
11. Бромбензол образуется в результате реакции замещения взаимодействием:
а) бензола с бромом;
б) бензола с бромоводородом;
в) бензола с бромидом калия.
12. Веществами x и y в схеме превращений 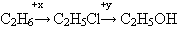 являются:
являются:
а) x-Cl2, y-H2O;
б) x-HCl, y-KOH;
в) x-Cl2, y-KOH.
13. Целью крекинга нефтепродуктов является получение:
а) бензола;
б) бензина;
в) парафинов.
14. Пространственное строение молекулы ацетилена:
а) линейное;
б) плоскостное;
в) тетраэдрическое.
15. Из 7,8г бензола получено 8,61г нитробензола. Выход продукта реакции составил:
а) 70%;
б) 65%;
в) 80%.
Вариант №2
Общая формула алкенов:
а) СnH2n; б) СnH2n+2; в) СnH2n-2.
Какая гибридизация не существует:
а) sp³; б) sp4; в) sp².
Длина связи (C≡C) в углеводородах:
а) 0,12нм; б) 0,14нм; в) 0,134нм.
CH3
׀
Для вещества, формула которого: CH3–CH–CH2–CH3, гомологом является:
а) CH3–CH2–CH2– CH2–CH3; в) CH3–CH–CH–CH3
б) CH3–CH–CH3; ׀ ׀
׀ CH3 CH3
CH3
Валентный угол при sp³ гибридизации:
а) 180°; б) 120°; в) 109°29'. CH3 CH3
׀ ׀
6. Назовите по международной номенклатуре: CH3–C=C–CH2–CH3:
а) гептен; б) 2,3–диметилпентен–2; в) 3,4–диметилпентен–3.
Реакция гидратации возможна для:
а) бутана; б) бутена; в) бензола.
Массовая доля углерода в углеводороде 80%, а плотность его по водороду 15. Найти молекулярную формулу.
а) С2H6; б) С3H4; в) С6H4.
9. Наиболее коптящим пламенем горит:
а) этилен; б) этан; в) ацителен.
10. Природный каучук по хим. строению представляет собой:
а) полибутадиен; б) транс-полиизопрен; в) цис-полиизопрен.
11. Не имеет изомеров:
а) циклобутан; б) гексен; в) пропан.
-x +y
12. Веществами x и y в схеме превращений С6H12→ С6H6→ С6H5NO2 являются:
а) x–H2, y–HNO3; б) x– H2, y– NO2; в) x– H2, y– NH3.
13. Перегонка нефти осуществляется для получения:
а) метана и бензола; б) аренов; в) различных нефтепродуктов.
14. При соединении пропилена с хлороводородом получают:
а) 1–хлорпропан; б) 2–хлорпропан; в) 1,2–дихлорпропан.
15. Для получения 22,4л ацетилена (н.у.) потребуется карбид кальция массой:
а) 32г; б) 96г; в) 64г.
Вариант l
Часть А
1. Фенол не реагирует с
FeCl3
HNO3
NaOH
HCl
2. При окислении метанола оксидом меди (ll) образуется
метан
уксусная кислота
метаналь
хлорметан
3. Свежеприготовленный осадок Cu(OH)2 растворится, если к нему добавить
глицерин
этанол
пропен
пропанол-2
4. При окислении пропанола-1 образуется
пропилен
пропанон
пропаналь
пропан
5. Фенол проявляет более слабые кислотные свойства по сравнению с
тринитрофенолом
водой
метанолом
этанолом
6. Верны ли следующие суждения?
А. Из-за действия межмолекулярных водороднх связей в гомологическом ряду спиртов (при н. у.) отсутствуют газообразные представители.
Б. Винный спирт – так называемый этанол.
верно только А
верно только Б
верны оба суждения
оба суждения неверны
7. Метиловый спирт, в отличие от этилового,
взаимодействует с натрием
не образует при дегидратации алкена
не образует при дегидратации простого эфира
окисляется подкисленным раствором KMnO4
Часть В
Запишите цифры в порядке возрастания
8. Метаналь может реагировать с
N2
Ag[(NH3)2]OH
C6H5OH
C6H5CH3
Na
H2
9. И этиленгликоль и метанол будут реагировать с
натрием
хлороводородом
гидроксидом алюминия
водородом
кислородом
гидроксидом меди (II)
Часть С
10. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
этан → этен → бромэтан → этанол → бромэтан
11. Рассчитайте массу фенола, которая может быть получена гидролизом бромбензола массой 628г, если массовая доля выхода продукта реакции равна 50%.
Поделиться…
Вариант ll
Часть А
Характерной реакцией для многоатомных спиртов является взаимодействие с
1)Ag2O(NH3 p-p) 2) Cu 3) Br2 4) Cu(OH)2
И с азотной кислотой, и с гидроксидом меди (ll) будет взаимодействовать
фенол 3) этанол
глицерин 4) метан
Фенол взаимодействует с
соляной кислотой 3) этиленом
гидроксидом натрия 4) метаном
Пропанол можно получить из пропена в результате реакции
гидратации 3) галогенирования
гидрирования 4) гидрогалогенирования
Глицерин, в отличие от пропанола, легкко растворяет
оксид железа (II) 3) гидроксид алюминия (III)
оксид алюминия (III) 4) гидроксид меди (II)
Верны ли следующие суждения?
А. Метиловый спирт – это яд, приводящий к слепоте и смерти.
Б. Этиловый спирт – это бесцветная жидкость с характерным запахом, не растворимая в воде.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
7.Метанол, в отличие от этанола, не может быть получен
1) щелочным гидролизом галогеналканов
2) гидролизом сложных эфиров
3) гидратацией алкенов
4) гидролизом алкоголятов
Часть В
Запишите цифры в порядке возрастания.
Фенол реагирует с
кислородом 4) хлороводородом
бензолом 5) натрием
гидроксидом натрия 6) оксидом кремния (IV)
Для метанола справедливы утверждения:
1) газообразен при обычных условиях
2) хорошо растворяется в воде
3) взаимодействует с аммиачным раствором оксида серебра
4) атом углерода находится в sp3 –гибридизации
5) синтезируют из водяного пара
6) в водном растворе проявляет сильные кислотные свойства
Часть С
Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
этен → хлорэтан → этанол → зтилат натрия → этанол
Рассчитайте массу фенолята натрия, которая может быть получена при взаимодействии 55 г фенола с 12 г гидроксида натрия.
Вариант lll
Часть А
Кислотные свойства наиболее выражены у
1)фенола 3) этанола
2) метанола 4) глицерина
2.Бутанол-2 и хлорид калия образуются при взаимодействии
1)1-хлорбутана и водного раствора КОН
2) 2-хлорбутана и спиртового раствора КОН
3) 1-хлорбутана и спиртового раствора КОН
4) 2-хлорбутана и водного раствора КОН
3.Глицерин в водном растворе можно определить с помощью
1)бромной воды 3) гидроксида меди (ll)
2) нитрата серебра 4) гидроксида натрия
4.При окислении этанола оксидом меди (ll) образуется
1)этан 3) этаналь
2) уксусная кислота 4) хлорэтан
5.Каждый из атомов кислорода в молекуле глицерина образует
1)одну σ-связь3) две σ-связи
2) одну π-связь 4)одну σ-связьи одну π-связь
6.Верны ли следующие суждения?
А. Предельным одноатомным спиртам, начиная с этанола, изомерны простые эфиры
с тем же числом атомов углерода в иолекуле.
Б. Температура кипения предельных одноатомных спиртов выше, чем температура
кипения соответствующих углеводородов.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
7. В отличие от этанола, этиленгликоль при обычных условиях взаимодействует с
1) гидроксидом меди (II) 3) бромоводородом
2) калием 4) аммиачным раствором оксида серебра
Часть В
Запишите цифры в порядке возрастания.
8.И этанол и глицерин
1) относятся к многоатомным спиртам
2) имеют молекулярную кристаллическую решетку
3) растворяют гидроксид меди (II)
4) окисляются кислородом
5) взаимодействуют с бромоводородом
6) используются в лаборатории для заправки спиртовки
9. И для фенола, и для бутантриола-1,2,4 справедливы утверждения
1) содержат функциональные группы – ОН
2) относятся к многоатомным спиртам
3) взаимодействуют с углекислым газом
4) проявляют кислотные свойства менее сильные, чем уксусная кислота
5) образуют характерный осадок при взаимодействии с бромной водой
6) в твёрдом состоянии имеют молекулярную кристаллическую решётку
Часть С
10.Составьте уравнения реакций, с помощью которых можно осуществить следующие
превращения:
этан → этен → дибромэтан → этиленгликоль → дихлорэтан
11.При взаимодействии 361 г глицерина с избытком азотной кислоты получено 908 г
тринитроглицерина. Вычислите массовую долю выхода продукта реакции.
Вариант lV
Часть А
Этанол можно получить из этилена в результате реакции
гидратации 3) галогенирования
гидрирования 4) гидрогалогенирования
Фенол не вступает в реакцию с
Na 2) HNO3 3) NaOH 4) HCl
Внутримолекулярная дегидратация спиртов приводит к образованию
альдегидов 3) алкенов
алканов 4) алкинов
Свежеприготовленный осадок Cu(OH)2 растворится, если к нему добавить
пропандиол-1,2 3) пропен
пропанол-1 4) пропанол-2
Пропанол-1 взаимодействует с
этановой кислотой 3) углекислым газом
этаном 4) гидроксидом алюминия
6.Верны ли следующие суждения?
А. Денатурированный спирт – это спирт, содержащий специальные примеси,
имеющие неприятный вкус или запах.
Б. Этиловый спирт – это плохой растворитель.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
7.Этиленгликоль получают при
1) взаимодействии этилена с бромной водой
2) взаимодействии этилена с этанолом
3) гидролизе жиров
4) окислении этилена водным раствором KMnO4
Часть В
Запишите цифры в порядке возрастания.
8.И этанол, и этиленгликоль
1) взаимодействуют с бромной водой
2) взаимодействуют с гидроксидом меди (II)
3) не взаимодействуют с гидроксидом алюминия
4) имеют молекулярное строение
5) образуются при окислении этена раствором перманганата калия
6) являются кислотами более слабыми, чем фенол
9.Для фенола справедливы утверждения:
1) в промышленности получают окислением изопропилбензола
2) не взаимодействует с бромной водой
3) является кислотой более сильной, чем этанол
4) вытесняется из раствора фенолята калия углекислым газом
5) используется в качестве топлива
6) имеет атомную кристаллическую решётку
Часть С
Запишите решения и ответы на обратной стороне бланка.
10.Составьте уравнения реакций, с помощью которых можно осуществить следующие
превращения:
СО → СН3ОН → CH3Br → CH3OH → CH3-O-CH3
11.Этилен объёмом 2,24 л (н.у) вступил в реакцию с водой. Рассчитайте массу
полученного этилового спирта, если выход продукта составляет 85%.







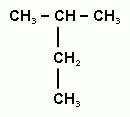
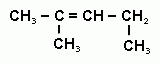 Вещество, формула которого
Вещество, формула которого  Вещество, формула которого
Вещество, формула которого 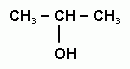


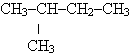 ;
;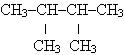 :
:


















