Контрольная работа № 2
по теме: « Кислород. Водород. Растворы. Вода»
1 вариант.
Напишите уравнения реакций горения в кислороде:
А) угля; б) лития; в) сероводорода H2S.Назовите продукты реакций.
Напишите уравнения реакций взаимодействия:
А) магния с соляной кислотой; б) натрия с водой; в)водорода с серой; г) водорода с оксидом меди.
Напишите уравнения реакций, позволяющих осуществить следующие превращения:FeO-----Fe-------FeSO4. и укажите к какому типу реакций относится каждая из них.
Вычислите, какую массу кислорода можно получить при разложении 43,4 г оксида ртути.
Рассчитайте, какой объем водорода (н.у.) образуется при взаимодействии 28 г железа с соляной кислотой.
Вычислите массовую долю растворенного вещества в растворе, полученном при растворении 15 г соли в 45 г воды.
Рассчитайте, какую массу воды необходимо взять для приготовления раствора с массовой долей вещества 20%, если нужно растворить 100 г соли.
Контрольная работа № 2
по теме: « Кислород. Водород. Растворы. Вода»
вариант.
1. Напишите уравнения реакций горения в кислороде:
А) магния; б) фосфора; в) этилена С2H4.
Назовите продукты реакций.
Напишите уравнения реакций взаимодействия:
А) железа с раствором серной кислоты; б) бария с водой; в)водорода с кислородом; г) водорода с оксидом железа Fe2O3.
Напишите уравнения реакций, позволяющих осуществить следующие превращения:Cu-----CuO-------Cu(NO3)2, и укажите к какому типу реакций относится каждая из них.
Рассчитайте, какую массу кислорода можно получить при разложении 24,5 г хлората калия KClO3.
Рассчитайте, какой объем водорода (н.у.) который вступит в реакцию с 25 г оксида кобальта CoO.
Выпарили 50 г раствора, при этом получили 5 г хлорида натрия. Вычислите массовую долю соли в растворе.
Рассчитайте, какую массу сахара и воды нужно взять для приготовления 250 г раствора с массовой долей сахара 15%.
Ответы к К\Р № 2.
Вариант 1.
А) C+O2 ------CO2 оксид углерода(4)
Б) 4Li+O2 -----2Li 2O оксид лития
В) 2H2S+3O2 -----2H2O + 2SO2
вода оксид серы
А) Mg+2HCl------ MgCl2+H2
Б) 2 Na+2H2O------2NaOH+ H2
В) H2 +S----- H2 S
Г)MoO3 +3 H2 ---------Mo+3H2O.
1 2
FeO-----Fe-------FeSO4.
FeO +CO----- Fe+CO2. реакция замещения
2)Fe + H2SO4----- FeSO4+ H2 реакция замещения.
4. Дано: m(HgO)=43,4г.
Найти: m(O2)----?
43,4г хг
РЕШЕНИЕ: 2 HgO--- 2Hg +O2 составляем пропорцию
434г 32 г
 43,4г Х г Х = 43,4*32 = 3,2г
43,4г Х г Х = 43,4*32 = 3,2г





 434 г 32 г 434
434 г 32 г 434
Ответ: m(O2)-3.2 г.
5. Дано: m(Fe)=28г.
Найти: V(H2)----?
РЕШЕНИЕ 28 г Х л
Fe + 2HCl = FeCl2 + H2↑
56 г 22,4 л
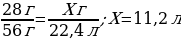
Ответ: V(H2)-11,2 л
6.Дано:
m(в-ва)=15 г
m(воды)=45 г
Найти W(в-ва)-?
Решение:
m(р-ра)=m(в-ва)+m(воды)=15+45=60 г
W(в-ва)=m(в-ва)/m(р-ра) *100%=15/60 *100%=25 %
Ответ: W(в-ва)- 25 %
7. Дано: m (соли) = 100 г ;
ω (соли) = 20 %.или 0,2
Найти: m (H₂O) – ?
Решение: m(р-ра)= m (соли)/ ω (соли)=100/0,2= 500г.
m (H₂O) = m(р-ра)- m (соли)=500г-100г=400г.
Ответ: m (H₂O)= 400 г.
Вариант 2.
1.А) 2. Mg + O₂ = 2MgO.
Б)4 P + 5O2 = 2P2 O5
В) C2 H4 +3O2= 2CO+2H2O
2. A)Fe + H2SO4----- FeSO4+ H2
Б) Ba+2H2O----- Ba(OH)2 + H2
В) 2 H2 + O2 ---2H2O
Г) Fe 2O3 + 3H2---2 Fe+3H2O
3. Cu-----CuO------- Cu(NO 3)2
1) 2Cu + O2 ---- 2CuO- р-я соединения
2) CuO + 2HNO3----- Cu(NO 3)2 +H2O р-я обмена.
4. Дано: m(KClO3)=24,5г.
Найти: m(O2)----?
24,5г хг
РЕШЕНИЕ: 2 KClO3--- 2KCl +3O2 составляем пропорцию
245г 96 г
 24,5г Х г Х = 24,5*96 = 9,6г
24,5г Х г Х = 24,5*96 = 9,6г





 245 г 96 г 245
245 г 96 г 245
Ответ: m(O2)-9,6 г.
5. Дано: m(CoO)=25г.
Найти: V(H2)----?
РЕШЕНИЕ 25 г Х л
CoO + H2 = Co++ H2О ↑
75 г 22,4 л

Ответ: V(H2)-7,467 л
Дано:
m р-ра (соль) = 50 г
m р. в. (соль) = 5 г
Найти: ω . (соль) - ?
Решение:
Массовая доля растворённого вещества соли:
ω . (соль) = m . (соль) / m р-ра (соль) = 5 г / 50 г = 0,1 (10%)
Ответ: ω р. в. (соль) = 10%
Дано: m (раствора) = 250 г ;
ω (соли) = 15 %.или 0,15
Найти: m (H₂O) – ?
m (сахара) –?
Решение: m(сах)= m (раствора)* ω (сах)=0,15*250 г= 37,5г.
m (H₂O) = m(р-ра)- m (сах)=250 г-37,5 г=212,5 г.
Ответ: m (H₂O)= 212,5 г
m (сахара) –37,5 г







 43,4г Х г Х = 43,4*32 = 3,2г
43,4г Х г Х = 43,4*32 = 3,2г


 434 г 32 г 434
434 г 32 г 434