РЕАКЦИИ ОБМЕНА
Ход урока.
I. Организационный момент
II. Актуализация знаний учащихся
Учитель: Всё, что нас окружает, состоит из веществ. Кажется, что они живут своей жизнью, таинственной и непостижимой. Взаимодействуя, они изменяют свои свойства и состав. И задача человека, изучив этот мир, постараться использовать полученные знания во благо.
И начать урок я хочу с загадки:
Эти явления знаете вы В жизни нашей встречаются они, А отличают эти явления - взаимные превращения, И образуются всегда – новые вещества Что же это за явления? ( химические реакции)
Учитель: Совершенно, верно. А кто ответит, что такое химическая реакция?
( ответ детей)
Учитель: С какими тремя типами химических реакций мы познакомились на предыдущих уроках?
(ответы детей)
Учитель: Хорошо, а сейчас я предлагаю вам немного поиграть. На слайде 4 химических реакций, 3 из них вам знакомы, а одна является «лишней», т.е. еще неизученной нами. Вам необходимо определить тип химических реакций, записать уравнения и расставить коэффициенты, поэтому открываем тетради, записываем сегодняшнее число – 7 марта и приступаем к выполнению заданий.
( 2 человека работают у доски, затем сверка ответов с объяснениями).
Закончить уравнения реакций, расставить коэффициенты и указать тип реакции.
H2 + Cl2 → 2HCl
Zn + 2HCl → ZnCl2 + H2
2HgO → 2Hg + O2
NaOH + HCl →… + …
Учитель: Итак, очевидно, что сегодня на уроке мы с вами познакомимся с новым типом химических реакций.
/Учитель подходит к ученику и просит у него ручку, а ему отдает карандаш/.
Вопрос: Что мы сделали? /Обменялись/.
III. Изучение нового материала.
И эти реакции получили название реакции обмена. Запишем тему урока: реакции обмена.
Тема урока : «Реакции обмена». (Слайд 11) /Записывают в тетрадях/.
Вопрос: Какая реакция называется реакцией обмена?
Реакции обмена – это реакции, в результате которых два сложных вещества обмениваются своими составными частями
АВ + СД → АД + СВ
Демонстрационный опыт. (В ходе опыта обязательно обращать внимание на среду раствора)
NaOH + фенофталеин + H2SO4 → раствор обесцветился. Какая среда?
 среда /нейтральная/
среда /нейтральная/
окраска малиновая кислотная
какая среда? /щелочная/
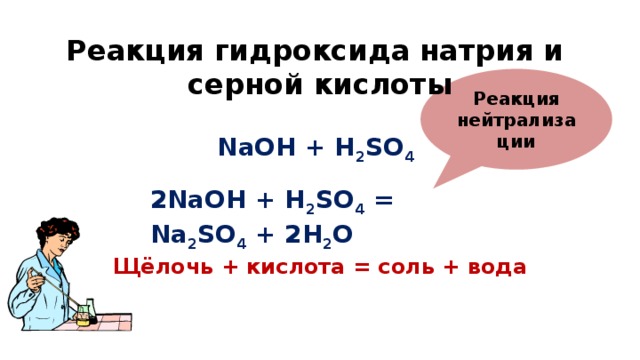
Реакция между основанием и кислотой, называется реакцией нейтрализации.
Это частный случай большого типа реакций обмена.
2. Прежде, чем мы приступим к практике, давайте вспомним основные правила техники безопасности в кабинете химии при проведении лабораторных работ. (беседа по Т.Б.). Цель нашего практикума не только провести опыты, но и выяснить в каких случаях реакции обмена идут до конца.
| Инструкция «Реакции обмена»
Правила безопасности. Соблюдайте осторожность при работе с растворами кислот и щелочей. Опыт 1. В пробирку налейте 1-2 капли раствора сульфата меди CuSO4 и прилейте раствор гидроксида натрия NaOH. Что наблюдаете? Составьте уравнение химической реакции. Опыт 2. В пробирку с осадком гидроксида меди (II) Cu(OH)2 прилейте соляную кислоту HCl. Что наблюдаете? Составьте уравнение химической реакции. Опыт3. В пробирку налейте раствор карбоната натрия Na2CO3 и осторожно прилейте раствор соляной кислоты HCl. Что наблюдаете? Составьте уравнение химической реакции. |
Лабораторный опыт №1 /учащиеся делают на местах/.
В пробирку налить раствор CuSO4 и прилить раствор NaOH. Что наблюдаем?
Выпал осадок.
Запишем уравнение реакции на доске.
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4. (Слайд 13)
Мы видели выпадение осадка. Какое же вещество выпало в осадок? Чтобы ответить на этот вопрос необходимо узнать какое вещество растворяется, а какое нет. Обратимся к таблице растворимости. Вещество Cu(OH)2 нерастворимо, следовательно именно оно выпало в осадок. Осадок обозначается стрелкой вниз ↓.
Вывод: Выпадение осадка одно из условий того, что реакция идёт до конца.
Лабораторный опыт №2 /учащиеся делают на местах/.
Взять пробирку с осадком Cu(OH)2 и прилить к нему HCl.
Что наблюдаете? Осадок растворился.
Чтобы определить продукты реакции запишем уравнение реакции.
Cu(OH)2 + 2 HCl → CuCl2 + 2H2O
Образовалась вода. (Слайд 14)
Вывод: Если в результате реакции образуется вода, то такие реакции
протекают до конца.
Лабораторный опыт №3 /учащиеся делают на местах/.
В пробирку налить раствор Na2CO3 и осторожно прилить раствор HCl.
Что наблюдаете? Образование газа.
Запишем уравнение реакции
Na2CO3 + 2HCl → 2NaCl + H2CO3
В таком виде записанное уравнение реакции не показывает образование газа. Угольная кислота в свободном виде не существует, т.к. является нестойкой и легко разлагается на воду и соответствующий оксид. (степень окисления углерода в кислоте и оксиде одинаковая + 4).
Na2CO3 + 2HCl → 2NaCl + CО2↑ + H2O
Оксид обозначается стрелкой вверх ↑. (Слайд 15)
Вывод: Если в результате реакции образуется газ, следовательно реакция
идет до конца (т.е. практически возможна).
Учитель: Мы с вами выяснили, что химические реакции обмена идут до конца в нескольких случаях. Назовите их.
( ребята отвечают)
Учитель: Обратите своё внимание ещё раз на экран:
Если выделился газ – это раз! И получится вода – это два! А еще нерастворимый осаждается продукт… «Есть осадок», говорим мы – это третий важный пункт! Химик «правила обмена» не забудет никогда: В результате – непременно будет газ или вода. Выпадает осадок – вот тогда порядок!
IV. Закрепление.
1) Среди предложенных реакций выбрать реакции обмена, и определить протекают ли они до конца. (Слайд 16)
| CuO + H2 = Cu + H2O | NaCl + AgNO3 = AgCl + NaNO3 |
| 3K2CO3 + 2H3PO4 = 2K3PO4 + 3H2O + +3CO2 | CaO + H2O → Ca(OH)2 |
| 2H2O = 2H2 + O2 | 3Ca(OH)2 + 2H3PO4 → Ca3(PO4)2 + +6H2O |
| CaO + 2HCl → CaCl2 + H2O | FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl |
2) Самостоятельная работа.
Закончите уравнения химических реакций и расставьте коэффициенты:
1 вариант 2 вариант
а) NaOH + HCl → а) Na2CO3 + HNO3 →;
б) Al(OH)3 + H2SO4 →; б) NaI + Pb(NO3)2 →
в) Ca(OH)2 + HCl →; в) CuO + H2SO4 →
г) CaCO3 + HCl →; г) KOH + CuSO4 →
д) KOH + H2SO4 →. д) BaCl2 + AgNO3 →.
V. Подведение итогов.
Вернемся к теме сегодняшнего урока.
Какую цель мы поставили в начале урока?
К какому выводу мы пришли?
Домашнее задание:
§ 27 (реакции обмена).
упр.2, 3 (выбрать реакции обмена и определить идут ли они до конца).
Объявление оценок.





 среда /нейтральная/
среда /нейтральная/