Тема: «Алкадиены»
Цель:
Систематизировать и конкретизировать знания учащихся о непредельных углеводородах на примере алкадиенов.
Задачи:
Образовательные:
ознакомить с физическими свойствами и основными способами получения алкадиенов;
изучить химические свойства алкадиенов: реакции присоединения и полимеризации;
ознакомить учащихся с натуральным и синтетическим каучуком, резиной;
Развивающие:
способствовать развитию внимательности, усидчивости, дисциплины;
развивать самостоятельность и волю учащихся , используя поощрение настойчивости при решении задач, устранении опеки при оказании помощи;
развивать познавательный интерес используя данные о применении алкадиенов;
Воспитательные:
продолжить формирование локальной химической картины мира;
содействовать в ходе урока формированию следующих мировоззренческих идей:
обусловленность развития химической науки потребностями производства, жизни и быта;
истинность научных знаний и законов природы;
обеспечить нравственно эстетическое воспитание.
Ход урока:
Работать будем по следующему плану, ваша задача составить опорный конспект.
1. Алкадиены. Общая характеристика.
2. Изомерия. Номенклатура.
3. Получение, физические свойства.
4. Химические свойства
5. Применение. Каучук. Резина.
Алкадиены - органические соединения, углеводороды алифатического (ациклического) непредельного характера, в молекуле которых между атомами углерода - две двойные связи, и которые соответствуют общей формуле CnH2n-2, где n =3 или n 3.
CH2 == CH –––– CH == CH2
бутадиен-1,3
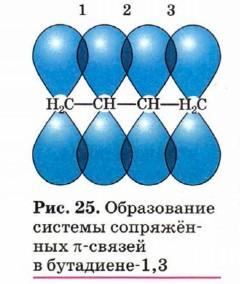
Для алкенов характерна sp2-гибридизация. У бутадиена - 1,3 у четырех негибридных p-электронов образуется общее π - электронное облако, в результате чего происходит делокализация двойных связей в молекуле, связи между молекулами C1 и C2, C3 и C4 удлиняются (по сравнению с двойной связью - 0,134 нм), а связь между C2 и C3 укорачивается (по сравнению с одинарной связью - 0,154 нм):
Такая особенность строения называется эффектом сопряжения двойных связей и определяет реакционную способность алкадиенов.
В названии алкенов содержится суффикс -диен («две» «двойные связи»), обозначающий принадлежность соединения к данному классу.
Классификация
CH2 = C = CH2
Пропадиен (аллен)
2. Диены с сопряженными связями
Двойные связи разделены одной одинарной связью
CH2 = CH – CH = CH2
Бутадиен-1,3 (дивинил)
3. Диены с изолированными связями
Двойные связи разделены двумя или более одинарными связями
CH2 = CH – CH2 – CH = CH2
Пентадиен-1,4
В определении названия алкадиена (как и у всех непредельных углеводородов) положение кратной связи имеет при нумерации преимущество перед остальными.
Для алкадиенов характерны следующие виды изомерии:
Структурная изомерия:
а) изомерия углеродного скелета
CH2=CH – CH = CH – CH3 CH2= C – CH = CH2
|
CH3
пентадиен-1,3 2-метилбутадиен-1,3 (изопрен)
б) изомерия положения кратной связи
CH2=CH – CH = CH – CH3 CH3–CH = C = CH – CH3
пентадиен-1,3 пентадиен-2,3
в) изомерия положения заместителей (Hal, - NO2, SO2-OH и др.)
CH2=CH – C = CH – CH3 CH2=CH – CH = C – CH3
| |
Cl Cl
3-хлорпентадиен-1,3 4-хлорпентадиен-1,3
Пространственная изомерия:
а) геометрическая изомерия
CH3 – CH = C – CH = CH2
|
CH3
3-метилпентадиен-1,3
Межклассовая изомерия (с циклоалкенами и алкинами)
CH2=CH – CH = CH – CH3 CH = CH
пентадиен-1,3
CH2 - CH2
CH ≡ C – CH2 – CH2 – CH3
CH2
пентин-1 циклопентен
Физические свойства.
Бутадиен-1,3 и пропадиен - газы; 2-метилбутадиен-1,3 - летучая жидкость; алкадиены с изолированными двойными связями – жидкости; высшие алкадиены - твердые вещества.
Химические свойства.
Химические свойства алкадиенов с изолированными связями протекают так же, как и у алкенов - только в два этапа, а у алкадиенов с сопряженными связями - с некоторыми особенностями: способность присоединять молекулы как в положения 1 и 2 (подобно алкадиенам с изолированными связями – 1,2-присоединение), так и в положении 1 и 4 (перераспределение двойной связи – 1,4-присоединение) – зависит от условий и способа проведения реакций.
Реакции присоединения
гидрирование
а) с изолированными связями
CH2=CH – CH2 – CH = CH2 + H – H CH3 – CH2 – CH2 – CH = CH2
пентадиен-1,4 пентен-1
CH3 – CH2 – CH2 – CH = CH2 + H – H CH3 – CH2 – CH2 – CH2 – CH3
пентен-1 пентан
б) с сопряженными связями
CH2 = CH – CH = CH – CH3 + H – H CH3 – CH = CH – CH2 – CH3
пентадиен-1,3 пентен-2
CH3 – CH = CH – CH2 – CH3 + H – H CH3 – CH2 – CH2 – CH2 – CH3
пентен-2 пентан
Галогенирование
CH2=CH – CH2 – CH = CH2 + Br – Br CH2Br – CHBr – CH2 – CH = CH2
пентадиен-1,4 4.5-дибромпентен-1
CH2Br – CHBr – CH2 – CH = CH2 + Br – Br CH2Br – CHBr – CH2 – CHBr – CH2Br
4,5-дибромпентен-1 1,2,4,5-тетрабромпентан
б) с сопряженными связями
CH2 = CH – CH = CH – CH3 + Br – Br CH2Br – CH = CH – CHBr – CH3
пентадиен-1,3 1.4-дибромпентен-2
CH2Br – CH = CH – CHBr – CH3 + Br – Br CH2Br – CHBr – CHBr – CHBr – CH3
1,4-дибромпентен-2 1,2,3,4-тетрабромпентан
Гидрогалогенирование (по правилу Марковникова: при присоединении веществ с полярной ковалентной связью типа HX (где X – это -Hal, -OH и т.д.) к несимметричным непредельным углеводородам по месту разрыва П-связи атом водорода присоединяется к наиболее гидрированному атому углерода, а X – к наименее гидрированному атому углерода)
CH2=CH – CH2 – CH = CH2 + H – Br CH3 – CHBr – CH2 – CH = CH2
Реакции полимеризации.
n CH2 = CH – CH=CH2-(– CH2 – CH = CH – CH2 –)n
бутадиен-1,3 бутадиеновый каучук
Получение.
1. Метод Лебедева (1932г.) – дегидратация и дегидрирование
450oC, Al2O3, ZnO
2 CH3 – CH2 – OH ----------------- CH2=CH – CH = CH2 + H2O + H2
этанол бутадиен-1,3
2. Способ дегидрирования
500-600⁰C, Kt
CH3– CH2 – CH2 – CH3 --------------- CH2=CH – CH = CH2 + H2
н-бутан бутадиен-1,3
(проходит в две стадии)
Применение.
Поскольку при разложении природного каучука образовывались диеновые углеводороды, стало ясно и обратное: полимеризацией диенов можно получать синтетические каучукоподобные материалы.
Диеновые углеводороды применяются в производстве синтетических каучуков, из которых в том числе делают и резину.
Природный каучук является липким эластичным, резиноподобным материалом, но по сравнению с каучуком выше.
Домашнее задание:
Решите тест по теме: «Алкадиены»
1. Повторите теоретический материал;
2. Диеновые углеводороды имеют формулу:
а) СnН2n + 2; б) СnС2n; в) СnНn; г) СnН2n – 2
2. Кратные связи в углеводороде:
СН2 = СН – СН = СН – СН3 называются
а) кумулированные.
б) сопряженные.
в) изолированные.
3. Укажите тип гибридизации атомов углерода в веществе:
СН2 = С = СН – СН3
4. Исходным веществом для синтеза бутадиена 1, 3 по методу Лебедева является
а) бутиловый спирт
б) бутен-1.
в) этиловый спирт.
5. Диеновые углеводороды являются межклассовыми изомерами:
а) алканов.
б) алкенов в) алкинов.

























