Просмотр содержимого документа
«Конспект урока "Переходные элементы. Амфотерные оксиды и гидроксиды"»
Переходные элементы. Амфотерные оксиды и гидроксиды
Элементы содержания: амфотерность оксидов и гидроксидов.
Требования к уровню подготовленности выпускников.
Уметь: составлять уравнения химических реакций с участием амфотерных оксидов и гидроксидов.
Цель: сформировать представление учащихся о переходных элементах, амфотерных соединениях; научить их записывать уравнения реакций с участием амфотерных оксидов и гидроксидов, доказывать амфотерность вещества.
Оборудование: цинк (гранулы или пластинка), растворы хлорида цинка, гидроксида натрия, соляной кислоты, демонстрационные пробирки; дополнительно: образец хрома, раствор хлорида хрома (III), оксид хрома (III).
Ход урока
I. Проверка домашнего задания.
У доски два человека – упр. 7, 8. Фронтально: с чем реагируют кислоты, щёлочи, соли, основные оксиды, кислотные оксиды? Как доказать кислотный характер оксида, гидроксида? Как доказать основный характер оксида, гидроксида? Как изменяется характер оксидов и гидроксидов в периоде, в группе?
II. Объяснение нового материала.
Перед вами простое вещество цинк. Металл это или неметалл? Почему? Давайте проверим наше предположение. Для этого получим гидроксид цинка. Как получить нерастворимый гидроксид? По каплям прильём к раствору хлорида цинка гидроксид натрия. Выпал осадок, запишем уравнение реакции:
ZnCl2 + 2NaOH → Zn(OH)2↓+ 2NaCl
Разделим Zn(OH)2 пополам; к одной части прильём соляную кислоту. Гидроксид растворился.
Запишем уравнение реакции:
Zn(OH)2+2HCI → ZnCl2+2H2О
Гидроксид цинка реагирует с кислотой, проявляет основные свойства.
Проверим, не будет ли гидроксид цинка растворяться в щёлочи. Растворяется. Значит, Zn(OH)2 можно записать в виде кислоты: 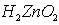 .
.
Тогда 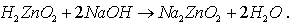
цинкат
натрия
Zn(OH)2 реагирует со щёлочью, проявляет кислотные свойства. Вещества, обладающие и кислотными, и основными свойствами, называются амфотерными, а элементы, образующие такие вещества, – переходными. На форзаце учебника эти элементы обозначены зеленым цветом. У некоторых элементов с переменной степенью окисления существует несколько рядов соединений: основные (в низшей степени окисления), амфотерные (в средней степени окисления), кислотные (в высшей степени окисления). Например, хром. Рассмотрите схему на с. 10 учебника. Эксперимент: из хлорида хрома (III) получим гидроксид хрома (III) и проведем реакции с соляной кислотой и гидроксидом натрия. Запишите уравнения реакций:
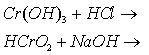
Домашнее задание: § 2, упр. 2, 3.