Просмотр содержимого документа
«Конспект и презентация учебного занятия по химии "Основания" 8 класс»
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа рос. Известковый Амурского муниципального района Хабаровского края.
Учитель химии: Алябьева Анна Сергеевна
Дата проведения урока: 18 января 2023 г.
Класс: 8
Учебник: Химия – 8. Авторы: Г.Е.Рудзитис, Ф.Г.Фельдман.
Тема: Основания
Цель: изучить новый класс неорганических соединений – основания.
Задачи:
познакомить учащихся с новым классом неорганических соединений – основаниями; рассмотреть классификацию, состав и номенклатуру оснований.
развить у учащихся такие личностные качества как сосредоточенность, наблюдательность; умение сравнивать, анализировать, обобщать, работать с таблицей растворимости.
воспитать у обучающихся умение высказывать свою точку зрения и аргументировать её, умение слушать и уважать мнение товарищей.
Тип урока: изучение нового материала.
Учебно-наглядные пособия: твёрдые щелочи и их растворы (NaOH, KOH, Ca(OH)2, индикаторы, свежеполученные осадки гидроксидов нерастворимых оснований, соляная кислота, электронная таблица «Растворимость кислот, оснований и солей в воде», инструкция по технике безопасности при работе со щелочами.
Ход урока
I. Организационный этап.
(Учитель приветствует учащихся, настраивает класс, проводит беседу с дежурным.)
II. Проверка домашнего задания и усвоения основных понятий предыдущих уроков
| Деятельность учителя | Деятельность обучающихся |
| Учитель задает устные вопросы. -Что такое бинарные соединения? | -Сложные вещества, состоящие из двух химических элементов. |
| -Какие бинарные соединения вы знаете? | -Оксиды, сульфиды, нитриды, силициды, фториды, хлориды и гидриды. |
| -Какие же вещества называются оксидами? | -Вещества состоящая из двух элементов, и на втором месте кислород называются оксидами. |
| -На какие группы делятся оксиды? | -1) оксиды металлов 2) оксиды неметаллов |
| Далее выполняются тестовые задания 1 и 2 вариант Формулы. Na, K2O, FeS, NaOH, ZnCl2 KCl, CaO, KOH, Cu, Al2O3
CaCl2, Br2, Cu(OH)2, NaH, CuO Fe, Na2O, Fe(OH)3, CaF2 Учащиеся должны распределять их по группам. На слайде таблица |
|
| Простые вещества | Бинарные соединения | Не знакомые вещества |
| На выполнение 3 минуты. Учащиеся обмениваются листочками с ответами. Взаимопроверка другого варианта и оценивание. |
| В графе незнакомых веществ учащиеся пишут следующие: NaOH, KOH, Cu(OH)2,Fe(OH)3. Эти формулы написаны на слайде. |
| 3.Актуализация знаний, постановка познавательной задачи, определение темы. Учитель обращает учащимся обратить внимание на экран. -Почему этих формул вы не написали на бинарные или на простые? | Потому что, в состав этих веществ входит 3 элемента. Мы пока знаем только
Учащиеся открывают тетради, пишут число и тему урока. |
| -Правильно , ребята. Оставшиеся формулы веществ, пока вам не знакомы и сегодня нам на уроке предстоит задача познакомиться с этими веществами. Они относятся к классу «Оснований». |
| Учитель ставит перед классом познавательную задачу. Учащиеся проговаривают цель урока и задачи. -Какие же вещества относятся основаниям? |
|
III. Изучение нового материала
| Деятельность учителя | Деятельность обучающихся |
| 1. Состав и названия оснований |
| Какие же вещества относятся основаниям? − Что общего между записанными на доске химическими формулами оснований? | − В состав химических формул оснований входят атомы металла, кислорода и водорода.
|
| Учитель объясняет, что атомы кислорода и водорода входят в состав молекул оснований в виде гидроксогруппы (гидроксид-иона) OH-. Учитель просит ребят определить суммарный заряд гидроксид-иона, записав степень окисления атомов водорода и кислорода -   | Суммарный заряд гидроксид-иона «-1» (ОН-). |
| Общая формула оснований: Men+(OH)n, где n – заряд иона металла, численно равный его степени окисления. | Записывают формулу оснований в тетрадь. |
| Учитель вместе с ребятами разбирают формулу на примере конкретного металла: калия, натрия, кальция, меди. | K+OH, Na+OH, Са2+(OH)2, Cu(OH)2. |
| Учитель подводит учащихся к самостоятельному формулированию определения оснований. Пытаются дать определение основаниям. Затем сравнивают с определением в учебнике §31 | Основания − это сложные вещества, состоящие из атомов металла и связанных с ними гидроксогруппами (записывают в тетрадь). |
| Учитель разбирает номенклатуру оснований: «гидроксид» + (кого? чего?) металла | KOH – гидроксид лития, NaOH – гидроксид алюминия, Ca(OH)2 – гидроксид кальция, Cu(OH)2 – гидроксид меди (II) |
|
2. Классификация оснований |
| Учитель объясняет, что по растворимости в воде, все основания делятся на две группы: на растворимые и малорастворимые, или щёлочи и нерастворимые.
| Учащиеся зрительно воспринимают схему (см.ниже). |
| Учитель знакомит и учит учащихся пользоваться таблицей растворимости. | Учащиеся помогают учителю соотнести вышеназванные формулы оснований к тому или иному типу оснований: 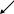 Основания Основания 
растворимые нерастворимые (щёлочи) Сu(OH)2 NaOH KOH
малорастворимые (щёлочи)  Ca(OH)2 Ca(OH)2 |
| Учитель даёт задания по определению растворимости оснований: Mg(OH)2, Al(OH)3, Ba(OH)2. | Mg(OH)2 – нерастворимое, Al(OH)3 – нерастворимое, Ba(OH)2 – растворимое (щёлочь) |
| Учитель объясняет, что щёлочи являются едкими веществами – они сильно разъедают кожу, дерево, бумагу. Если раствор щёлочи попадёт на руку и его не смыть, кожу начинает щипать и вскоре образуется язва. Если щёлочь случайно попала на кожу, её надо немедленно смыть большим количеством проточной воды, а затем при необходимости протереть поврежденный участок кожи слабым раствором борной или уксусной кислоты. Поэтому, гидроксид натрия NaOH ещё известен под названием едкий натр, каустическая сода, каустик, а гидроксид кали KOH – как едкое кали. Сильно разбавленные растворы мыльные на ощупь. | Учащиеся слушают и запоминают. Знакомятся с техникой безопасности. |
| Учитель предлагает провести эксперимент: испробовать действие индикаторов на гидроксид натрия. (Учащиеся в 3 пробирки с 2 мл раствора гидроксида натрия добавили по одной капли каждого индикатора. Полученные результаты записали в тетрадь). При добавлении индикаторов к нерастворимым основаниям изменений окраски не происходит.
| Учащиеся наливают в три пробирки раствор гидроксида натрия. Полученные результаты фиксируют в таблице: | Сравнительный признак | Щелочь | | Взаимодействие с индикаторами: а) бесцветный фенолфталеин; б) фиолетовый лакмус; в) метиловый оранжевый |
а) малиновая окраска б) синяя окраска в) жёлтая |
|
IV. Закрепление материала. Проверка усвоения учебного материала.
| Деятельность учителя | Деятельность обучающихся |
| Учитель проводит игру «Веришь-не веришь». Отвечаем на вопросы «да» или «нет». Верите ли вы, что- В состав оснований входит металл и гидроксильная группа? Гидроксид ион- это сложный анион? Основание-это простое вещество? Гидроксид меди(II) –растворимый гидроксид? Лакмус оранжевого цвета? В щелочной среде бесцветный фенолфталеин становится малиновым? Гидроксид бария имеет формулу- Ba(OH)3 Гидроксид алюминия является щелочью? |
Учащиеся отвечают на вопросы учителя: да да Нет Нет Нет Да
Нет да нет
|
| V. Итоги урока. Учитель подводит итоги урока. Оценивает работу класса в целом и отдельных учащихся, комментирует полученные учащимися оценки. |
|
| VI. Домашнее задание §31 стр93-95 (до «химические свойства». Вопрос №1-5 стр 99 |
|
| VII. Рефлексия. Каждому учащемуся раздаются листочки с таблицей для последующего заполнения | |
| Понравился ли урок? | Что узнали нового? | Что хотели бы узнать? |
|
|
|
|
7






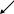 Основания
Основания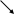
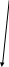 Ca(OH)2
Ca(OH)2


















