Просмотр содержимого документа
«Комуртек жана анын касиеттери.»

Көмүртек


Физикалык касиеттери
Көмүртек ар түрдүү физикалык касиеттерге ээ болгон, көптөгөн аллотропиялык модификациялар түрүндө кездешет. Модификациялардын түрдүүлүгү көмүртектин ар түрдүү химиялык байланыштарды пайда кылуу жөндөмдүүлүгү менен шартталган.
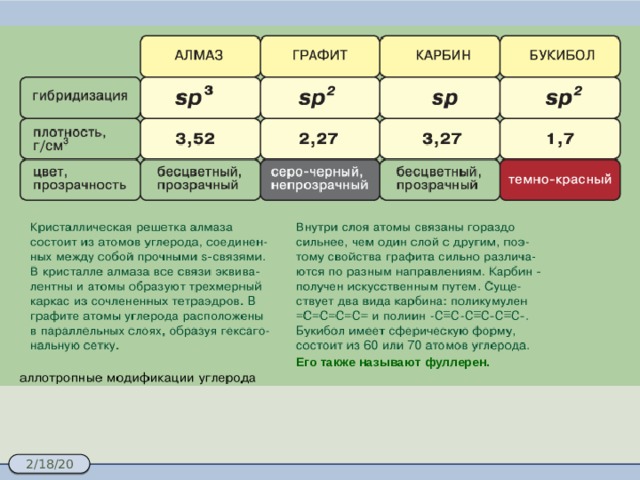
Его также называют фуллерен.
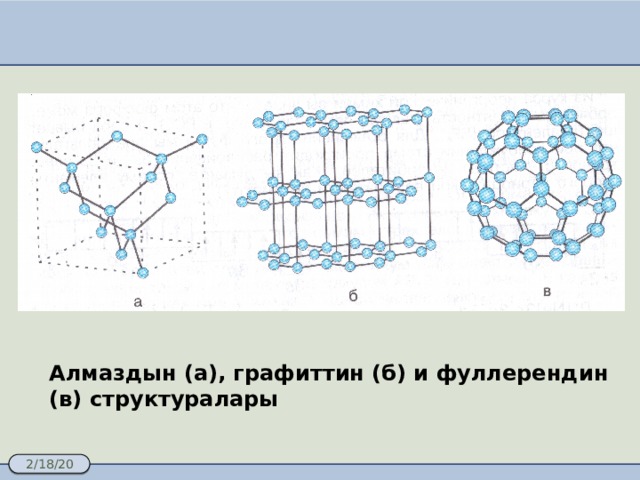
Алмаздын (а), графиттин (б) и фуллерендин (в) структуралары

Алмаздын (а) жана графиттин (б) кристаллдык торчолору
а
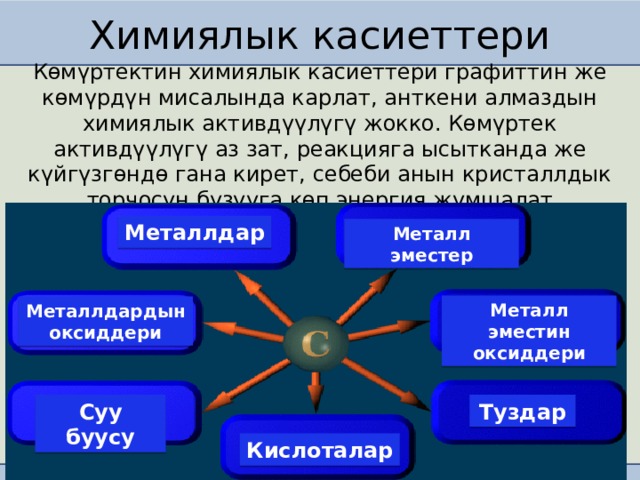
Химиялык касиеттери
Көмүртектин химиялык касиеттери графиттин же көмүрдүн мисалында карлат, анткени алмаздын химиялык активдүүлүгү жокко. Көмүртек активдүүлүгү аз зат, реакцияга ысытканда же күйгүзгөндө гана кирет, себеби анын кристаллдык торчосун бузууга көп энергия жумшалат
Металлдар
Металл эместер
Металл эместин оксиддери
Металлдардын оксиддери
Туздар
Суу буусу
Кислоталар
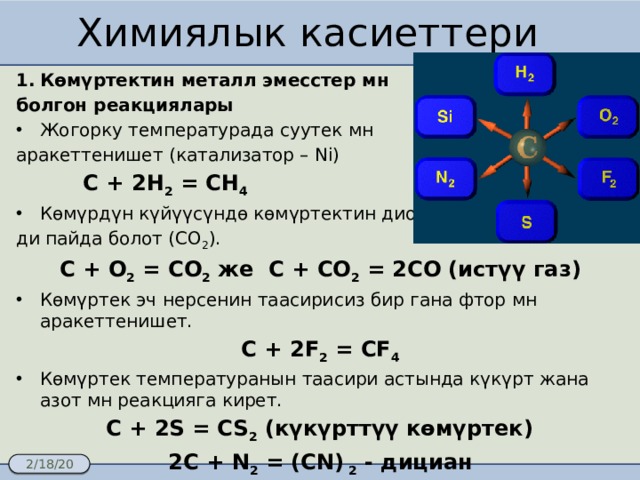
Химиялык касиеттери
- Көмүртектин металл эмесстер мн
болгон реакциялары
- Жогорку температурада суутек мн
аракеттенишет (катализатор – Ni)
C + 2H 2 = CH 4
- Көмүрдүн күйүүсүндө көмүртектин диокси-
ди пайда болот (СО 2 ).
C + O 2 = CO 2 же С + СО 2 = 2СО (истүү газ)
- Көмүртек эч нерсенин таасирисиз бир гана фтор мн аракеттенишет.
С + 2F 2 = CF 4
- Көмүртек температуранын таасири астында күкүрт жана азот мн реакцияга кирет.
C + 2S = CS 2 (күкүрттүү көмүртек)
2C + N 2 = (CN) 2 - дициан

Химиялык касиеттери
- Көмүртектин металлдар жана алардын оксиддери мн болгон реакциялары
- Жогорку температурада көмүртек металлдар жана алардын оксиддери мн карбиддерди пайда кылат.
2C + Ca = CaC 2 2Na + 2C = Na 2 C 2
4Al + 3C = Al 4 C 3 C + 3Fe = Fe 3 C;
- Көмүр ысытканда күчтүү калыбына келтиргич касиетти көрсөтөт, ошондуктан металлургияда колдонулат
CaO + 3C = CaC 2 + CO 2 ; Al 2 O 3 +9C = Al 4 C 3 + 6CO
Fe 3 O 4 + 2C = 3Fe + 2CO 2 ; 2ZnO + C = 2Zn + CO 2
MnO 2 + C = Mn + CO 2

3. Кислоталар менен болгон реакциялары
Көмүртек ысытканда азот жана конц. күкүрт кислоталары мн кычкылданат. (төмөнкү температурада кислоталардын таасирине туруктуу).
C + 2H 2 SO 4 (конц.) = CO 2 + 2SO 2 + 2H 2 O
3C + 4HNO 3 (эрит.) = 3CO 2 + 4NO + 2H 2 O
4. Металл эместердин оксиддери менен реакциясы
Жогорку температурада (1000 o C) көмүр сууну ажыратат:
С + H 2 O = CO + H 2
SiO 2 + C = Si + CO 2
5. Туздар менен болгон реакциялары:
BaSO 4 + 2C = BaS + 2CO 2
Ca 3 (PO 4 ) 2 + 10C + 6SiO 2 = P 4 + 6CaSiO 3 + 10CO

Көмүртек организмде
Көмүртек – жердеги жашоонун негизин түзгөн маанилүү биогендүү элемент, организмдердин курамын түзгөн жана алардын турмуш-тиричилигин камсыздаган көптөгөн органикалык заттардын структуралык бирдиги (биополимерлер, ошондой эле көптөгөн майдамолекулярдуу активдүү заттар - витаминдер, гормондор, медиаторлор ж.б.). Организмге керектелген энергиянын маанилүү бөлүгү көмүртектин кычкылдануусунун эсебинен жүрөт. Жердеги жашоонун пайда болуусу күнүбүздөгү илимде көүртектүү бирикмелердин эволюциясынын татаал процесси катары каралат.

Жаратылышта кездешүүсү
Жаратылышта көмүртек төмөнкү түрлөрдө кездешет:
- Алмаз
- Карбин
- Графит
- Бирикмелерде – таш жана күрөң көмүр жана нефтинин курамында.
- Табигый карбонаттардын курамына кирет: акиташ, мрамор, бор - CaCO 3 , доломит CaCO 3 , MgCO 3 . органикалык заттардын негизги курамдык бөлүгү болуп саналат.
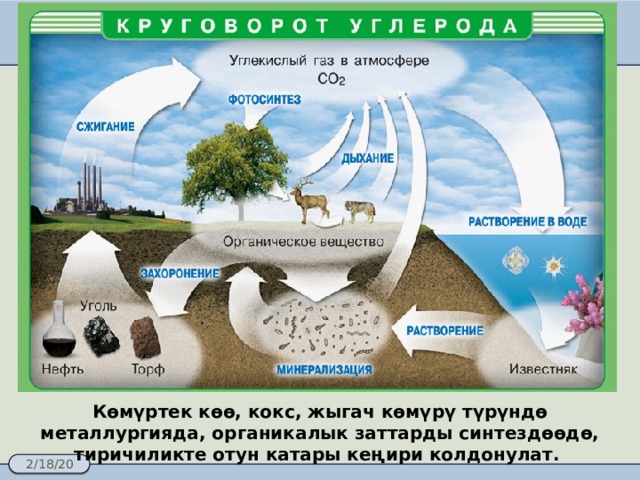
Көмүртек көө, кокс, жыгач көмүрү түрүндө металлургияда, органикалык заттарды синтездөөдө, тиричиликте отун катары кеңири колдонулат.





































