Просмотр содержимого документа
«Кейс "Алюминий"»

Вопросы
1. Дайте характеристику алюминию по его положению в периодической системе химических элементов по плану:
«Адрес» элемента
Число протонов, электронов и нейтронов в атоме
Распределение электронов по энергетическим уровням.
Металл или неметалл?
Характерная степень окисления.
Формула оксида и гидроксида алюминия, их характер.
2. Объясните происхождение названия химического элемента алюминия?
Физические свойства и применение алюминия

Из учебника химии:
Алюминий – серебристо-белый металл. Очень пластичен, легко вытягивается в проволоку. Не подвергается коррозии, так как на его поверхности есть защитная пленка оксида алюминия. Хорошо проводит электрический ток и тепло. Алюминий не токсичен, то есть не ядовит.
Из учебника физики: Чем ниже электрическое сопротивление металла, тем лучше он проводит электрический ток, то есть обладает высокой электропроводностью.
Удельная теплоемкость показывает какое количество теплоты требуется для нагревания 1 кг вещества на 1 градус Цельсия.
Чем выше удельная теплоемкость вещества, тем медленнее оно нагревается и дольше остывает в одних и тех же условиях.
Вопросы
Пользуясь информацией кейса, опишите физические свойства алюминия.
Пользуясь информацией кейса, сравните физические свойства алюминия с железом и медью. Сделайте выводы.
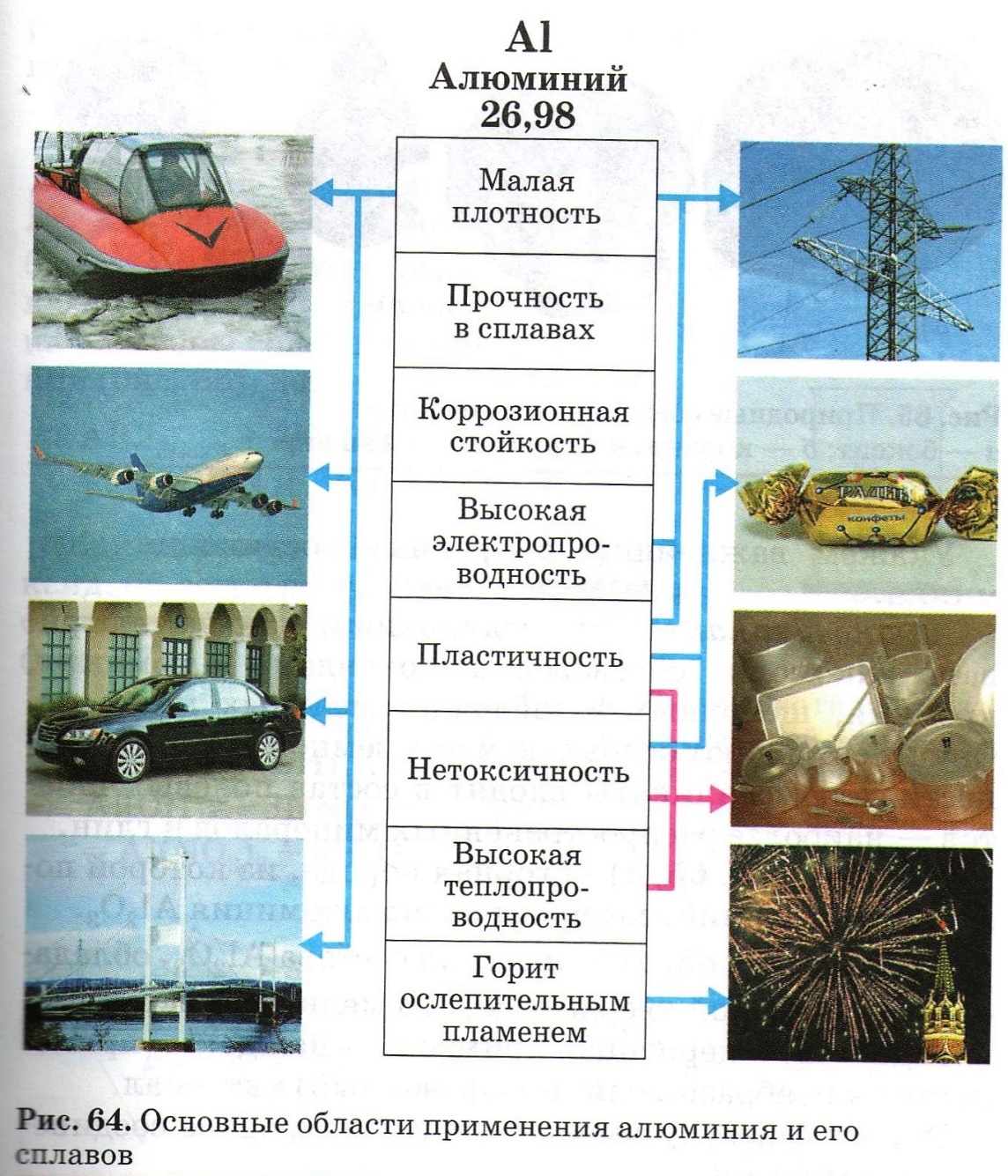
На основании рис.64 опишите области применения алюминия, основанные на его физических свойствах

Вопросы
По предложенной диаграмме определите какое место занимает алюминий по распространенности в природе среди всех элементов? Среди металлов?
Назовите соединение алюминия, наиболее распространённое в природе. Встречается ли алюминий в природе в чистом виде? Назовите минералы, содержащие алюминий.
Кто и когда впервые получил алюминий? Напишите уравнения реакции.
Современный способ получения алюминия был изобретен в 1886 году. Кем он был предложен? В чем его суть? Напишите уравнение реакции, которое соответствует этому методу.

Задание (ВНИМАНИЕ! Соблюдайте правила техники безопасности!!!)
Напишите уравнения реакций, изображения которых содержит кейс.
Вам предложены следующие реактивы: гранулы алюминия, раствор сульфата меди (II), раствор хлорида натрия. Опустите в 2 пробирки по грануле алюминия. В первую пробирку прилейте раствор сульфата меди (II), во вторую раствор хлорида натрия. В пробирку с раствором сульфата меди (II) добавьте катализатор – кристаллики поваренной соли. Рассмотрите содержимое пробирок через 2 минуты. Какое свойство металлов вы проверили на примере этих взаимодействий? Что такое катализатор? Напишите уравнение произошедшей реакции.
Вам предложены следующие реактивы: гранулы алюминия, кусочки медной проволоки, раствор соляной кислоты. Опустите в первую пробирку гранулу алюминия. Во вторую пробирку поместите медь. Прилейте в обе пробирки раствор соляной кислоты. Что наблюдаете? Если внешних изменений не происходит, то подогрейте содержимое пробирок до первых признаков кипения. Зафиксируйте наблюдения. Какую гипотезу можно проверить с помощью данного исследования? Напишите уравнение произошедшей реакции.
Для реакции алюминия с раствором гидроксида натрия составьте электронный баланс, укажите окислитель и восстановитель, расставьте коэффициенты.





























