
КАРБОН КИСЛОТАЛАР
Маъруза режаси:
- Тузилиши, синфланиши, изомерияси, номенклатураси
- Олиниш усуллари, физик ва кимёвий хоссалари
- Карбон кислоталарнинг галогенли ҳосилалари
- Айрим вакиллари

Тузилишида - карбоксил гуруҳи бўлган органик бирикмаларга карбон кислоталар дейилади.
Классификация
- 1. Тўйинган 2. Тўйинмаган 3. Ароматик
- Карбоксил гуруҳи сонига қараб
- 1. Бир асосли 2. Кўп асосли

С n H 2n+1 COOH ёки R-СООН
Умумий формуласи –
R=-Н: - СН 3 ; -С 2 Н 5 ва бошқа радикаллар
Номенклатура
Систематик номенклатура бўйича номлашда тегишли тўйинган углеводород номига кислота сўзи қўшиб ўқилади



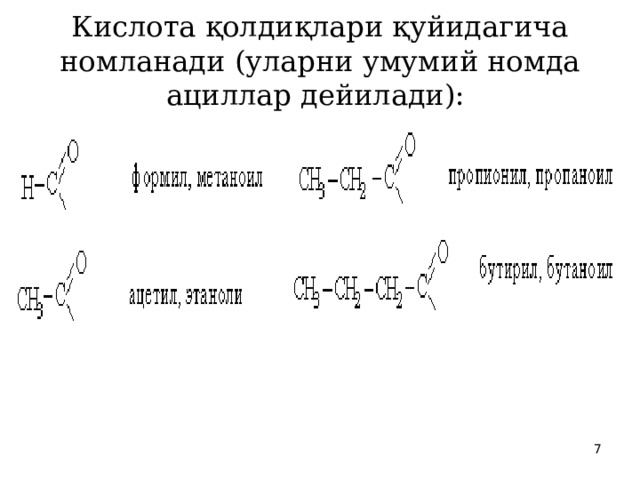
Кислота қолдиқлари қуйидагича номланади (уларни умумий номда ациллар дейилади):
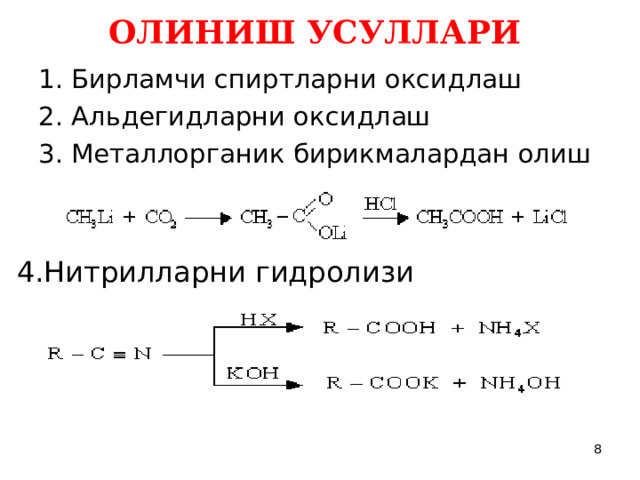
ОЛИНИШ УСУЛЛАРИ
1. Бирламчи спиртларни оксидлаш
2. Альдегидларни оксидлаш
3. Металлорганик бирикмалардан олиш
4.Нитрилларни гидролизи

5. Оксосинтез – энг истиқболли усул
6. Парафин углеводородларини юқори ҳароратда катализаторлар иштирокида ҳаво билан оксидлаб олиш
Бунда кичик молекуляр массага эга бўлган углеводородлар буғ фазада юқори босим остида
Катта молекуляр массага эга бўлган (С 16 Н 34 -С 30 Н 62 ) углеводородлар суюқ фазада 400-500 0 С ва 130-200 атм босим остида оксидланади.

7 . Ён занжирида битта углерод атомида 3 та галоген тутган углеводородларни гидролизи
8. Пропиленни оксидлаш орқали:
9. Акрилонитрини гидролизлаб:
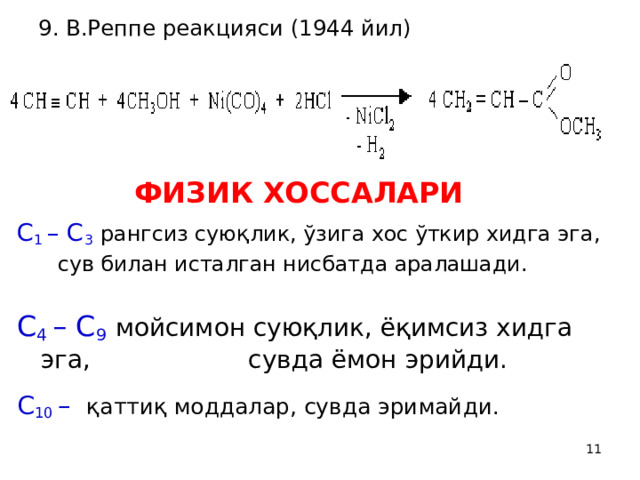
9. В.Реппе реакцияси (1944 йил)
ФИЗИК ХОССАЛАРИ
С 1 – C 3 рангсиз суюқлик, ўзига хос ўткир хидга эга , сув билан исталган нисбатда аралашади.
С 4 – C 9 мойсимон суюқлик, ёқимсиз хидга эга, сувда ёмон эрийди.
С 10 – қаттиқ моддалар, сувда эримайди.
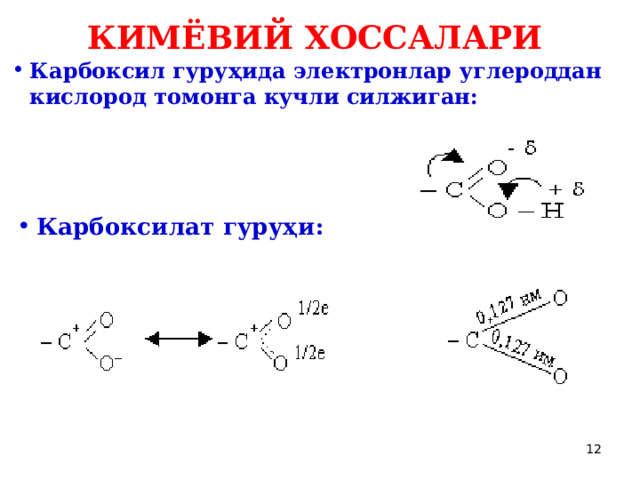
КИМЁВИЙ ХОССАЛАРИ
- Карбоксил гуруҳида электронлар углероддан кислород томонга кучли силжиган:
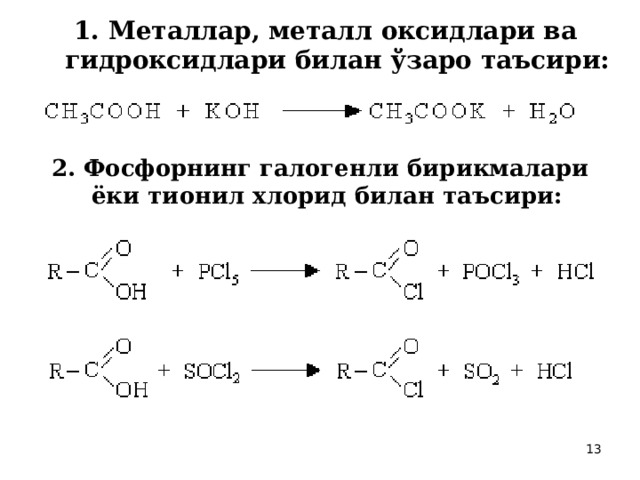
1. Металлар, металл оксидлари ва гидроксидлари билан ўзаро таъсири:
2. Фосфорнинг галогенли бирикмалари ёки тионил хлорид билан таъсири:
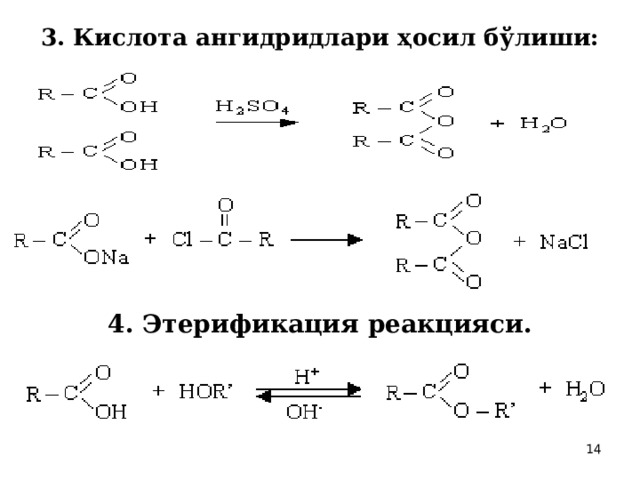
3. Кислота ангидридлари ҳосил бўлиши:
4. Этерификация реакцияси.
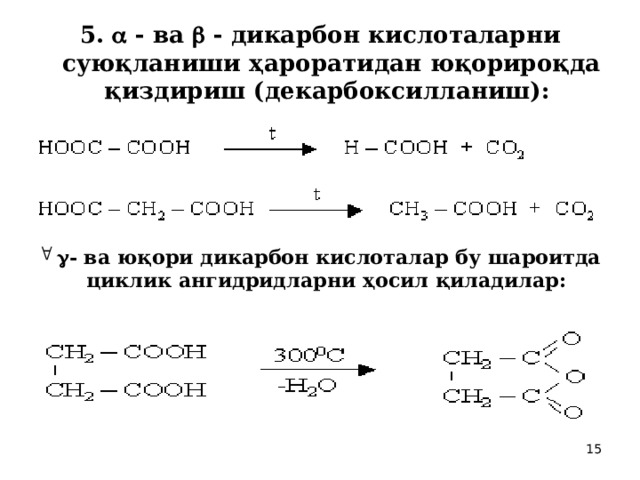
5. - ва - дикарбон кислоталарни суюқланиши ҳароратидан юқорироқда қиздириш (декарбоксилланиш):
- - ва юқори дикарбон кислоталар бу шароитда циклик ангидридларни ҳосил қиладилар:
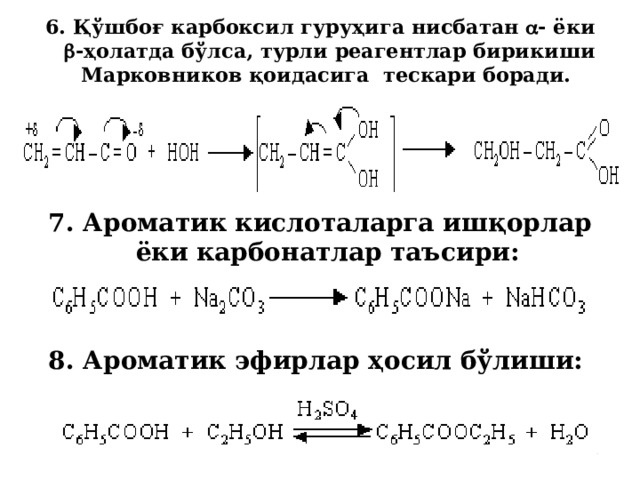
6. Қўшбоғ карбоксил гуруҳига нисбатан - ёки -ҳолатда бўлса, турли реагентлар бирикиши Марковников қоидасига тескари боради.
7. Ароматик кислоталарга ишқорлар ёки карбонатлар таъсири:
8 . Ароматик эфирлар ҳосил бўлиши:


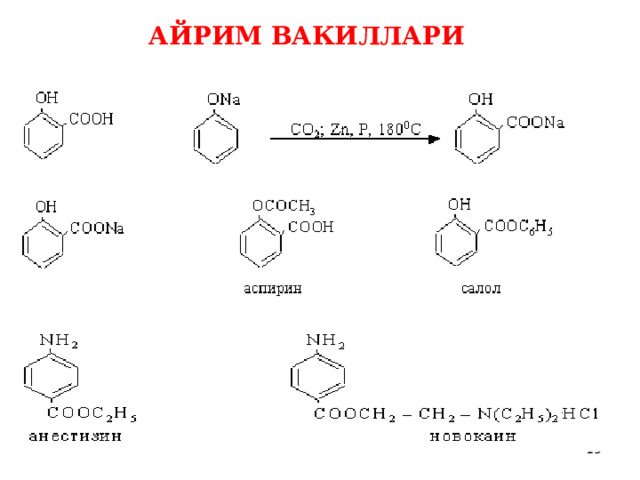
АЙРИМ ВАКИЛЛАРИ
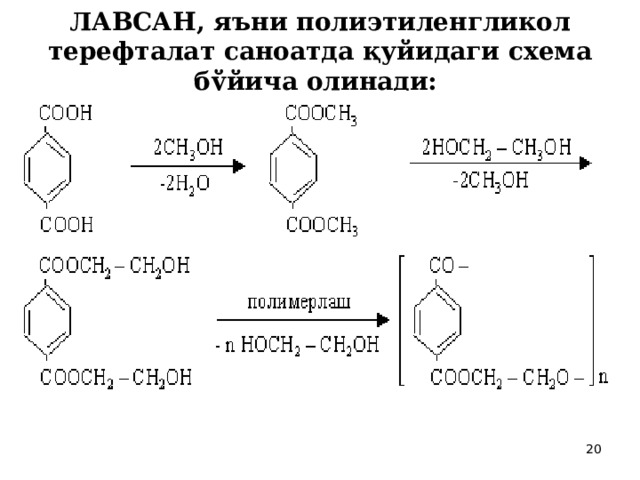
ЛАВСАН, яъни полиэтиленгликол терефталат саноатда қуйидаги схема бўйича олинади:
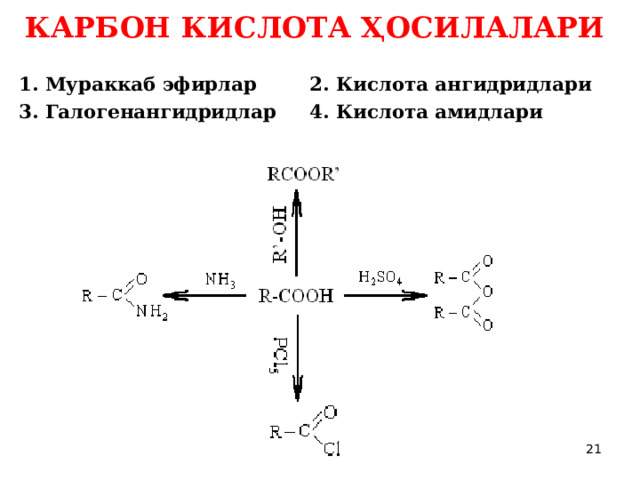
КАРБОН КИСЛОТА ҲОСИЛАЛАРИ
1. Мураккаб эфирлар 2. Кислота ангидридлари
3. Галогенангидридлар 4. Кислота амидлари

Мураккаб эфирлар мева эссенциялари олишда кенг ишлатилади:
- Этилформиат – ром ҳидини
- Этилбутират – ананас ҳидини
- Изоамилбутират – нок ҳидини
- Изовалериан кислота эфирлари – олма ҳидини
- Бензилацетат – жасмин ҳидини

Галогенангидридлар қуйидагича номланади.
ацетил хлорид, этаноил хлорид,
сирка кислота хлор ангидриди
бутирил хлорид, бутаноил хлорид
мой кислота хлор ангидриди
АЛОҲИДА ВАКИЛЛАРИ.
Чумоли кислота Н-СООН
100,8 0 С да қайнайдиган ўткир хидли суюқлик. Техникада ишқор ва углерод (II) оксиддан олинади:

Чумоли кислотанинг ўзига хос хусусиятлари
Сирка кислота
118,5 0 С да қайнайди, +16,6 0 да суюқланади, ўткир хидли суюқлик. Саноатда сирка альдегидини оксидлаб ёки метил спирти ва углерод (II) оксиддан синтез қилинади. Техникада сирка кислота полимерлар олишда, озиқ-овқат саноатида, синтетик толалар ишлаб чиқаришда кенг қўлланилган.

ИККИ АСОСЛИ КИСЛОТАЛАР

ОЛИНИШ УСУЛЛАРИ
1. Икки атомли спиртларни окидлаш:
2. Динитрилларни гидролизлаш:
3. Оксикислоталарни оксидлаш:
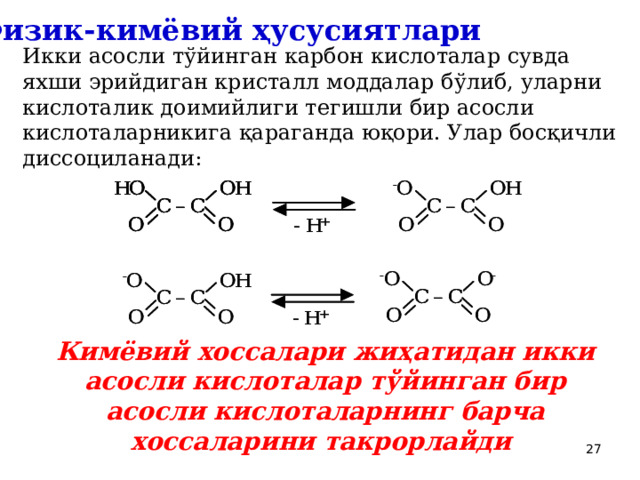
Физик-кимёвий ҳусусиятлари
Икки асосли тўйинган карбон кислоталар сувда яхши эрийдиган кристалл моддалар бўлиб, уларни кислоталик доимийлиги тегишли бир асосли кислоталарникига қараганда юқори. Улар босқичли диссоциланади:
Кимёвий хоссалари жиҳатидан икки асосли кислоталар тўйинган бир асосли кислоталарнинг барча хоссаларини такрорлайди
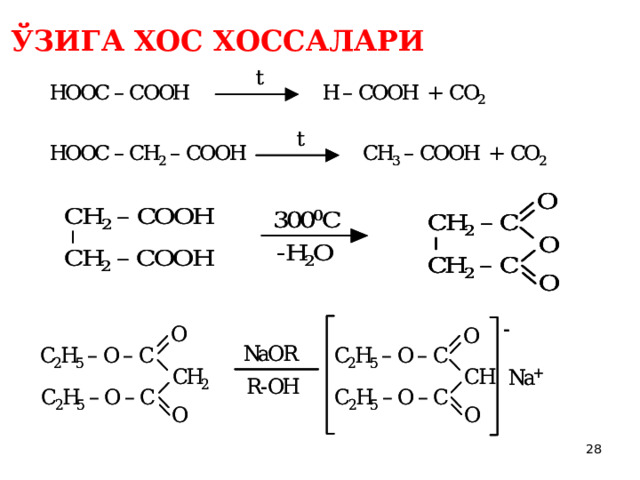
ЎЗИГА ХОС ХОССАЛАРИ

Аналитик кимёда, малон кислота турли қимматбахо бирикмаларни олишда, қахрабо кислота қишлоқ хўжалигида, адипин, себоцин кислоталар эса сунъий толалар ишлаб чиқаришда ишлатилади.





















































