Вариант 1
Часть 1 (выберите один верный ответ из четырех предложенных)
В атоме химического элемента, расположенного в 3 периоде, VI группе, главной подгруппе, заряд ядра равен
1) +3 2) +6 3) +16 4) +18
На трёх электронных слоях размещаются все электроны в атомах химических элементов
1) C и Cl 2) Mg и S 3) B и Al 4) P и N
Атом какого из указанных элементов имеет наибольший радиус?
1) кислорода 2) азота 3) лития 4) бериллия
В каком ряду химических элементов усиливаются неметаллические свойства соответствующих им простых веществ?
1) германий → кремний → углерод 3) барий → магний → кальций
2) литий → натрий → калий 4) кислород → азот → углерод
Ионная связь характерна для
1) S8 2) SO3 3) K2S 4) H2S
Какой вид химической связи в молекуле азота?
1) ковалентная неполярная 3) металлическая
2) ковалентная полярная 4) ионная
Кристаллическая решетка хлорида натрия
1) атомная 2) ионная 3) молекулярная 4) металлическая
Вещества, формулы которых СаO и СаCl2 являются соответственно
1) основным оксидом и основанием 3) амфотерным оксидом и кислотой
2) основным оксидом и солью 4) кислотой и основанием
Кислоте и соли этой кислоты соответствуют формулы веществ
1) H2SiO3 и CaSiO3 3) H2S и K2SO4
2) HNO2 и Al(NO3)3 4) H3PO3 и Na3PO4
Установите соответствие между схемой процесса, происходящего в окислительно-восстановительной реакции, и названием этого процесса: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА ПРОЦЕССА НАЗВАНИЕ ПРОЦЕССА
А) �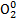 � → 2O–1 1) окисление
� → 2O–1 1) окисление
Б) Ba0 → Ba+2 2) восстановление
В) Br+5 → Br–1
Масса уксусной кислоты, содержащаяся в 0,5 л раствора её с массовой долей 80% (плотность 1,1 г/мл), равна
1) 480 г 2) 440 г 3) 160 г 4) 220 г
Часть 2 (дайте развернутый ответ)
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
HNO3 + Zn → Zn(NO3)2 + N2 + H2O
Определите окислитель и восстановитель.
Составьте молекулярное, полное и сокращенное ионное уравнение взаимодействия гидроксида алюминия и серной кислоты.
Сколько граммов 98%-ной серной кислоты надо добавить к 300 г воды, чтобы получить 10%-ный раствор кислоты? Ответ округлите до ближайшего целого числа.
Вариант 2
Часть 1 (выберите один верный ответ из четырех предложенных)
В атоме химического элемента, расположенного во 2 периоде, V группе, главной подгруппе, число электронов на внешнем уровне равно
1) 3 2) 5 3) 7 4)14
Одинаковое число электронов во внешнем электронном слое атома имеют элементы с порядковыми номерами
1) 6 и 14 2) 19 и 20 3) 7 и 17 4) 2 и 10
Электроотрицательность фосфора меньше, чем электроотрицательность
1) кремния 2) азота 3) алюминия 4) магния
Металлические свойства простых веществ усиливаются в ряду
1) магний → алюминий → кремний 3) алюминий → магний → натрий
2) литий → бериллий → бор 4) калий → натрий → литий
Ковалентную полярную связь имеет
1) О2 2) SO3 3) Сu 4)К2S
Какой вид химической связи в сульфиде натрия?
1) ионная 3) ковалентная полярная
2) металлическая 4) ковалентная неполярная
Металлическая кристаллическая решетка у
1) оксида цинка 2) воды 3) кислорода 4) магния
Вещества, формулы которых CO2 и Fe(OH)3, являются соответственно
1) основным оксидом и основанием 3) амфотерным оксидом и основанием,
2) амфотерным оксидом и солью 4) кислотным оксидом и амфотерным гидроксидом
Солью кремниевой кислоты и щёлочью соответственно являются
1) Na2SiO3 и Cа(OH)2 3) SiO2 и Na2SO4
2) H2SiO3 и Cu(OH)2 4) Na2SO3 и NaOH
Установите соответствие между схемой процесса, происходящего в окислительно-восстановительной реакции, и названием этого процесса: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА ПРОЦЕССА НАЗВАНИЕ ПРОЦЕССА
А) N–3 → N+2 1) окисление
Б) Cr+3 → Cr0 2) восстановление
В) �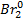 � → 2Br+5
� → 2Br+5
При растворении в 270 г воды сульфата калия был получен раствор с массовой долей соли 10%. Масса растворенного вещества равна
1) 30 г 2) 60 г 3) 45г 4) 50г
Часть 2 (дайте развернутый ответ)
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
NaOH + Br2 → NaBrO3 + NaBr + H2O
Определите окислитель и восстановитель.
Составьте молекулярное, полное и сокращенное ионное уравнение взаимодействия оксида железа (III) и соляной кислоты.
Вычислите массу 5%-го раствора вещества, который надо добавить к 120 г 30%-го раствора, чтобы получить 15%-й раствор. Ответ дайте в граммах с точностью до целых.

























