
Исследовательский проект «Углерод. Графит. Алмаз.»
8«А» класс МОУ «СОШ № 2 г.Ершова Саратовской области» Руководитель: учитель физики Филиппова Е.В.
Цели работы:
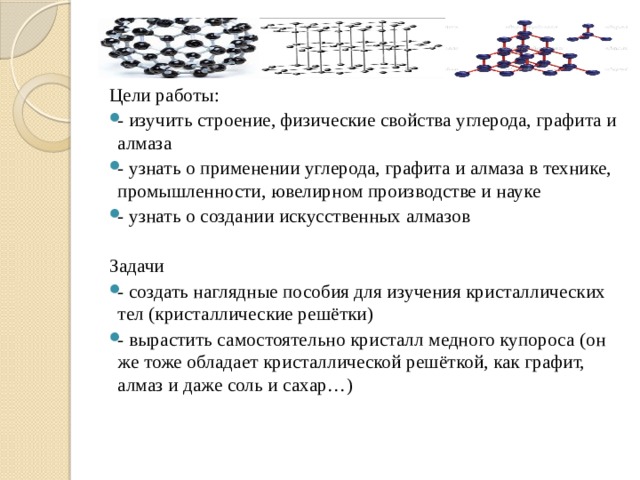
- - изучить строение, физические свойства углерода, графита и алмаза
- - узнать о применении углерода, графита и алмаза в технике, промышленности, ювелирном производстве и науке
- - узнать о создании искусственных алмазов
Задачи
- - создать наглядные пособия для изучения кристаллических тел (кристаллические решётки)
- - вырастить самостоятельно кристалл медного купороса (он же тоже обладает кристаллической решёткой, как графит, алмаз и даже соль и сахар…)
Разнообразие веществ, составляющих тело животных и растений, известно каждому. Воск и масло, скипидар и смола, хлопчатая бумага и белок, клеточная ткань растений и мускульная ткань животных, винная кислота и крахмал – все эти и множество иных веществ, входящих в ткани и соки растений и животных, представляют соединения углеродистые. Область соединений углерода так велика, что составляет особую отрасль химии, т.е. химии углеродистых или, лучше, углеводородистых соединений. Ни в одном из элементов такая способность к усложнению не развита в такой мере, как в углероде. Поныне нет основания для определения меры полимеризации угольной, графитной, алмазной молекулы, только можно думать, что в них содержится большое их количество. В молекулах белков – многие тысячи атомов. Там обязательно есть водород, кислород, азот; очень часто – сера. Но основа этих молекул – всегда углерод . И без углерода нет жизни, во всяком случае – на Земле. Этот газ преобладает и в атмосфере Марса. А вот в атмосферах Сатурна, Юпитера, Урана и Нептуна наряду с аммиаком доминирует иное соединение углерода – метан. Углерод обнаружен в составе метеоритов и комет. С помощью спектроскопических наблюдений углерод найден и на далеких звездах.

из графита изготавливают
- твёрдые смазочные материалы, в комбинированных жидких и пастообразных смазках - наполнитель пластмасс - замедлитель нейтронов в ядерных реакторах - компонент состава для изготовления стержней для чёрных графитовых карандашей (в смеси с каолином ) - для получения синтетических алмазов - для изготовления контактных щёток и токосъёмников для разнообразных электрических машин , электротранспорта и мостовых подъёмных кранов с троллейным питанием, мощных реостатов , а также прочих устройств, где требуется надёжный подвижный электрический контакт - как токопроводящий компонент высокоомных токопроводящих клеёв Многие аппараты химических производств, например, теплообменники.


Практическая часть
1. Изготовление моделей кристаллических решёток:
Оборудование и материалы:
Стальная проволока (вязальные спицы)
Пластилин
Пряжа различного цвета
Схемы построения кристаллических решёток алмаза, графита.

Практическая часть
Способы выращивания кристаллов:
1. Охлаждение насыщенного горячего раствора
2. Постепенное удаление воды из насыщенного раствора
3. Выращивание кристаллов из расплавленных веществ при медленном охлаждении жидкости.
2. Домашний эксперимент: Оборудование и материалы: Медный купорос Вода (лучше использовать дистиллированную воду или использовать обычную кипяченую воду) Стеклянный стакан или банка Нитка, тонкая проволока Палочка или обычный карандаш Бесцветный лак для ногтей Резиновые перчатки



Заключение
Алмаз
самый твердый минерал
Графит
бесцветный и прозрачный (бывают окрашенной формы, например розовые или черные, но встречаются редко)
очень мягкий
темно-серый, непрозрачный
плотность 3,5 г/см 3
проводит тепло
плотность 2,2 г/см 3
проводит тепло
не проводит электрический ток
проводит электрический ток
Алмаз и графит – это вещества с атомной кристаллической решеткой, где каждый атом связан со своими соседями очень прочными ковалентными связями, а весь кристалл в целом при желании можно считать огромной молекулой.

Иполь зуемая литература: 1. Банн Ч. Кристаллы. Их роль в природе и науке . М., «Мир», 1970 2.Китайгородский А.И. Порядок и беспорядок в мире атомов . М., «Наука», 1977 3.Шаскольская М.Л. Очерки о свойствах кристаллов . М., «Наука», 1978 4.Шаскольская М.Л. Кристаллы . М., «Наука», 1978 5.Харгиттаи И., Харгиттаи М. Симметрия глазами химика . М., «Мир», 1989 6.Ахметов Н.С. Неорганическая химия. Учеб. пособие для учащихся 8–9 кл. шк. с углуб. изучением химии. В 2-х частях – ч. 1, ч. 2, – 2-е изд. – М.: Просвещение, 1990 – 208 с. 7."Большая школьная энциклопедия", т. 2, изд. "Олма-пресс« Интернет-ресурсы http://n-t.ru/ri/ps/pb006.htm http://dic.academic.ru/dic.nsf/enc3p/168486 http://ru.wikipedia.org/wiki/Алмаз http://dic.academic.ru/dic.nsf/enc_geolog/151/Алмаз http://wiki.web.ru/images/2/22/Diamond_Cubic-F_lattice_animation.gif http://edu.ioffe.ru/register/?doc=efros/6.tex http://solidstate.karelia.ru/~materials/fi...t%201/1_1_2.htm http://www.astronet.ru/db/msg/1172686 http://ru.wikipedia.org/wiki/Графит http://www.nanoscopy.org/tutorial/graphite/graphite.html http://how-make.ru hobby-live.ru www.encycl.yandex, www.krugosvet, wwwrmika.
































