ОГБОУ СПО Ульяновский техникум приборостроения
Методическая разработка интегрированного учебного занятия по дисциплине
« Химия и биология»
Тема: «Белки»
|
|
| Работу выполнила: Анчикова Лариса Федеровна преподаватель химии и биологии |
г. Ульяновск
2015г
Тема урока: "Строение белков"
Тип учебного занятия: комбинированный
Цели занятия:
обучающие: сформировать у обучающихся знания о составе, строении, свойствах и функциях белка; умение устанавливать причинно-следственные связи строения и свойств.
развивающие: развитие умения сравнивать, обобщать, делать выводы; развитие логического мышления учащихся; развитие познавательного интереса учащихся, установление межпредметных связей; продолжить развитие навыков самообразования – работа с дополнительной литературой, работа в группе.
воспитывающие: совершенствовать коммуникативные качества обучающихся, способность к взаимодействию с сокурсниками, воспитание трудолюбия, настойчивости.
Содержание: знать: что является мономером белков; общую формулу; особенности структурной организации белка; физические и химические св-ва белков; функции белков; уметь: объяснять многообразие белков; отличать 4 структуры белка; объяснять св-ва белка, исходя из организации белка, строения белковой молекулы.
Формируемые общие компетенции: ОК2, ОК3, ОК5, ОК6.
Методы и приемы обучения: метод поисковой беседы, лабораторного эксперимента.
Формы организации познавательной деятельности: фронтальная, групповая.
Средства обучения:
Плакат: «Сроение белка», интерактивная доска (презентация: «Строение белка»),на доске: распечатка:(ощая формула аминокислоты, уравнение реакции образования трипептида, эпиграф урока: "Жизнь, есть способ существования белковых тел" - Ф. Энгельса, формула гемоглобина, схема пептидной связи), закрепление материала распечатки: опорный конспект урока, тест: «Строение белка», учебники, реактивы и оборудования для лабораторных опытов: раствор яичного белка, раствор соляной кислоты, сухой спирт, спички, этиловый спирт, ацетат свинца, молоко, лимон.
Разновидность: интегрированный урок по химии и биологии
Источники информации:
1.Рудзицис Г. Е. Химия. 10класс../Г. Е. Рудзитис, Ф. Г. Фельдман-М.: Просвещение, 2010-192с.
2. Константинов В. М. Общая биология для СПО/В. М. Константинов, А. Г. Резанов, Е. О. Фадеева-М.: «Академия», 2008-256с.
3. Органическая химия http://formula44.narod.ru/
4. Курс органической химии за 10 класс http://formula44.narod.ru
Конспект урока: Урок начинает учитель биологии I. Постановка цели урока. В Библии сказано: "Вначале было Слово". Современная книга о происхождении жизни по аналогии могла бы начинаться фразой "Вначале был белок". "Жизнь, есть способ существования белковых тел" - знакомая фраза Ф. Энгельса. Белки называют протеинами – это название подчёркивает первостепенную роль этих веществ (греч. «протео» - занимаю первое место) II. Виды белка. Первый белок, с которым мы знакомимся в своей жизни, это белок куриного яйца альбумин - хорошо растворим в воде, при нагревании свертывается, а при долгом хранении в тепле разрушается, яйцо протухает. Кератин (волосы, ногти, когти, шерсть, перья, копыта, наружный слой кожи ) не растворяется в воде, не свертывается, не разрушается в земле: рога древних животных сохраняются так же хорошо, как и кости. А белок пепсин, содержащийся в желудочном соке, способен разрушать другие белки, это процесс пищеварения. Белок интерферон применяется при лечении насморка и гриппа, т.к. убивает вызывающие эти болезни вирусы. А белок змеиного яда способен убивать человека. III. Содержание белка в организме. Если из организма животного удалить всю воду, то больше половины его сухой массы составляют различные белки. Чем сложнее организм, тем больше белков он содержит. В организме бактерии примерно 3-4 тыс. разных белков, а у млекопитающих - уже около 50 тысяч(
слайд 6). Каждый организм имеет собственный набор белков, то есть индивидуален. На Земле нет двух одинаковых людей по белковому веществу, за исключением однояйцовых близнецов. Как устроен белок? Естественно очень сложно. Некоторое представление о сложности белков дает формула гемоглобина С
3032Н
4816О
872N
780Fe
4 белка, придающего красный цвет крови и разносящий кислород по всему телу.(найти мол. массу ) Для того, чтобы запомнить основные сведения о строении белков, вам надо понять значение всего трех ключевых терминов и уметь разъяснять их значение.
- Белки - это макромолекулы(слайд 5). (найти мол массу гемоглобина)
- Белки - это биополимеры (жизнь, много, часть).
- Мономером белков являются аминокислоты. Известно много аминокислот, но в качестве мономеров любых природных белков известно только 20 аминокислот(слайд 11). Они получили название "волшебных", их список представлен в таблице из них может быть образовано 2 432 902 008 176 640 000 комбинаций (~2*1018)
Учитель химии: Аминокислоты-что это?
Общая формула:
H R O NH2 – аминогруппа
N – C – C R – радикал
H H OH COOH – карбоксильная группа
Как образуется белковая молекула?
Сначала образуется дипептид потом трипептид и т.д.(на доске показываю заранее распечатанными аминокислотами) Аминокислоты соединяются друг с другом в длинные цепочки с выделением воды, образуя белковую молекулу(реакция образования белка стр 156 Химия). Такая реакция называется реакцией поликонденсации(стр.140 Химия Габрилян 10кл)
(записываем)!!! она идет последовательно, путем образования дипептидов, трипептидов и полипептидов
(слайд17,18,19). Как называется связь? Соединение аминокислот происходит за счет пептидных связей
(слайд16). Пептидная(амидная)
O H
– С – N –
Учитель биологии (какие хим элементы входят в состав белка?) Состав белков(какие хим элементы входят в состав белка?)
(слайд 7,8) | W (C)=50-55%; | W (H)=6,3-6,7%; |
| W (O)=20-23%; | W (S)=0-2,5%; |
| W (N)=14-18%; | W (P)=0-2,5% |
Аминокислоты бывают:
1.заменимые аминокислоты - они могут синтезироваться в организме 2.незаменимые - в организме не образуются, их получают с пищей (лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, метионин)
(слайд9,10,11) Урок продолжает учитель химии.
Свойства аминокислот и белков Обратите внимание на структурные формулы аминокислот. Какие функциональные группы они содержат? Предположите, как они могут повлиять на белок?
(слайд 12,13 аминокисл) (26 слайд)свойства записываем!!! 1.Аминокислоты и соответственно белки являются амфотерными соединениями, обладают одновременно свойствами кислоты и основания(стр. 155 Химия реакции). 2.Качественная реакция на пептидную связь : биуретовая реакция Раствор белка +NaOH+CuSO
4= красно-фиолетовая окраска;
Раствор белка+ азотн. кислота(конц.)=жёлтое окрашивание
3.Гидролиз белка (при нагревании белков со щелочами или кислотами)-эта реакция с водой образуются аминокислоты---эта реакция ращепления белка которая происходит в организме(стр 161 Химия реакция)
Урок продолжает учитель биологии. Превращения белковой молекулы в организме Под влиянием ферментов происходит гидролиз белка(распад пептидных связей) Выдел Q Погл Q Выдел Q Белок-аминокислота-белок- CO2 , H2O, мочевина Классификация белков
(слайд 10) 1.Протеины или простые белки состоят только из аминокислот. 2.Протеиды или сложные белки кроме аминокислот в составе имеют небелковая часть 3.полноценные – содержат весь набор аминокислот 4.неполноценные – какие-то аминокислоты в них отсутствуют
Итак: белки это - макромолекулы, биополимеры, полипептиды. Белки - сложные органические соединения, состоящие из углерода, водорода, кислорода, азота, иногда серы и атомов металлов, мономерами которых являются аминокислоты.
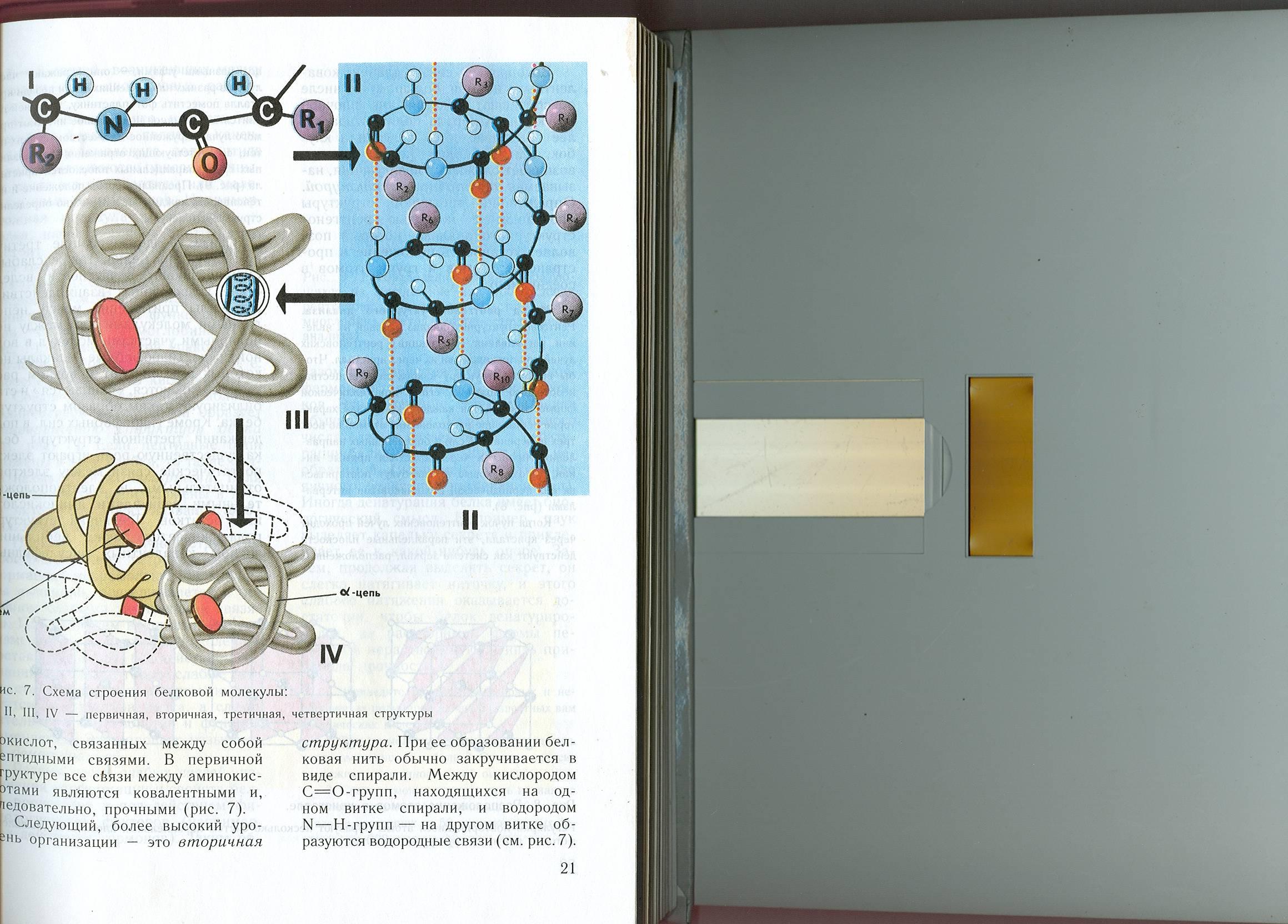
V. Структуры белка. Давайте рассмотрим на экране модели первичной, вторичной, третичной и четвертичной структуры белка
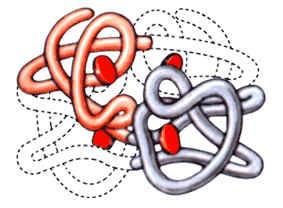
.(слайд20,21,22,23,24) Первичная - прямая цепочка из аминокислот, удерживается ковалентыми связями. Вторичная - скрученная в спираль первичная цепочка, удерживается водородными связями. Такую структуру имеют фибриллярные белки (коллаген, белок кожи; фибриноген, белок крови; миозин, белок мышц)). Третичная - многократно скрученная спираль, глобула, удерживается слабыми дисульфидными связями. Такую структуру имеют глобулярные белки (альбумины, глобулины). Некоторые белки имеют четвертичную структуру - объединение нескольких глобул. Четыре глобулы связаны атомом железа имеет белок гемоглобин.
(записываем)!!!
Самостоятельная работа. Моделирование структур белка. Ученики моделируют первичную, вторичную и третичную структуры белка, используя проволоку и набор бусин разных цветов.
Что необходимо сделать, чтобы получить четвертичную структуру? Ученики объединяются в группы, моделируя молекулы гемоглобина и инсулина. Вы сейчас разошлись на свои места. Что случилось с вашей белковой молекулой? (Распалась).Верно, это момент начала процесса денатурации, во время которого происходит разрушение структур белка. Ученики по группам моделируют процесс денатурации: 1 группа - разрушает третичную структуру, 2 группа - разрушает вторичную структуру. 3ья гр разрушает первичную структуру. Наблюдали ли вы в жизни процессы денатурации белков?
Урок продолжает учитель химии. Денатурация белка может происходить под влиянием различных факторов: температуры, кислоты, щелочи, солей и т.д. Давайте выясним влияние температуры, спирта, кислоты, солей тяжелых металлов на белок куриного яйца. Лабораторный опыт №1. Денатурация белков. 1. При нагревании пробирки с раствором яичного белка в ней появляются белые хлопья. 2. Действие спирта на белок. 3. При действии лимонной кислоты на молоко белок сворачивается.4.ацетат свинца+молоко а) денатурация белка соляной кислотой; б) спиртом в) осаждение белка ацетатом свинца (Обсудите результаты, сделайте вывод. Почему опасно отравление тяжелыми металлами? Обработка спиртом для обезараживания, укс. кислота для закрутки, кипечение.) Денатурация - это утрата белковой молекулой своей структурной организации При денатурации происходит как полное разрушение структур белка, так и частичное. Если первичная структура не разрушена, то может произойти восстановление остальных структур - этот процесс называется ренатурация(пример восстановление рибонуклеазы). Ренатурация - процесс восстановления структуры белка
Урок продолжает учитель биологии. Вы смоделировали процесс денатурации. У какой группы возможна ренатурация? У тех, кто не успел разобрать модель до отдельных бусинок. VI Функции белка Роль белков в природе(стр.10 старый уч. Биологии для СПО) 1. Строительная. 2. Каталитическая. 3. Двигательная. 4. Транспортная. 5. Защитная. 6. Энергетическая. Каждый учащийся внутри своей группы берет 2 функции белка, изучает. Затем, те кто изучал 1 и 2 собираются в группу сменного состава и обсуждают изученный материал. Учитель, если необходимо, помогает разобраться, проверяет. Каждый возвращается в свою группу, и уже внутри своей группы рассказывает, в чем заключается изученная роль белка. Таким образом, тема будет изучена всеми за меньший промежуток времени.
Вывод по роли белков: белки действительно выполняют многочисленные важные функции в клетках живых организмов. В настоящее время изучены структуры и свойства многих белков. Это даёт возможность синтезировать их в лабораторных условиях. Например, в 1954 году был синтезирован инсулин. Искусственный синтез белков может быть использован при лечении многих заболеваний человека, а также болезней обмена веществ.
Выводы по уроку (учащиеся записывают в тетрадь):
В ходе урока записать :
1.эпиграф("Жизнь, есть способ существования белковых тел" - Ф. Энгельс)
2. Белки - это макромолекулы(слайд 5). (найти мол массу гемоглобина) Белки - это биополимеры (жизнь, много, часть).
Мономером белков являются аминокислоты( их всего 20 шт.)
3.Общая формула аминокислоты
4.Образование белковой молекулы(стр.156)
5.Опред. поликонденсации(стр.140)
6. Состав белков:
| W (C)=50-55%; | W (H)=6,3-6,7%; |
| W (O)=20-23%; | W (S)=0-2,5%; |
| W (N)=14-18%; | W (P)=0-2,5% |
| 7. Аминокислоты бывают: 1.заменимые 2.незаменимые(8 шт.) |
|
белки это - макромолекулы, биополимеры, полипептиды. Белки - сложные органические соединения, состоящие из углерода, водорода, кислорода, азота, иногда серы и атомов металлов, мономерами которых являются аминокислоты( 20 шт.) Из них может быть образовано (~2*10
18) комбинаций
8.Белки бывают:
1.растворимые
2.нерастворимые
3.протеины (простые белки ), состоящие только из аминокислот,
4.протеиды(сложные) – содержащие небелковую часть
5.полноценные – содержат весь набор аминокислот
6.неполноценные – какие-то аминокислоты в них отсутствуют
9.Хим. Свойства белков:
1. амфотерные -обладают одновременно свойствами кислоты и основания(стр.155 уравнения реакции записать Химия Габрилян 10кл). 2.Качественная реакция на пептидную связь (цветные реакции) : биуретовая реакция Раствор белка +NaOH+CuSO
4= красно-фиолетовая окраска;
Раствор белка+ азотн. кислота(конц.)=жёлтое окрашивание
3.Гидролиз белка (при нагревании белков со щелочами или кислотами-эта реакция расщепления белка которая происходит в организме.
10.Структуры белка. Первичная - прямая цепочка из аминокислот, удерживается ковалентыми связями. Вторичная - скрученная в спираль первичная цепочка, удерживается водородными связями.
Третичная - многократно скрученная спираль(глобула), удерживается слабыми дисульфидными связями.
Четвертичная - объединение нескольких глобул.
11.Денатурация - это утрата белковой молекулой своей структурной организации. 12.Ренатурация - процесс восстановления структуры белка 13.Функции белка: 1. Строительная(в составе клеточных мембран и органоидов клетки). 2. Каталитическая (ферменты). 3. Двигательная(сократительные белки-они обуславливают сокращение мускулатуры животных, движение жгутиков, движение растений и др.) 4. Транспортная (способность белков крови обратимо соединятся с орг. и неорг. соединениями и доставлять их разные органы и ткани). 5. Защитная(антитела ,связывающие и обезвреживающие чужеродные вещества). 6. Энергетическая(при расщеплении выделяется энергия).
Домашнее задание. Сообщение по одной из предложенных тем. Проблема белкового голодания в 21 веке. Модифицированный белок: добро или зло? Искусственный белок.
Соевый белок, отношение к нему.
Закрепление изученного материала.
Опорный конспект для работы на уроке
1.Белки – это ------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
2. Мономеры белков - --------------------------------------------------------------------,
в составе которых --------------------------------------------------------------------------
![]()
![]()
![]()
-
3. Аминокислоты: заменимые и незаменимые (лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, метионин)
4. Структуры белков (уровни организации):
| Название структуры | Чем представлена структура | Какими связями поддерживается |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. 2.

3. 4.
Задание: По рисункам определить уровень организации --------------------------------------------------------------------------------------------------------------------------------------
5. Свойства белков:
а) растворимость
б) денатурация – это -----------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
ренатурация это -----------------------------------------------------------------------------
в) гидролиз белков (пример уравнения реакции) -----------------------------------------------------------------------------------------------------------------------------------------------
г) цветные реакции белков
| Название реакции | Реактивы | Какой процесс происходит |
|
|
|
|
|
|
|
|
д) амфотерность аминокислот (белков) – реакция с растворами кислот и щелочей
задание 1.
написать уравнение реакций аминоуксусной кислоты с раствором соляной кислоты и раствором гидроксида натрия;
------------------------------------------------------------------------------------------------------Написать схему образования биполярного иона ------------------------------------------------------------------------------------------------------------------------------------------------
Задание 2.
Написать уравнение реакции гидролиза трипептида глицил-аланил-глицина…
------------------------------------------------------------------------------------------------------
Тест «Строение белков»
1. Расположи химические элементы, входящие в состав белков в порядке убывания массовых долей?
а) углерод б) водород в) кислород г) сера д) фосфор е) азот
2. Сколько аминокислот участвуют в образовании белков?
а) 30 в) 20 б) 26 г) 10
3. Сколько аминокислот являются незаменимыми для человека?
а) 16 б) 10 в) 20 г) 8
4. Какие белки называются неполноценными?
а) в которых отсутствуют некоторые аминокислоты
б) в которых отсутствуют некоторые незаменимые аминокислоты
в) в которых отсутствуют некоторые заменимые аминокислоты
5. В результате какой реакции образуется пептидная связь?
а) реакция гидролиза в) реакция поликонденсации
б) реакция гидратации г) все вышеперечисленные реакции
6. Между какими группировками аминокислот образуется пептидная связь?
а) между карбоксильными группами соседних аминокислот
б) между аминогруппами соседних аминокислот
в) между аминогруппой одной аминокислоты и карбоксильной группой другой
7. Какие связи стабилизируют первичную, вторичную, третичную структуру? (Соотнесите)
а) ковалентные в) сульфидные мостики
б) водородные г) такие связи отсутствуют
8. Белки, состоящие только из аминокислот-это
1.протеиды 3.протеины
2.полноценные 4.неполноценные
9. Утрата белковой молекулой своей структурной организации-это
1.поликонденсация 3.денатурация
2.ренатурация 4.гидролиз





























