Муниципальное общеобразовательное учреждение средняя общеобразовательная школа села имени Героя Советского Союза Ивана Сергеевича Кошелева с.Лермонтово Белинского района Пензенской области
«Элементы в военном деле»
(интегрированный урок химии, литературы, истории, ОБЖ в 11 классе)
подготовила
учитель химии и биологии
Сорокина Виктория Николаевна
«Элементы в военном деле»
11 класс
Тип урока: комбинированный
Форма проведения: урок - исследование
Цели:
- развивать познавательный интерес, реализуя межпредметные связи курсов химии, истории, литературы, ОБЖ;
- развивать умение обучающихся логически мыслить, анализировать;
- расширение кругозора обучающихся, развитие умений работы в коллективе.
Задачи:
Образовательная: углубить и систематизировать знания о физических свойствах металлов, о месторождениях металлосодержащих руд и выявить значение металлов в военном деле.
Развивающая: продолжить формировать умения проводить параллели между различными областями наук; развивать познавательный интерес к предмету, реализуя межпредметные связи курсов химии, истории, литературы, ОБЖ, развивать навыки работы с географической картой, дополнительной литературой; анализировать, логически мыслить, собирать информацию, способствовать тренировке памяти.
Воспитательная: воспитывать в обучающихся чувство патриотизма, показать и подтвердить значение химических знаний для жизни.
Оборудование: Выставка «Металлы в военном деле», макет автомата, сапёрная лопата, гильзы, каска, макет машин, фляжка, граната, противогаз, карта «Великая Отечественная война», модели кристаллических решеток металлов, образцы металлов, коллекции руд, минералов и горных пород, компьютер, мультимедийный проектор, реактивы для демонстрации опытов.
План урока:
Организационный момент. Начало урока:
сообщение темы, задач, плана работы
2. Основная часть – формирование новых знаний
Вступительное слово учителя
Ориентировочно – мотивационный этап (основные понятия, подготовка к активной учебно – познавательной деятельности). В исследовании каждой из групп учителем созданы проблемные ситуации или поставлены проблемные вопросы.
Проблемно – поисковый этап (работа в группах, самостоятельное приобретение знаний учащимися).
Этап рефлексии (презентация полученных результатов)
Демонстрационный этап
3.Закрепление знаний – викторина «Металлы тоже воевали»
4. Итоги. Выводы.
5. Домашнее задание (дифференцированное).
Ход урока.
Эпиграф: «Не могу представить себе химика, незнакомого с высотами поэзии, с картинами живописи, с хорошей музыкой».
Пейзажи мирной жизни…(песня «Широка страна моя родная» стихи В. Лебедева – Кумача, музыка И.Дунаевского)

Учитель: Ребята, сегодня мы должны собрать всю информацию, которую знаем про металлы, в единое целое. Должны обсудить их свойства, месторождения и понять, каково значение химических элементов-металлов в истории Великой Отечественной войны, как помогали металлы ковать победу над фашистской Германией.
Железо.
В таблице Д.И.Менделеева трудно найти какой – либо иной элемент, с которым так неразрывно связывалась бы жизнь всего человечества.
Нет другого элемента при участии, которого проливалось бы так много крови, терялось бы столько жизней, происходило бы столько несчастий:
«Век девятнадцатый железный,
Воистину железный век,
Тобою в мрак ночной, беззвездный
Беспечный брошен человек».
А.Блок.
«Железные рудники доставляют человеку превосходнейшее и зловреднейшее орудие. Ибо этим орудием вспахиваем мы землю, сажаем кустарники, обрабатываем лозы с виноградом, вынуждаем их каждый год молодеть.
Но тем же самым железом производим битвы и грабежи и употребляем его не только вблизи, но и посылаем окрылённое вдаль, то из бойниц, то из мощных рук, то в виде оперенных стрел. Самое порочное ухищрение ума человеческого ибо, чтобы смерть поскорее постигла человека, сделали её крылатою и железу придали перья. Того ради да будет вина приписана человеку, а не природе.
А ведь Плиния – старшего испугало совсем уже безобидное, на наш взгляд оружие – мечи, копья, стрелы. Что бы он сказал, если бы увидел современные пушки и пулемёты, танки и крейсеры.
Но дело не в металлах, дело в том, что металлы используют люди. И как они их используют.
«Клинок уральский – восхищенье глаз:
В лазурном поле мчится конь крылатый,
Почтен неоценимою оплатой
Строй красоты, не знающий прикпас
Таков же, мастер, живой волшебный сказ –
Связуя вязью, тонкой и богатой,
Торжественно тревожный век ХХ
И быль веков, - обворожая нас.
Да будет это творческое слово,
Грядущему, являя мир былого
Оружьем столь же мощным на века,
Как эта сталь и как душа народа,
Как с ней одноимённая свобода –
Крылаты конь уральского клинка».
(Ю.Верховский)
Секрет булатных мечей.
Много столетий назад в Индии процветало искусство изготовления из стали мечей и кинжалов особой твёрдости с необычным узором, острых и тонких, как бритва, и гибких, как ветка ивы. С течением времени рецепты изготовления такой булатной стали были забыты.
Разгадать секрет производства булатов, объяснить чудесные свойства старинных дамасских клинков пыталось не одно поколение учёных 18-19 веков. Безуспешно занимался этой проблемой физик М.Фарадей. П.А.Аносову первому удалось открыть тайну булата. В течение 10 дней осуществлял тысячи экспериментов, исследуя влияние на качество стали кремния, марганца, хрома, углерода, алюминия, титана, алмаза, платины, золота. Эти опыты увенчались успехом, и Аносов получил сталь не уступающую по качеству прославленной дамасской, сочетающую изумительную твёрдость и невиданную упругость. На клинках из этой стали были необыкновенные узоры.
«Мне приснилась иная печаль
Про седую дамасскую сталь.
Я увидел, как сталь закалялась,
Как из юных рабов одного
Выбирали, кормили его,
Чтобы плоть его сил набиралась.
Выжидали положенный срок,
А потом раскалённый клинок
В мускулистую плоть погружали,
Вынимали готовый клинок.
Крепче стали не видел Восток,
Крепче стали и горче печали».
(Ю.Кузнецов)
Железо являлось основным металлом, из которого изготовляли многочисленные и разнообразные орудия для истребления людей.
Недаром копьё и щит, характерные принадлежности бога войны Марса, древние мудрецы сделали символом, обозначающим железо. Оно действительно верно и безотказно служило Марсу.
С изобретением огнестрельного оружия на изготовление пуль для ружей, пистолетов и картечи для артиллерии стали расходовать много свинца. (показывается кинофрагмент из учебного фильма «Великая Отечественная война», часть «Курская дуга».)
Ученик читает стихотворение Михаила Дудина «Разговор»:
«Труба и ракета сказали: «Отбой».
Замолкли орудия. Кончился бой.
Три друга склонились над другом своим,
Который на камне лежал недвижим.
Был первый моложе и тише других
И первый тревожно взглянул на двоих.
И голосом сломанным, из темноты:
«Я тоже погибну, товарищ, как ты».
И звёзды рассыпались над головой,
И голову поднял товарищ второй:
«За нами Россия – родимая мать,
Без слова готов за неё умирать».
Но третий спокойно сказал: «Не тужить,
Надо уметь побеждать и жить».
На службу войне были поставлены и другие металлы. В первой половине прошлого столетия никель добывался в небольших количествах и стоял очень дорого. Он считался, поэтому ювелирным металлом. Позднее никель стали добавлять в стальную броню. Долгие годы это было его основное применение. Однако позже он стал неотъемлемой составляющей бронированных орудий и танков. Вот что пишет С.Гагарин в произведении «Три лица Януса» о роли никеля в Отечественной войне.
На подводной лодке «Валькирия», исчезнувшей при загадочных обстоятельствах для германского командования, находилось 160 тонн никеля в слитках и монетах США и Канады.
Никель –серебристо – белый металл, значащийся в периодической системе Д.И.Менделеева под № 28, тугоплавкий, твёрдый, не изменяющийся на воздухе, - был такой же сложной проблемой для германии, как горючее, а может, и сложнее. Ведь горючее из нефти можно хоть чем – то заменить. Никель же незаменим. Без никеля нет брони. Без брони нет танков. Без танков нет победы на военных дорогах второй мировой войны.
Природа обделила Германию никелем. Незначительные запасы его есть в Рейнской долине. Основную часть никеля Германия получает из Канады.
Началась война, и канадский никель был потерян для Рейха. Гитлер захватил Грецию, а вместе с ней и никелевые рудники. Вассальная Финляндия открыла для немцев рудники на севере в районе Петсамо. Там работали заключённые и военнопленные. Целый эсэсовский корпус обеспечивал охрану рудников и гарантировал бесперебойную добычу красного колчедана и отправку его в Германию на металлургические заводы.
Когда советские танки Т – 34 появились на полях сражений, немецкие специалисты были поражены неуязвимостью их брони.
По приказу из Берлина первый же захваченный Т- 34 был доставлен в Германию. Здесь за него взялись химики. Они установили: русская броня содержит большой процент никеля, что делает её сверхпрочной. Недостаток никеля в стали привёл к тому, что к 1944 году имперские военные заводы вынуждены были изготовлять танковую броню повышенной толщины, и «тигры», и «пантеры», и «фердинанды», одетые в неё, оказывались тяжелее и слабее советских танков и самоходок».
В декабре 1944 года на окраине небольшого польского городка органами советской контрразведки была задержана подозрительная женщина, которая «теряла» у колонны машин с боеприпасами «автоматические ручки». При проверке было установлено, что это диверсионное зажигательное средство со сложным воспламенителем, с корпусом из сплава, имеющего в основе алюминий. Из этого сплава изготавливают и корпуса зажигательных бомб.Алюминиевые соли органических кислот составляют основу «напалма», применявшегося американскими войсками в войне с Южным Вьетнамом, португальскими колонизаторами в Анголе. Так алюминий был поставлен на службу в войне.
В книге А.Валентинова «Металла огненный поток» есть такой занимательный рассказ. «В один из морозных зимних дней на петербургском складе военного обмундирования царила паника. Складской сторож, отставной солдат, доживающий свой век «при должности», обалдело привалился к штабелю ящиков и тупо глядел перед собой пустыми глазами. Даже его холённые бакенбарды и те обвисли, вытянулись грустными сосульками и сильно смахивали на банную мочалку, небрежно приклеенную к помертвевшему лицу.
Неподалёку пять или шесть чиновников военного ведомства столпились вокруг открытых ящиков и, забыв про респектабельность, возбужденно размахивали руками. Да и было, отчего прийти в волнение: на складе пропали…пуговицы. Да, да, блестящие оловянные солдатские пуговицы таинственным образом исчезли из ящиков. Мало того, что государству нанесён убыток, поскольку олово стоит немало, но сам факт случившегося внушал тревогу: сегодня злоумышленник похитил пуговицы, а завтра, глядишь, и оружие заберёт.
А этот злоумышленник оказался очень уж нахальным. Мало того, что выгреб все пуговицы, он ещё, словно в насмешку, насыпал в ящики какой – то серый порошок. Нет, это был явно опасный тип. А олух – сторож имеет наглость уверять, что караулил исправно и не допускал к дверям склада никого из посторонних. И как теперь докладывать генералу, начальнику департамента, который потребует немедленно изловить похитителя?
История не донесла до нас, как вышли чиновники из этого положения и какое наказание понёс сторож. Случай с пуговицами наделал много шума, но постепенно о нём забыли. И вспомнили только почти через сто лет, когда весь мир был потрясён трагической гибелью экспедиции англичанина Роберта Скотта.
Когда причины гибели экспедиции Скотта стали известны, вспомнили и историю с пуговицами».
Дело в том, что при низкой температуре атомы олова перестраивают свою кристаллическую решётку и металл разрушается, «заболевает». Название этой болезни – оловянная чума. Солдатские пуговицы нельзя хранить на морозе. Металлы олово и медь образуют сплав – бронзу. Из бронзы во всём мире изготавливают памятники воинам.
В Трептов – парке в г.Берлине и памятника воинам Советской Армии, павшим при штурме столицы фашистской Германии, отлиты пять огромных (до пяти метров в диаметре) бронзовых венков, лежащих на братских могилах. Там же в мемориальном зале Мавзолея воинам Советской Армии на постаменте из чёрного лабрадора в золотом ларце хранится книга с именами героев павших смертью храбрых при героическом штурме столицы Германии.
Учащиеся читают стихи Михаила Дудина «Благословенный полдень»:
«Благословенный полдень,
Весь мир в цвету. Они прошли вперёд.
Я видел лица, блеск военной стали,
На гимнастёрках звонкие медали,
На тёмных касках пуль тяжёлый след,
Литого солнца золотая рассыпь,
И этот шаг – торжественную поступь.
Воистину, и равных в мире нет».
Для ведения войн были необходимы не только железо, никель, алюминий, но и золото, много золота.
Стихи о золотой пыли:
«На шумной площади, взобравшись на скамью,
Какой – то шарлатан румянорожий
Взывает к публике прохожей:
Я средство от всех болезней продаю!
Вот порошок неслыханного свойства:
Он придаёт ума глупцу,
Честь – подлецу,
Трусливому – геройство…
Его влиянью нет предела и границ,
Всего поможет вам достичь он,
Перед ним всё клониться, всё упадает ниц…
Он в полном смысле энциклопедичен!
Я подошёл и заглянул в бутыль –
Простая золотая пыль».
В 1918 году Германия должна была уплатить победителям с каждой «немецкой души» 3000 долларов золотом.
Войско Александра Великого, более известного под именем Македонского двигалось с боями по странам Азии. Как только войска вступили на территорию Индии, среди воинов начались тяжёлые желудочно – кишечные заболевания.
После ряда кровопролитных сражений и пышно отпразднованных побед весной 326 года Александр вышел к берегам Инда. Однако победить своего врага – «непобедимое» войско Александра не могло. Воины, истощённые и обессиленные отказались идти вперёд к берегам Ганга, куда влекла Македонского жажда завоеваний. Осенью 326 года войска начали отступление.
Сохранившиеся описания истории походов Македонского показывают, что рядовые воины болели чаще, чем военачальники. Через 2250 лет причина заболеваемости воинов была найдена. Она заключалась в разности снаряжения: рядовому воину полагался оловянный бокал, а военачальнику – серебряный.
Серебро, растворяясь в воде, убивает бактерии. Это свойство серебра использовали ещё раньше жители Египта для лечения открытых ран: на раны накладывали серебряные пластинки.
В ходе обсуждения физических свойств, учащиеся обращаются к образцам металлов на демонстрационном столе, плакатам, моделям кристаллических решеток.
Вопрос учителя: «О каком металле идет речь?»
Учитель начинает, корректирует, направляет, обучающиеся дополняют своим материалом.
Учитель. Немцы разрушили в СССР почти 32000 промышленных предприятий, 4100 железнодорожных станций, 40000 больниц, 84000 школ, техникумов и ВУЗов, 43000 библиотек. Полностью или частично разрушено и сожжено 1710 городов и более 70000 сел и деревень…
Враг сеял смерть…
В разрывах даль…
Страна пожарами объята…
В сердцах и ярость, и печаль…
Но гас огонь и гнулась сталь
О волю русского солдата.
Выпуск химической продукции к концу войны приблизился к довоенному уровню, а в 1945 году он достиг 92% от уровня 1940 года.
Учитель: И, конечно же, Великая победа это заслуга не только металлов. Не нужно забывать людей, которые впервые применили эти металлы и добились введения в производство изделий из их сплавов.
Проецируется на экран:
Бериллиевая бронза (сплав меди и 1–2,5% Ве с добавками 0,2–0,5% Ni и Со) используется в самолетостроении. А сплав Ве, Mg, Al, Ti необходим в создании ракет и скорострельных авиационных пулеметов, впервые примененных в годы войны.
На основе Mg и Al изготовлялись прочные и сверхлегкие сплавы для самолетостроения.
Сплав титана (до 88%) с другими металлами идет на изготовление танковой брони. Состав брони у этого танка был такой, что его не могли пробить фашистские снаряды. Титан применяют также в радиотехнике.
Хромовые стали нужны для изготовления огнестрельных орудий, корпусов подводных лодок.
Более 90% всех металлов, которые использовались в Великой Отечественной войне, приходилось на железо.
К обальтовая сталь использовалась для изготовления магнитных мин.
обальтовая сталь использовалась для изготовления магнитных мин.
Дульнозарядный миномет и мина Сплав Cu (90%) и Sn (10%) – пушечный металл. Сплав Cu (68%) и Zn (32%) – латунь – использовали для изготовления артиллерийских снарядов и патронов.
Без германия не было бы радиолокаторов.
Тантал – важнейший стратегический материл для изготовления радарных установок, передаточных радиостанций.
Из вольфрамовых сталей и сплавов изготавливают танковую броню, оболочки торпед и снарядов.
Учитель:
Ученые-химики создавали новые способы производства взрывчатых веществ, топлива для реактивных снарядов “Катюш”, высокооктановых бензинов, каучука, материалов для изготовления броневой стали, легких сплавов для авиации, лекарственных препаратов.
Это химики Александр Евгеньевич Ферсман, Александр Николаевич Несмеянов, Николай Дмитриевич Зелинский и другие. (Демонстрация фотографий ученых – см. приложение)
Памяти химиков–фронтовиков посвятил свое стихотворение старший преподаватель ДХТИ, бывший фронтовик З.И. Барсуков:
Кто про химика сказал: “Мало воевал”,
Кто сказал: “Он мало крови проливал?”
Я в свидетели зову химиков–друзей, -
Тех, кто смело бил врага до последних дней,
Тех, кто с армией родной шел в одном строю,
Тех, кто грудью защитил Родину мою.
Сколько пройдено дорог, фронтовых путей…
Сколько полегло на них молодых парней…
Не померкнет никогда память о войне,
Слава химикам живым, павшим - честь вдвойне.
Элементы – неметаллы.
В первую мировую войну 22 апреля 1915 года хлор применили как оружие массового уничтожения на западном фронте недалеко от бельгийского города Ипра против англо – французских войск.
Вскоре для той же цели был применён другой удушающий газ – фосген – соединение хлора с оксидом углерода. В 1917 году массовое применение нашёл иприт, который тоже содержал хлор. К концу войны было разработано более 50 различных боевых отравляющих веществ, 95 % которых были производными хлора.
Чтобы судить о действии отправляющих веществ на организм человека, достаточно указать, только английской армии, занимавшей среди воюющих государств пятое место по численности, они вывели из строя с июля 1917 г. по ноябрь 1918 г. более 160000 человек.
Зачитывается отрывок из романа М.Шолохова «Тихий Дон», где описывается зелёно – жёлтый газ, являющийся убийцей многих тысяч людей.
«На рассвете 3 октября немцы, употребив удушливые газы отравили три батальона 256 – го полка и заняли первую линию наших окопов…
Валет, клацнув зубами, отпрыгнул, и на место, где секунду назад стояли его ноги, спиленным деревом упал стоявший под сосной человек. Они перевернули его лицом вверх и тут только догадались, что под сосной нашёл себе последний приют этот отравленный газами, бежавший от смерти, которую нёс в своих лёгких, солдат одного из трёх батальонов 265 – го пехотного полка. Рослый, широкоплечий парень, он лежал вольно откинув голову с лицом, измазанным при падении клейкой грязью, с изъеденными газом, разжиженными глазами, из стиснутых зубов его чёрным глянцевидным бруском торчал пухлый, мясистый язык.
- Пойдём. Пойдём ради бога! Пусть он себе лежит, - шепнул товарищ, дёргая Валета за руку».
(Показывается фрагмент из учебного фильма об отравляющих веществах).
Академик Н.Д.Зелинский, выдающийся химик, изобрёл противогаз, действующий по принципу адсорбции. Это произошло в 1915 году. Использование угольного противогаза целиком освобождало вдыхаемый воздух от ядовитых примесей.
В настоящее время древесный уголь, сохранивший в былых войнах миллионы людей от ужасных мучений и смерти, в знак благодарности демонстрируется на музейных стендах.
Обучающиеся слушают отрывок из произведения Э.М.Ремарка «На западном фронте без перемен».
«Глухие хлопки химических снарядов смешивались с грохотом разрывов. Между разрывами слышно гудение набатного колокола: гонги и металлические трещотки возвещают далеко вокруг: «Газ, газ, газ!»
В эти первые минуты решается вопрос жизни и смерти: герметична ли маска?
Я помню страшные картины в лазарете: отравленные газом, которые ещё несколько долгих дней умирают от удушья и рвоты, по кусочкам отхаркивая перегоревшие лёгкие.
Я дышу осторожно, прижав губы к клапану…
Моя голова в противогазе звенит и гудит, она, кажется, вот – вот лопнет. Лёгкие работают с большой нагрузкой, им приходится вдыхать всё тот самый горячий, уже не раз побывавший в них воздух, вены на висках вздуваются. Ещё немного, и я, наверно, задохнусь.
…Ветер разогнал, воздух чист. Тогда м я тоже с хрипом срываю с себя маску и падаю. Воздух хлынул мне в грудь, как холодная вода, глаза вылезают из орбит, какая – то тёмная волна захлёстывает меня и гасит сознание».
В этом же романе говорится о том, что отравляющий газ особенно долго держится у земли. «Увидав наверху людей без противогазов, они (солдаты в воронке) тоже сняли свои маски и успели глотнуть достаточно газа, чтобы сжечь себе лёгкие. Сейчас их состояние безнадёжно, они умирают медленной, мучительной смертью от кровохарканья и приступов удушья».
Константин Паустовский в одном из своих рассказов описывает, как белогвардейцы пытались уничтожить партизан, скрывавшихся в керченских каменоломных. Заливая по трубам в шахты серную кислоту, они вызывали реакцию выделения углерода кислого газа, который при концентрации свыше 4% вызывает отравление, нарушение двигательных и речевых функций, а при концентрации свыше 10 % - смерть от паралича дыхательного центра.
Специальными опытами было установлено, что кусочки фосфора загораются на воздухе при 40 градусах, а порошок, образующийся после испарения растворителей, - 0 градусов. Это свойство фосфора и привлекло внимание военных. Во время второй мировой войны немцы применили против англичан «бомбы – листочки» для поджигания хлебов на корню, сельских построек, лесов. Такие же бесшумные диверсионные устройства сбрасывались на мирные города и сёла Кореи, Индонезии, Кубы.
Вся «бомба» представляет собой целлулоидную пластинку размером 10х15 см., в центре которой укреплена таблетка белого фосфора, прикрытая мокрой ватой. Хранят и перевозят их в банках с водой. Во время падения вода испаряется, и «бомба» загорается. Горение продолжается около одной минуты.
Раствор белого фосфора в сероуглероде и скипидаре применяется в огнемётах.
На вооружении американской армии имеются фосфорные снаряды, содержащие до 7 кг. белого фосфора, и дымовые мины с таким же зарядом.
Во время второй мировой войны использовались зажигательные бутылки (раствор белого фосфора в сероуглероде). Подобные бутылки использовались в Анголе и Южном Вьетнаме.
В «Повести временных лет» - летописном своде событий, составленном в Киеве, - описание похода князя Игоря заканчивается словами очевидцев: «Словно молнию… которая на небе, греки имеют у себя и пускали её, сжигая нас, поэтому мы и не одолели их». Дружинники князя защищались от «греческого огня» мокрыми воловьими шкурами, кожаными щитами, но терпели поражение. Горящая смесь выбрасывалась греками через медные трубы, установленные на бортах византийских кораблей. Состав этой смеси греки держали в тайне.
Предполагают, что в неё входили сера, нефть, горючие масла, смола, селитра, клей и вещества для окраски пламени. Погасить этот состав водой было трудно.
Хотелось бы надеяться, что мощь этой прекрасной науки – химии – будет направлена не на создание новых видов оружия, не на разработку новых отравляющих веществ, а на решение глобальных общечеловеческих проблем.
Завершаем урок мы символическим салютом в честь тех, кто ковал победу на полях сражений и в тылу. (Звучит песня “День Победы” – фоном).
Учащиеся показывают опыт “салют”. (Приложение)
В конце урока предлагается провести тест “Немного о металлах и неметаллах”
1. Какой металл добавляется в сталь для придания танкам Т – 34 особой прочности брони?
А) марганец; б)никель; в)хром
2. Копьё и щит – это символы, обозначающие:
А)медь; б)золото; в)железо
3. Какой металл придаёт ума глупцу, честь подлецу, трусливому геройство?
А)серебро; б)платина; в)золото
4. Пули для ружей и пистолетов изготавливают из:
А)свинца; б)железа; в)меди
5. Если верить древнему историку, то во времена похода Александра Македонского в Индию офицеры его армии гораздо реже болели желудочно – кишечными заболеваниями, чем солдаты. Еда и питьё у них были одинаковыми, но вот посуда разная. Посуда для офицеров была изготовлена из:
А)олова; б)серебра; в)меди
6. Какой металл А.Б.Ферсман назвал «металлом консервной банки»?
А)железо; б)олово; в)алюминий
7. Какой металл может болеть «чумой»?
А)олово; б)свинец; в)железо
8. К.Паустовский в одном из своих рассказов описывает, как белогвардейцы пытались уничтожить партизан, применяя:
А)оксид углерода (II); б)оксид углерода (IV); в)оксид серы (IV)
9. Кусочки фосфора загораются при температуре:
А)20; б)30; в) 40
10. Автоматические ручки – это «диверсионные» зажигательные устройства, содержащие:
А)алюминий; б)олово; в)натрий
Ответы: 1-б; 2-в; 3-в; 4-а; 5-б; 6-б; 7-а; 8-б; 9-в; 10-а.
Обучающиеся пишут ответы в двух экземплярах: один сдают учителю, а второй оставляют у себя, сверяют с ответами на доске, и сразу оценивают свой тест.
Подведение итогов работы на уроке (положительную оценку получает каждый ученик).
Выводы.
Сегодня на уроке мы с вами охватили только часть материала о великой роли химии, в том числе металлов и неметаллов для победы в Великой Отечественной войне. Немаловажную роль в исходе войны сыграли не столько сами металлы и неметаллы, сколько знания людей об их свойствах, применении этих свойств на практике. Это ещё раз доказывает огромную важность и значимость химических знаний для жизни, ведь химия по сути своей это и есть – жизнь. И только от людей зависит, будет она разрушать или созидать.
Д/З: параграф, написать соответствующие реакции и расставить коэффициенты.
Приложение №1
Опыт «Салют»
Оборудование: железный тигель, штатив с кольцом, фарфоровый треугольник, спиртовка, лист бумаги, стеклянная палочка, порошки железа и древесного угля, сухой мелкокристаллический перманганат калия.
На чистом листе бумаги (или на стекле) тщательно смешиваем стеклянной палочкой или шпателем равные количества (примерно по 1-2 чайной ложки) порошков железа, древесного угля и перманганата калия. Полученную смесь переносим в железный тигель, закрепленный в фарфоровом треугольнике, который находится на кольце штатива. Нагреваем тигель в пламени спиртовки. Через некоторое время из тигля начинают разлетаться раскаленные частички железа в виде снопа искр. С появлением искр спиртовку следует поставить. (Опыт эффективнее проводить в затемненном помещении).
Опыт «фейерверк»: жёлтый цвет – бертолетова соль 2г, 1г серы, 1г безводной соды; зелёный цвет – 3,5 г бертолетовой соли, 1 г серы, 1,5 г карбоната бария; красный цвет – 2 г бертолетовой соли, 5,5 г серы, 0,5 г угля (в порошке) и 17 г нитрата стронция.
Опыт «Салют -2»: в чистые фарфоровые чашки наливаем по 5 мл этилового спирта. В спирт добавляем по 1 г мелкорастёртых хлоридов натрия, калия, лития, бария. Смеси поджигаем. Гамму цветов можно разнообразить, используя другие соли.
Приложение №2
Что называют металлами?
Металлами называют вещества с определенным набором физических и химических свойств. Понятия “металл” применяют к двум разным объектам: к химическому веществу и химическому элементу.
В каком виде встречаются металлы в природе?
(В виде руд, в самородном виде.) В свободном состоянии в природе встречаются только некоторые металлы: золото, платина, палладий, родий. Большинство металлов встречаются в природе в виде соединений: оксидов, сульфидов, хлоридов, сульфатов и т.д
- Приведите примеры руд, содержащих металлы (Хромовые -1, железная-2, марганцовая-3, никелевая-4, вольфрамовая-5, молибденовая-6, оловянная-7, алюминиевая-8, медная-9, ртутная-10.)
- Приведите пример металла, встречающегося в самородном виде, и найдите соответствие с условными знаками на доске. (Золото – 11.)
- Какие месторождения металлосодержащих руд были выявлены за годы Великой Отечественной войны?
На физической карте России отмечают условными знаками месторождения полезных ископаемых, работа с коллекциями.
Оловянные месторождения на Дальнем Востоке.
Свинцовые – в Средней Азии.
Вольфрамовые – в Кузнецком Алатау и на Алтае, в Средне Азии.
Медные – на Среднем Урале.
Молибден – к северу от озера Балхаш.
Источники редких металлов – лития, молибдена, ванадия – Казахстан.
Руды кобальта, необия, алюминиевые – Уральские горы.
Приложение №3
- Почти все химические элементы таблицы Д.И.Менделеева принесли пользу Родине. Немаловажна роль металлов.
- Физические свойства металлов
Наиболее важными физическими свойствами металлов являются тепло- и электропроводимость. Характерной особенностью металлов является металлический блеск, что связано с их способностью отражать свет. Все металлы, кроме ртути, при обычной температуре твердые вещества.
Характерные свойства металлов – ковкость и тягучесть. Наибольшей ковкостью обладают золото, серебро, медь, а наименьшей – марганец.
По температуре плавления металлы сильно отличаются друг от друга: температура плавления ртути – 39о С, температура плавления вольфрама – 3370о С.
1. Агрегатное состояние. В основном, все твердые вещества, имеют металлическую кристаллическую решетку. Исключение, ртуть – жидкая.
2. Температуры кипения и плавления разнообразны. Температура плавления ртути – 39 градусов Цельсия, галлия – 29,8 (плавится в руках), у цезия – 28, вольфрам – 3390 градусов Цельсия, это самый тугоплавкий металл, используется в нитях электроламп.
3. Твердость. Самые мягкие – щелочные металлы и свинец, режутся ножом. Самый твердый – хром, царапает стекло.
4. Плотность. Литий – самый легкий металл, осмий – самый тяжелый. Плотность легких металлов ниже 5 г/см.куб, тяжелых – больше 5.
5. Электропроводность и теплопроводность. Благодаря свободным электронам, в кристаллической решетке металлы проводят электрический ток. Самые лучшие проводники – серебро, медь, золото, алюминий, железо. Худшие проводники – ртуть, свинец, вольфрам. Теплопроводность соответствует электропроводности.
6. Ковкость, пластичность, прочность. При механическом воздействии происходит смещение слоев атомов, благодаря свободным электронам, разрыва связей не происходит. Высокая пластичность у золота, серебра, меди, олова, железа, алюминия.
7. Металлический блеск, серый цвет, непрозрачность.
Приложение № 4. к индивидуальным д/з.
Вспомним начало войны, 1941 г. в два дня на одном из военных заводов был налажен выпуск бутылок КС (Качурина–Солодовникова), или просто бутылок с горючей смесью. Это незамысловатое химическое устройство уничтожало немецкую технику не только в начале войны, но и даже весной 1945 г. – в Берлине.
Что представляли собой бутылки КС? К обыкновенной бутылке прикреплялись резинкой ампулы, содержащие концентрированную серную кислоту, бертолетову соль, сахарную пудру. (Демонстрация модели бутылки.) В бутылку заливали бензин, керосин или масло. Как только такая бутылка при ударе разбивалась о броню, компоненты запала вступали в химическую реакцию, происходила сильная вспышка, и горючее воспламенялось.
Реакции, иллюстрирующие действие запала (на экран проецируются уравнения реакций):
3KClO3 + H2SO4 = 2ClO2 + KСlO4 + K2SO4 + H2O,
2ClO2 = Cl2 + 2O2,
C12H22O11 + 12O2 = 12CO2 + 11H2O.
Три компонента запала берутся в отдельности, их нельзя смешивать заранее, т.к. получается взрывоопасная смесь.
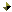
Многие наши сверстники в военные годы во время налетов дежурили на крышах домов, тушили зажигательные бомбы. Начинкой таких бомб была смесь порошков Al, Mg и оксида железа, детонатором служила гремучая ртуть. При ударе бомбы о крышу срабатывал детонатор, воспламенявший зажигательный состав, и все вокруг начинало гореть. На экране приведены уравнения реакций, происходящих при взрыве бомбы:
4Al + 3O2 = 2Al2O3,
2Mg + O2 = 2MgO,
3Fe3O4 + 8Al = 9Fe + 4Al2O3.
Горящий зажигательный состав нельзя потушить водой, т.к. раскаленный магний реагирует с водой:
Mg + 2Н2O = Mg(ОН)2 + Н2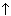 .
.
Вывод: тушить водой нельзя, т.к. раскаленный магний выделяет водород, который может при горении взорваться.
Во время ночных налетов для освещения цели бомбардировщики сбрасывали на парашютах осветительные ракеты. В состав такой ракеты входили порошок магния, спрессованный с особыми составами, и запал из угля, бертолетовой соли и солей кальция. При запуске осветительной ракеты высоко над землей красивым ярким пламенем горел запал; по мере снижения свет постепенно делался более ровным, ярким и белым – это загорался магний. Наконец, когда цель была освещена и видна так же хорошо, как и днем, летчики начинали прицельное бомбометание.
 Магний использовали не только для создания осветительных ракет. Основным потребителем этого металла была военная авиация. Магния требовалось много, поэтому его добывали даже из морской воды. Технология извлечения магния такова: морскую воду смешивают в огромных баках с известковым молоком, затем, действуя на выпавший осадок соляной кислотой, получают хлорид магния. При электролизе расплава MgCl2 получают металлический магний (на экран проецируются уравнения реакций):
Магний использовали не только для создания осветительных ракет. Основным потребителем этого металла была военная авиация. Магния требовалось много, поэтому его добывали даже из морской воды. Технология извлечения магния такова: морскую воду смешивают в огромных баках с известковым молоком, затем, действуя на выпавший осадок соляной кислотой, получают хлорид магния. При электролизе расплава MgCl2 получают металлический магний (на экран проецируются уравнения реакций):
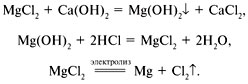
Было бы несправедливо не вспомнить сегодня о порохе. В основном во время Великой Отечественной войны использовался бездымный порох, который был создан Д. И. Менделеевым. Основой бездымного пороха является взрывчатое вещество нитроцеллюлоза.
Грозные боевые машины тех лет - легендарная «Катюша», знаменитый штурмовик ИЛ-2, которого панически боялись фашисты и называли его «черной смертью», были вооружены реактивными снарядами, топливом для которых служили бездымный порох.
Гораздо в меньших количествах использовался дымный порох, черный.
2КNO3 + 3C + S K2S + 3CO2 + N2
- Ребята, что по- вашему, позволило выдержать Т-34 натиск немецких танков?
/ использование сталей и сплавов /.
В годы войны кобальт стали применять для создания жаропрочных сталей и сплавов.
Используемая литература:
1. « Химия» - прилож. к «1 сентября» - №24, 2008 г.
2. Ж. «Современный урок» - №2, 2008 г.
3. О.С. Габриелян « Настольная книга учителя химии» -М., «Дрофа» - 2007г.
4. А.И. Буш «Внеклассная работа. Химия. 10 кл.» -Волгоград, «Корифей» - 2007г.
5. С.М. Курганский «Интеллектуальные игры по химии» -М., «5 за знания»- 2006 г.
6. Н.Б. Ковалевская «Химия в таблицах и схемах» -М., «Школа 21 век» - 2005г.
7. Интернет – ресурсы.








 обальтовая сталь использовалась для изготовления магнитных мин.
обальтовая сталь использовалась для изготовления магнитных мин.