Просмотр содержимого документа
«ЕГЭ по химии - задание 28»

ЕГЭ по химии задание 28

План
Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ

Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ
В подобных вычислениях нужно применить следующий алгоритм:а) сделать запись уравнения соответствующей условию задачи реакции. Расставить правильно стехиометрические коэффициенты;
б) сделать расчёт числа молей в-ва, количество которого указано в задаче. Если речь идёт о массе какого-то в-ва (А), то применить формулу:
n A = m A /M A
здесь
m A – масса в-ва A;
M A – молярная масса в-ва.
Если указаны объёмы газа, то вычислять по формуле:
n A = V A /V m ,
здесь
V A – объём газа A;
V m – молярный объём, равный для всех газообразных в-в при н.у. 22,4 л/моль.
Примечание. Если кол-во вещества даётся в молях , то его находить уже не требуется.
 преобразовав формулу: n B = n A /k A · k B г) определив количество в-ва В, найти его массу: m B = M B · n B для газообразного в-ва В использовать соответствующую формулу: V B = V m · n B = 22,4 л/моль · n B " width="640"
преобразовав формулу: n B = n A /k A · k B г) определив количество в-ва В, найти его массу: m B = M B · n B для газообразного в-ва В использовать соответствующую формулу: V B = V m · n B = 22,4 л/моль · n B " width="640"
в) затем определить моли искомого в-ва (В), используя следствия из закона Авогадро –
n A /k A = n B /k B
n A и n B – кол-во веществ А и В,
k A и k B – коэффициенты перед ними в уравнении.
= преобразовав формулу: n B = n A /k A · k B
г) определив количество в-ва В, найти его массу:
m B = M B · n B
для газообразного в-ва В использовать соответствующую формулу:
V B = V m · n B = 22,4 л/моль · n B
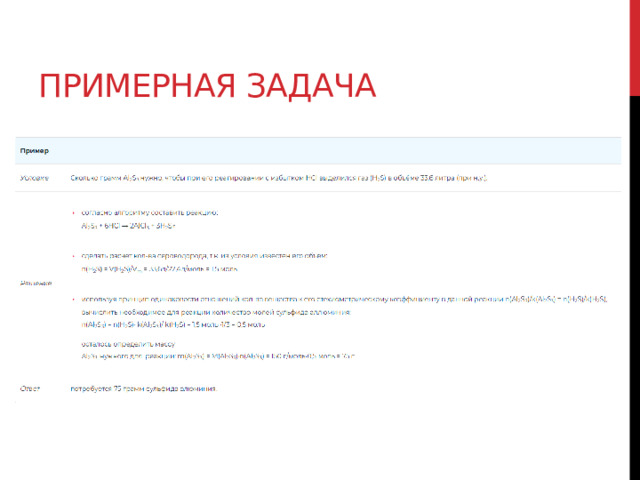
Примерная задача

Задача для подготовки к егэ
Определение значения «выхода продукта реакции» или «массовой примеси»
Из 150 кг природного известняка при взаимодействии с азотной кислотой был получен нитрат кальция массой 196,8 кг. Вычислите массовую долю (%) примесей в указанном известняке. (Запишите число с точностью до целых.)

Задача для подготовки к егэ
Расчет массы или объёма, вещества по параметрам
Рассчитайте объём (н. у.) ацетилена, который выделится при взаимодействии с водой 50 г карбида кальция, содержащего 8% примесей. Ответ укажите в литрах с точностью до десятых.

Домашняя работа
Вариант № 5511376
Ссылка - https:// chem-ege.sdamgia.ru/test?id=5511376








 преобразовав формулу: n B = n A /k A · k B г) определив количество в-ва В, найти его массу: m B = M B · n B для газообразного в-ва В использовать соответствующую формулу: V B = V m · n B = 22,4 л/моль · n B " width="640"
преобразовав формулу: n B = n A /k A · k B г) определив количество в-ва В, найти его массу: m B = M B · n B для газообразного в-ва В использовать соответствующую формулу: V B = V m · n B = 22,4 л/моль · n B " width="640"





















