Урок обобщения, повторения и систематизации знаний по теме "Атомы химических элементов". 8-й класс
Цель урока: Обобщить и систематизировать изученный материал по темам «Строение атома и систематизация химических элементов. Структура Периодической системы».
Задачи урока:
Образовательные: повторить, обобщить и систематизировать знания учащихся по изученной теме; подготовить учащихся к контрольной работе.
Развивающие: развивать у учащихся умения сравнивать и анализировать теоретические сведения, применять их на практике, делать выводы; развивать логическое мышление.
Воспитательные: формировать естественно-научное мировоззрение; информационную культуру.
Методы, используемые на уроке: частично-поисковые; индивидуальная работа учащихся.
Оборудование: периодическая таблица химических элементов Д.И.Менделеева; индивидуальные карточки – заготовки; компьютер; мультимедийный проектор и экран.
Ход урока
Вводная часть.
После приветствия учитель называет тему урока и сообщает его цели и задачи. Поясняет, что цель урока – не только обобщение и систематизация знаний по изученному материалу, но и выяснение степени готовности учащихся к контрольной работе. Чтобы вовлечь весь класс в совместный процесс познания, заинтересовать учащихся с любым уровнем подготовки учитель вводит игровой момент. Он сообщает, что на сегодняшний урок, знаний учащихся уже достаточно для того, чтобы отправиться в небольшое путешествие-плавание по океану “Периодическая система химических элементов Д.И.Менделеева”. Необходимо представить, что каждый ряд учащихся класса – это корабль (ученики, сидящие на первой парте – капитаны, а все остальные – матросы корабля).
I этап.
Итак, выполняя первое задание, вы можете получить разрешение выхода “кораблей” в океан “Периодическая система химических элементов Д.И.Менделеева”.
Задание: угадайте химический элемент.
| 1 вариант: | а) 3-й период III группа ______; | б) 20 p+ , 20 n0 , 20 e- ________; |
| | в) 3717 Э ____; | г) 1s22s22p5_______. |
| 2 вариант: | а) 2-й период IV группа ______; | б) 12 p+ , 12 n0 , 12 e- ________; |
| | в) 4019 Э ____; | г) 1s22s22p3_______. |
(Учитель проверяет задание у “капитана”, а он в свою очередь у членов своей команды.)
Подводится итог первого этапа: за правильно выполненное задание вручаются баллы (карточки или открытки).
фронтально: «Верю – не верю»
Ребята, вам предлагаются пять утверждений о внутреннем строении атома. Вы вправе верить им или нет. Ваша задача в тетради напротив номера утверждения, с которым вы согласны, поставить значок «+», а где не согласны «-».
Утверждения:
1.Только электроны входят в состав атома.
2.Электроны - отрицательно заряженные частицы.
3.Количество нейтронов и электронов одинаковое.
4.Относительная атомная масса равна количеству электронов.
5.Заряд ядра зависит от количества протонов.
Количество правильных ответов совпадает с оценкой.
Ответы: Нет, Да, Нет, Нет, Да
- Объясните, почему высказывания 1, 3 и 4 неверны? (С места 1 – 2 ученика)
- А что такое «химический элемент»? (Это определённый вид атомов)
II этап.
Учитель: Поздравляю с успешным началом плавания. Впереди “корабль” ____ ряда. Плавание продолжается! Вы знаете, что команда – “дружная семья”, поэтому следующая работа – коллективная, состоит из двух заданий.
1 задание: Определите, какие величины, характеризующие строение атома и положение химического элемента в таблице периодической системы, численно равны между собой. Буквы, соответствующие правильным ответам, образуют название химического элемента, обнаруженного в 1868 году астрономами Ж. Жансеном и Н. Локьером в солнечном спектре. Каждый участник команды выполняет одно задание и карточку передает другому ученику. ( Этот элемент – гелий).
| Строение атома | Положение химического элемента в таблице периодической системы Д.И. Менделеева |
| Порядковый номер | Номер периода | Номер группы |
| Заряд ядра | Г | Е | Д |
| Число электронов в атоме | Е | З | К |
| Число протонов в ядре атома | Л | В | М |
| Число электронов в наружном слое | О | А | И |
| Число электронных слоев | Р | Й | Я |
2 задание: Заполните таблицу. Каждый участник команды выполняет одно задание и карточку передает другому ученику.
| Знак | Название | Число протонов | Число нейтронов | Число электронов |
| S | | | | |
| | алюминий | | | |
| | | 14 | | |
| | | | | 20 |
| К | | | | |
Подводится итог второго этапа: за правильно выполненное задание вручаются баллы (карточки или открытки).
III этап.
Учитель: после второго этапа впереди “корабль” ____ ряда. Ночь, но любой моряк должен хорошо ориентироваться по звездам. В нашем случае – хорошо разбираться, как изменяются металлические и неметаллические свойства элементов в периодах и группах.
Задание: Укажите знаком “”
А) усиление неметаллических свойств:
| S | N | O |
| As Se Br | Si P S | P S Cl |
| Te | As | Se |
Б) усиление металлических свойств:
| B | Mg | Be |
| Mg Al Si | K Ca Se | Na Mg Al |
| Ga | Sr | Ca |
Работа выполняется у доски и в тетрадях учащихся, за правильно выполненное задание вручаются баллы (карточки или открытки). Подводится итог третьего этапа.
Учитель: да, путешествовать вы любите и можете, а умеете отгадывать загадки?
Славен ГОД зимой и летом
А алмазом славен этот…
(Углерод)
Это и не ВОР как раз,
Это самый легкий газ!
(Водород)
Вот ЖЕЛЕ скажу я вам,
Мне совсем не по зубам. (Железо)
Этот СОР бывает красным,
Белым тоже он бывает.
Он слывет огнеопасным
И об этом всякий знает. (Фосфор)
Этот ХОР нам всем известен,
Только не поет он песен. (Хлор)
IV этап.
Учитель: после третьего этапа и разминки впереди “корабль” ____ ряда. Но вот на пути наших кораблей препятствия “рифы”. Преодолеть их Вам опять поможет периодическая система химических элементов Д.И.Менделеева – своеобразная навигационная карта. Таблица несет в себе очень много информации: позволяет определять электронную конфигурацию атомов химических элементов, устанавливать максимальные степени окисления атомов в молекулах, а также помогает различить ионные и ковалентные соединения элементов!
Задание 1: вспомним строение атома. На доске изобразить строение атомов №6 и № 14, в классе по вариантам №11 и № 17
Сравните строение атомов этих химических элементов. Ребята, когда вы изображали строение атомов, вы указывали количество валентных электронов. Какие электроны мы называем валентными?
Задание № 2
Ниже приведены схемы строения атомов некоторых химических элементов. Какие из них относятся к атомам металлов, какие — к атомам неметаллов?


Задание 3. Распределите химические элементы, знаки которых приведены ниже, на две группы — металлы и неметаллы: S, Na, Р, Fe, N, Ag, А1, С, Ni
Si, CI, К, Br, Си, I, Ca, O, Zn.
Задание № 4
На следующем этапе мы обратимся к Периодической таблице, но для этого мы должны вспомнить её строение.
Посмотрите внимательно на Периодическую систему. Она вся поделена на клетки горизонтальными и вертикальными рядами. Как мы их называем? Расскажите мне о них поподробнее, используя план ответа на экране. (К ПС вызываются по одному 2 человека)
План ответа:
Определение.
Количество в периодической системе.
Деление на составляющие (какие?).
Как их найти?
Как обозначаются?
Физический смысл.
V этап.
Учитель: после четвертого этапа впереди “корабль” ____ ряда. Итак, путешествие подходит к концу, необходимо сделать соответствующие записи в “судовом журнале” (чистые листы с копировальной бумагой).
Характеристика химического элемента по следующему плану (план на листе ватмана в виде таблицы)
порядковый номер элемента, химический знак; номер периода;
номер группы (главная или побочная подгруппа); металл или неметалл;
число электронов на внешнем уровне; схема строения атома.
1 вариант: химический элемент – углерод; 2 вариант: химический элемент – литий.
Задание № 7
Найди элемент в периодической системе:
1. Это было известно еще до нашей эры. Правитель Персии Кир (2500 лет до н.э.) в военных походах питьевую воду сохранял в сосудах из этого металла.
...в Древней Индии накаленные стержни этого металла погружали в воду и потом ее использовали для обмывки ран, вода, приобретала лечебные свойства: в ней погибали микроорганизмы. Этот металл располагается в 4 периоде 1 группе побочной подгруппы, назовите его. (серебро)
2.Элемент находится в главной подгруппе VII группы 3 периода. Вещество, состоящее из атомов этого элемента, применяют для обеззараживания питьевой воды и уничтожения полевых грызунов. (хлор)
3. Недостаток этого элемента в организме приводит к выпадению шерсти у овец, появлению уродливой формы копыт и рогов у сельскохозяйственных животных и, поэтому, добавляется в рацион животных при возникновении названных отклонений в их развитии. Он находится 4 периоде 6 группе главной подгруппе. (Селен)
4. Для повышения урожайности томатов в качестве удобрения применяют соединения элемента электронная конфигурация атома которого1S2 2S22р3. Определите, какой это элемент. (Азот)
5. Элемент, являющийся необходимой составляющей костей и зубов
имеет строение внешнего энергетического уровня: 2s22p5? (фтор)
VI этап.
Учитель: после пятого этапа впереди “корабль” ____ ряда. Наше путешествие подошло к концу, возвращаемся в порт, просчитываем самый короткий путь.
Задание: Мини-лабиринт(рисунок 1). Найдите путь, который приведет Вас к финишу. Начните прохождение лабиринта с верхней левой клетки. Если суждение, вписанное в эту клетку, правильно, то продолжайте путь по стрелке с обозначением “Да”. Если данное суждение ошибочно, то вам следует продолжить путь по стрелке с обозначением “Нет”. Если Вы потеряли путь, то начните его сначала.
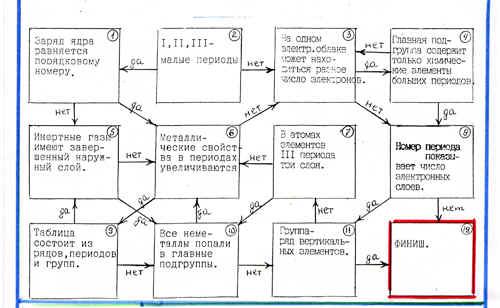
Рисунок 1 (1-6-3-8-11-12)
Заключительный этап.
Подводим итоги. Оценка за лабиринт; за характеристику элемента по плану будет выставлена на следующем уроке. Учитель: Изучение периодического закона и периодической системы, строения атома не заканчивается для вас: в дальнейшем вы будете изучать химию элементов, опираясь на закон и систему.
3




























