Просмотр содержимого документа
«Урок-презентация "Амины". Химия 10 класс.»

МАОУ Лицей №1 им. А.С. Пушкина Урок по теме: «Амины»

Понятие об аминах
Амины — производные аммиака,
в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал .
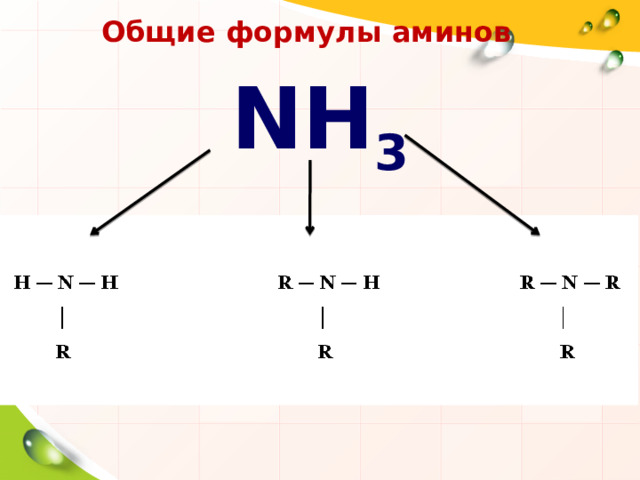
Общие формулы аминов
NH 3
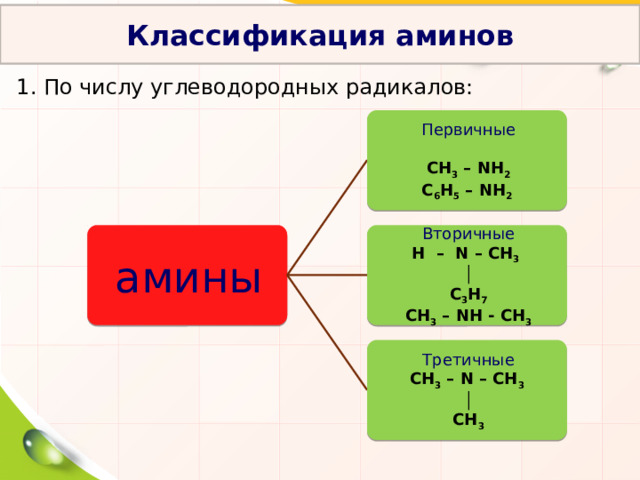
Классификация аминов
1. По числу углеводородных радикалов:
Первичные
СН 3 – NН 2
С 6 Н 5 – NН 2
Вторичные
амины
H – N – CH 3
│
С 3 Н 7
СН 3 – NН - СН 3
Третичные
CH 3 – N – CH 3
│
СН 3
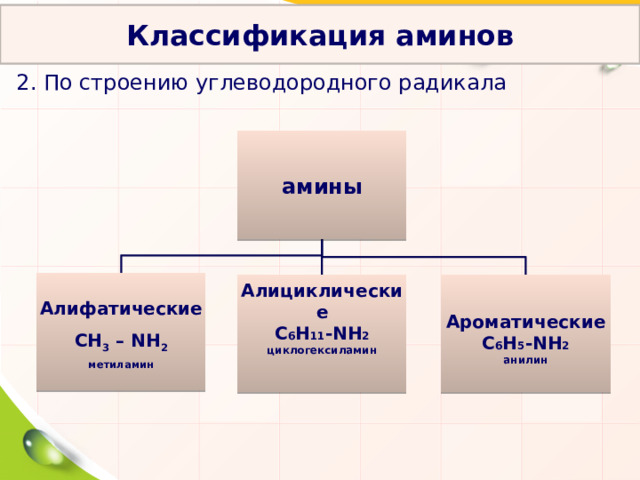
Классификация аминов
2. По строению углеводородного радикала
амины
Алифатические
СН 3 – NН 2
метиламин
Алициклические
С 6 Н 11 -NН 2
циклогексиламин
Ароматические
С 6 Н 5 -NН 2
анилин

Номенклатура аминов
РАДИКАЛ + АМИН

Изомерия аминов

Строение и свойства
- Атом азота имеет неподеленную электронную пару
- Аммиак проявляет основный характер
- Амины - органические основания
- Основный характер выражен слабее, чем у аммиака
- Основный характер выражен сильнее, чем у аммиака

Характеристика метиламина и анилина
Признаки сравнения
Метиламин
Формула
Анилин
СН 3 NH 2
С 6 Н 5 NH 2
Физические свойства
Бесцветный газ с резким аммиачным запахом, хорошо растворим в воде.
Бесцветная нерастворимая в воде жидкость с неприятным запахом, быстро темнеющая на воздухе, очень ядовитая

Анилин С 6 Н 5 -NH 2

Химические свойства
- Присоединение катионов водорода (донорно-акцепторный механизм, подобно аммиаку)
СН 3 -NH 2 + Н + СН 3 -NH 3 + ион метиламмония
С 6 Н 5 -NH 2 + Н + С 6 Н 5 -NH 3 + ион фениламмония
![Амины – это органические основания 2. Взаимодействие с кислотами СН 3 -NH 2 + НCl [СН 3 -NH 3 ] + Cl - или СН 3 -NH 2 · HCl хлорид метиламмония С 6 Н 5 -NH 2 + НCl [С 6 Н 5 -NH 3 ] + Cl - или С 6 Н 5 -NH 2 · HCl хлорид фениламмония СН 3 -NH 2 NH 3 С 6 Н 5 -NH 2 Метиламин Аммиак Анилин Основные свойства уменьшаются](https://fsd.multiurok.ru/html/2023/04/01/s_6427e9c7f1c73/img11.jpg)
Амины – это органические основания
2. Взаимодействие с кислотами
СН 3 -NH 2 + НCl [СН 3 -NH 3 ] + Cl - или
СН 3 -NH 2 · HCl
хлорид метиламмония
С 6 Н 5 -NH 2 + НCl [С 6 Н 5 -NH 3 ] + Cl - или
С 6 Н 5 -NH 2 · HCl
хлорид фениламмония
СН 3 -NH 2 NH 3 С 6 Н 5 -NH 2
Метиламин Аммиак Анилин
Основные свойства уменьшаются
![3. Взаимодействие с водой. CH 3 NH 2 + H OH →[CH 3 NH 3 ]OH Гидроксид метиламмония C 6 H 5 NH 2 + H OH → не взаимодействует](https://fsd.multiurok.ru/html/2023/04/01/s_6427e9c7f1c73/img12.jpg)
3. Взаимодействие с водой.
CH 3 NH 2 + H OH →[CH 3 NH 3 ]OH
Гидроксид метиламмония
C 6 H 5 NH 2 + H OH → не взаимодействует

4. Реакция горения.
9CH 3 NH 2 +9O 2 →4CO 2 +2N 2 +10H 2 O
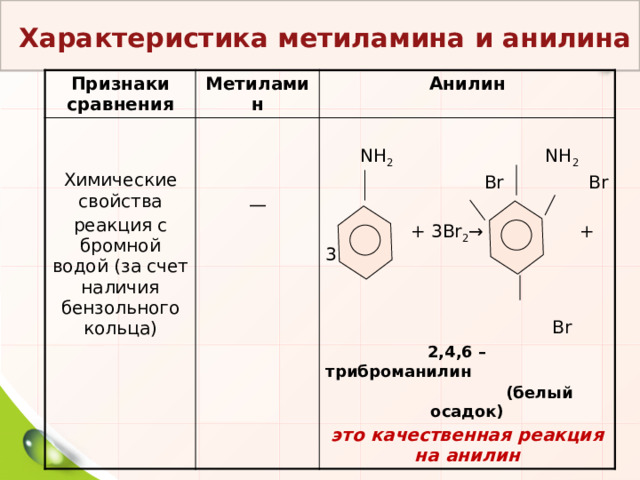
Характеристика метиламина и анилина
Признаки сравнения
Метиламин
Анилин
Химические свойства
реакция с бромной водой (за счет наличия бензольного кольца)
NH 2 NH 2
—
Br Br
+ 3Br 2 → + 3HBr
Br
2,4,6 – триброманилин
(белый осадок)
это качественная реакция на анилин

!
Анилин в отличие от бензола вступает в
реакцию бромирования по трем циклам (2,4,6)
КАЧЕСТВЕННАЯ РЕАКЦИЯ НА АНИЛИН

Получение аминов
1.Взаимодействие аммиака с галогенпроизводными углеводородов
CH 3 Cl+2 NH 3 →
→ CH 3 NH 2 +NH 4 Cl
2.Восстановление нитросоединений
C 6 H 5 NO 2 +3H 2 →
→ C 6 H 5 NH 2 +2H 2 O
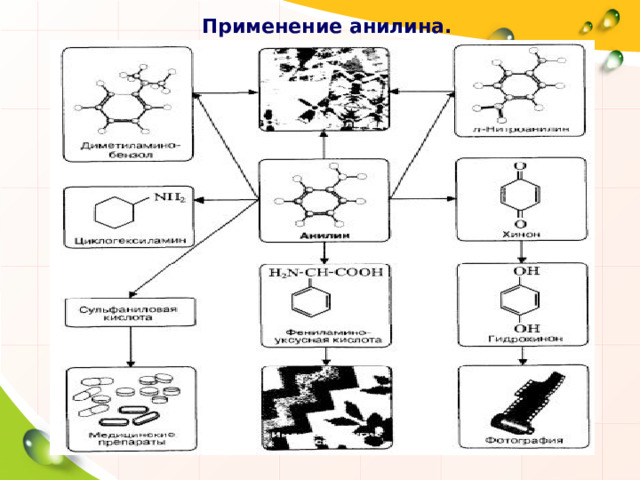
Применение анилина.

Решите задачу.
- Органическое вещество содержит 38,7% углерода, 45,15% азота и 16,15% водорода. Относительная плотность его паров по водороду равна 15,5. Определите формулу вещества.

Спасибо за урок!

















![Амины – это органические основания 2. Взаимодействие с кислотами СН 3 -NH 2 + НCl [СН 3 -NH 3 ] + Cl - или СН 3 -NH 2 · HCl хлорид метиламмония С 6 Н 5 -NH 2 + НCl [С 6 Н 5 -NH 3 ] + Cl - или С 6 Н 5 -NH 2 · HCl хлорид фениламмония СН 3 -NH 2 NH 3 С 6 Н 5 -NH 2 Метиламин Аммиак Анилин Основные свойства уменьшаются](https://fsd.multiurok.ru/html/2023/04/01/s_6427e9c7f1c73/img11.jpg)
![3. Взаимодействие с водой. CH 3 NH 2 + H OH →[CH 3 NH 3 ]OH Гидроксид метиламмония C 6 H 5 NH 2 + H OH → не взаимодействует](https://fsd.multiurok.ru/html/2023/04/01/s_6427e9c7f1c73/img12.jpg)

























