| Цель урока: Изучить свойства оксидов серы(4 и 6). Познакомить учащихся с качественной реакцией на сульфит и сульфат - ионы. Основные понятия: сернистый газ, серный ангидрид, сульфаты и гидросульфаты. Планируемые результаты обучения: Знать свойства оксидов серы 4 и 6. Уметь составлять уравнения реакций, характеризующие свойства данных оксидов с точки зрения ОВР. Оборудование: Штатив с пробирками, пробиркодержатель, химический стакан, Реактивы: Растворы серной кислоты, сульфата меди, гидроксида натрия, хлорида бария. Металлы: медь и цинк. Оксид меди Индикатор – фенолфталеин. Ход Урока: Работа у доски: Карточка 1 С какими из перечисленных веществ, формулы которых: H2O, BaO, CO2, может взаимодействовать оксид серы (4). Составьте уравнения химических реакций. Карточка 2 С какими из перечисленных веществ, формулы которых: NaOH, H2O, O2, может взаимодействовать сероводород . Составьте уравнения химических реакций
Фронтальный опрос: Какие степени окисления характерны для серы? Какими физическими свойствами обладает сернистый газ? Где в природе встречается сероводород? Какое значение имеет сероводород? Какими физическими свойствами обладает сернистый газ? Какой это оксид, и какие свойства он проявляет? Какие соли образует сернистая кислота? Где используется сернистый газ и соли сернистой кислоты? Назовите Вещество: - SO3 Новый материал: Сера проявляет степени окисления: S-2, S0, S+4, S+6. оксиде серы(IV) SO2 степень окисления +4, поэтому сернистый газ проявляет свойства окислителя и восстановителя SO2 (сернистый ангидрид; сернистый газ) 
Физические свойства Бесцветный газ с резким запахом; хорошо растворим в воде (в 1V H2O растворяется 40V SO2 при н.у.); более чем в два раза тяжелее воздуха, ядовит; t°пл. = -75,5°C; t°кип. = -10°С. Обесцвечивает многие красители, убивает микроорганизмы. Получение 1) При сжигании серы в кислороде: S + O2 → SO2 2) Окислением сульфидов: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 3) Обработкой солей сернистой кислоты минеральными кислотами: Na2SO3 + 2HCl → 2NaCl + SO2 + H2O 4) При окислении металлов концентрированной серной кислотой: Cu + 2H2SO4(конц) → CuSO4 + SO2 + 2H2O Химические свойства 1) Сернистый ангидрид - кислотный оксид. · взаимодействие с водой При растворении в воде образуется слабая и неустойчивая сернистая кислота H2SO3 (существует только в водном растворе) Оксид серы (VI) - SO3 (серный ангидрид) 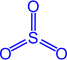 Физические свойства Бесцветная летучая маслянистая жидкость, t°пл. = 17°C; t°кип. = 66°С; на воздухе "дымит", сильно поглощает влагу (хранят в запаянных сосудах). SO3 хорошо растворяется в 100%-ной серной кислоте, этот раствор называется олеумом. Получение 1) 2SO2 + O2 → 2SO3 (катализатор – V2O5, при 450˚С) 2) Fe2(SO4)3 → Fe2O3 + 3SO3 (разложение при нагревании) Химические свойства 1) Серный ангидрид - кислотный оксид. Взаимодействие со щелочами 2NaOH + SO3 → Na2SO4 + H2O NaOH + SO3 (избыток) → NaHSO4 Взаимодействие с основными оксидами Na2O + SO3 → Na2SO4 2) SO3 - сильный окислитель. Взаимодействие с водой При растворении в воде дает сильную двухосновную серную кислоту: SO3 + H2O → H2SO4 Задания для закрепления №1. Осуществите превращения по схеме: 1) ZnS - SO2 - Na2SO3 - SO2- S 2) S - SO2 - SO3 - H2SO4 - K2SO4 №2. Закончите уравнения практически осуществимых реакций в полном и кратком ионном виде: Na2CO3 + H2SO4 - Cu + H2SO4 (конц) - №3. Запишите уравнения реакций взаимодействия оксида серы 6 с гидроксидом железа (III), оксидом алюминия. На дом: | 



























