
Реакции ионного обмена
БАРБАШИНА ЛЮБОВЬ ВИКТОРОВНА ВОРОНЕЖСКИЙ ГОСУДАРСТВЕННЫЙ ПРОФЕССИОНАЛЬНО-ПЕДАГОГИЧЕСКИЙ КОЛЛЕДЖ

Цель: закрепить навык составления уравнений реакций в ионном виде

Вставьте пропущенные слова:
Уравнения реакций, в которых вещества записаны в форме молекул, называются _________________.
Уравнения реакций, в которых вещества записаны в виде ионов, называются ___________.
Чтобы составить ионное уравнение, надо записать в виде ионов все _________ ____________.
Сильными электролитами являются:
соли: ______________,
кислоты: ________________________,
основания: _____ ___ ____________________.
молекулярными
ионными
электролиты
сильные
растворимые
серная, соляная, азотная
NaOH, KOH, Ba(OH) 2 , Ca(OH) 2
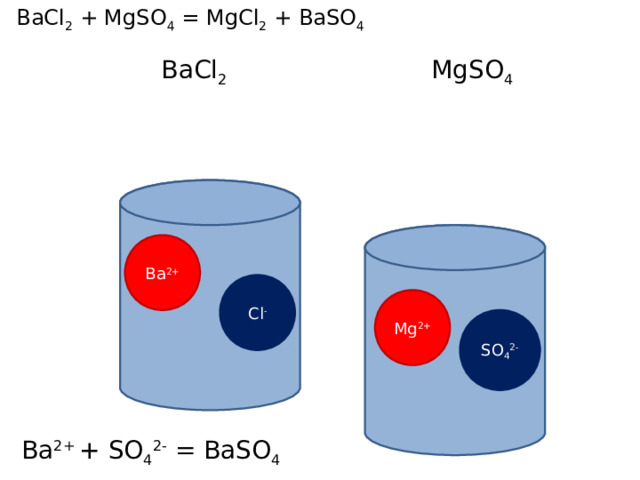
BaCl 2 + MgSO 4 = MgCl 2 + BaSO 4
BaCl 2
MgSO 4
Ba 2+
Cl -
Mg 2+
SO 4 2-
Ba 2+ + SO 4 2- = BaSO 4
+ 2 H 2 O
2 H + +SO 4 2-
+ 2 OH - +
2 Na +
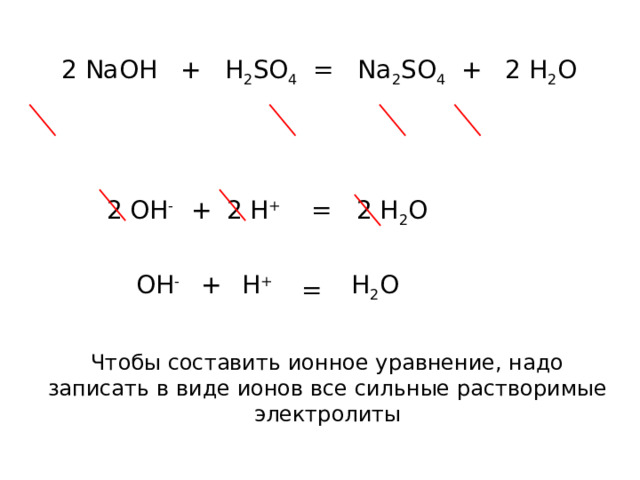
2 NaOH + H 2 SO 4 = Na 2 SO 4 + 2 H 2 O
= 2 Na + + SO 4 2-
+
=
2 H +
2 H 2 O
2 OH -
OH -
+
H 2 O
H +
=
Чтобы составить ионное уравнение, надо записать в виде ионов все сильные растворимые электролиты
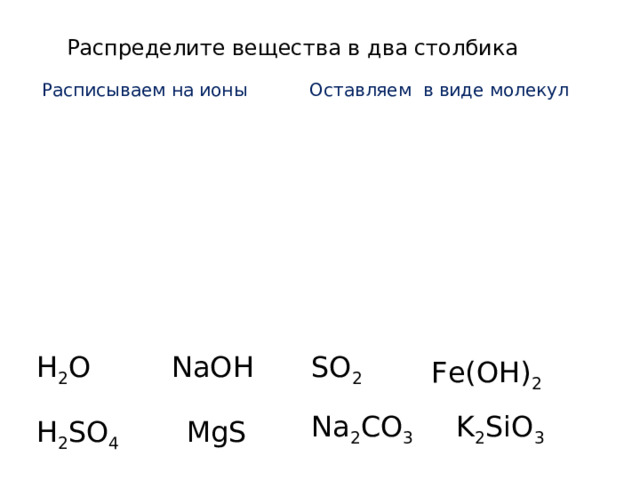
Распределите вещества в два столбика
Расписываем на ионы Оставляем в виде молекул
H 2 O
NaOH
SO 2
Fe(OH) 2
Na 2 CO 3
K 2 SiO 3
H 2 SO 4
MgS
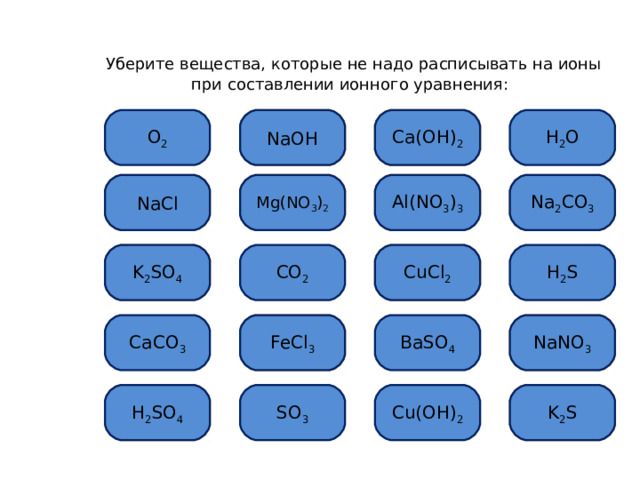
Уберите вещества, которые не надо расписывать на ионы при составлении ионного уравнения:
Ошибка
Ca(OH) 2
Ошибка
H 2 O
О 2
NaOH
Mg(NO 3 ) 2
Ошибка
Al(NO 3 ) 3
Ошибка
NaCl
Ошибка
Ошибка
Na 2 CO 3
Ошибка
CuCl 2
Н 2 S
CO 2
Ошибка
K 2 SO 4
CaCO 3
Ошибка
FeCl 3
Ошибка
NaNO 3
BaSO 4
S О 3
K 2 S
Ошибка
Cu(OH) 2
H 2 SO 4
Ошибка

Ученик составил полные ионные уравнения для данных молекулярных. Исправьте ошибки. Составьте сокращенные ионные уравнения.
Fe ( OH) 3 + 3 HCl = FeCl 3 + 3 H 2 O
Fe 3+ + 3 OH - + 3 H + + 3 Cl - = Fe 2+ + 3 Cl - + 3 H 2 O
Са ( OH) 2 + 2 HCl = CaCl 2 + 2 H 2 O
Ca 2+ + OH - + 2 H + + Cl - = Ca 2+ + Cl - + 2 H 2 O
Ba (NO 3 ) 2 + Na 2 SO 4 = BaSO 4 + 2 NaNO 3
Ba + 2 NO 3 + 2 Na + SO 4 = BaSO 4 + 2 Na + 2 NO 3
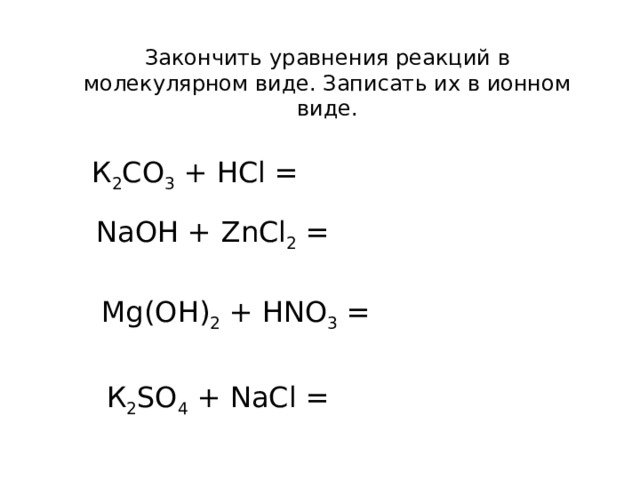
Закончить уравнения реакций в молекулярном виде. Записать их в ионном виде.
К 2 СО 3 + HCl =
Na О H + ZnCl 2 =
Mg( О H) 2 + HNO 3 =
К 2 S О 4 + NaCl =
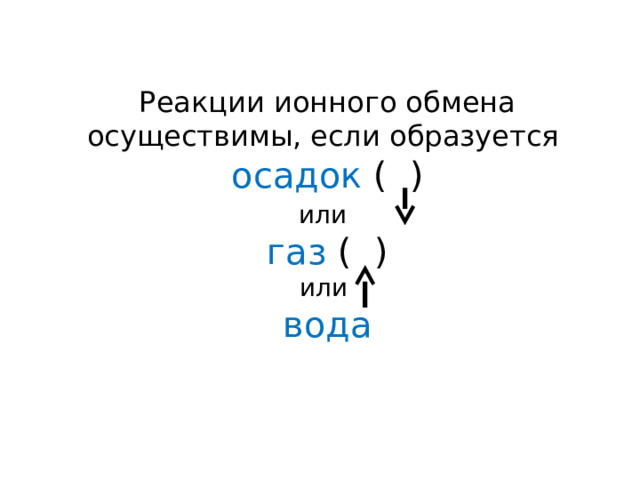
Реакции ионного обмена осуществимы, если образуется
осадок ( )
или
газ ( )
или
вода
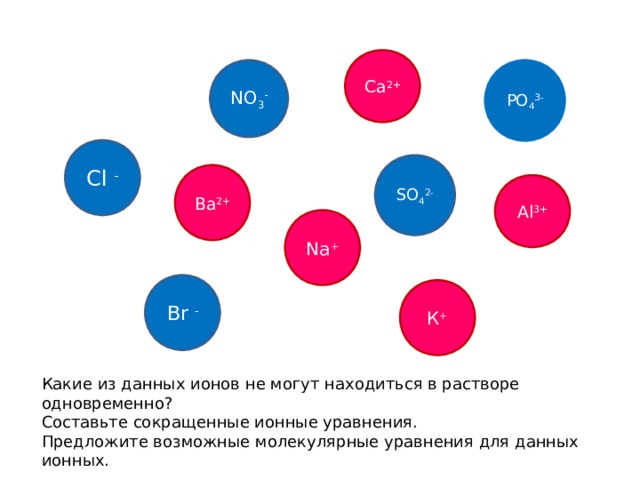
Са 2+
NO 3 -
PO 4 3-
Cl -
SO 4 2-
Ba 2+
Al 3 +
Na +
Br -
К +
Какие из данных ионов не могут находиться в растворе одновременно?
Составьте сокращенные ионные уравнения.
Предложите возможные молекулярные уравнения для данных ионных.

Самостоятельная работа
Составьте уравнения реакций в молекулярной, ионной и сокращенной ионной формах
Вариант 1
Вариант 2
- Al Cl 3 + Ag NO 3 =
- Zn (OH) 2 + 2 HNO 3 =
2) Cu (OH) 2 + 2 HCl =

Проверь себя:
Вариант 1
- 3 CaCl 2 + 2 K 3 PO 4 = Ca 3 (PO 4 ) 2 + 6 KCl
3 Са 2+ + 6 Cl - + 6 K + + 2 PO 4 3- = Ca 3 (PO 4 ) 2 + 6K + + 6Cl -
3 Са 2+ + 2 PO 4 3- = Ca 3 (PO 4 ) 2
2) Cu (OH) 2 + 2 HCl = CuCl 2 + 2 H 2 O
Cu (OH) 2 + 2 H + + 2Cl - = Cu 2+ + 2 Cl - + 2 H 2 O
Cu (OH) 2 + 2 H + = Cu 2+ + 2 H 2 O
Вариант 2
- Al Cl 3 + 3 Ag NO 3 = Al (NO3)3 + 3AgCl
Al 3+ + 3Cl - + 3 Ag + + 3 NO 3 - = Al 3+ + 3NO 3 - + 3AgCl
Cl - + Ag + = AgCl
2) Zn (OH) 2 + 2 HNO 3 = Zn (NO 3 ) 2 + 2 H 2 O
Zn (OH) 2 + 2 H + + 2 NO 3 - = Zn 2+ + 2 NO 3 - + 2 H 2 O
Zn (OH) 2 + 2 H + = Zn 2+ + 2 H 2 O

Домашнее задание:
§ 37 (повторить).
Придумать свои реакции, в которых бы:
А) образовался осадок;
Б) выделился газ;
В) реакции не происходило.
Составить уравнения в молекулярном и ионном виде.








































