
Глюкоза – хімічныя ўласцівасці, атрыманне і прымяненне
Падрыхтавала
Міхайлава Яніна Яўгеньеўна
настайніца хіміі
ДУА ”НПК Забалацкія яслі-сад-сярэдняя школа”

Пазнаемціся са спісам магчымых мэтаў вывучэння тэмы і адзначце для сябе самыя галоўныя:
- Вывучыць матэрыял падручніка
- Засвоіць асноўныя законы і паняцці
- Падрыхтаваць творчае заданне, паведамленне па адной з праблем
- Добра падрыхтавацца да тэста, кантрольнай работы
- Авалодаць эксперыментальнымі метадамі вывучэння рэчываў
- Атрымаць добрую адзнаку
- Праявіць і развіць свае здольнасці (пералічыць)
- Магу даведацца штосьці новае
- Свой варыянт мэты і інш.

Пазнанне пачынаецца са здзіўлення Арыстоцель
Гістарычная даведка:
- У 1861г. А.М.Бутлераў атрымаў рэчыва “Х” з фармальдэгіду
- У 1811г. рэчыва “Х” атрымаў рускі вучоны К.С.Кірхгоф пры гідролізе крухмалу
- Рэчыва “Х” салодкае на смак, добра раствараецца ў вадзе, тэмпература плаўлення 146°С
- У 100мл крыві чалавека знаходзіцца 80-120мг рэчыва “Х”
- Рэчыва “Х” шырока сустракаецца ў прыродзе, асабліва многа ў вінаградным соку, садавіне, мёдзе
- Утвараецца рэчыва “Х” у працэсе фотасінтэзу ў зяленых лістах раслін
- Рэчыва “Х” – прадстаўнік монацукрыдаў рада гексозаў

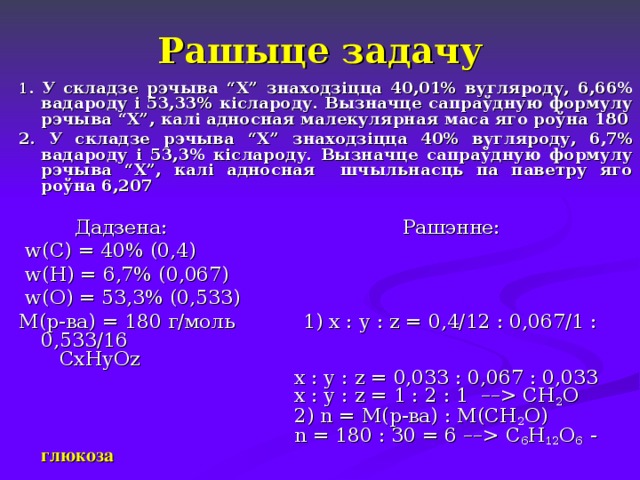
Рашыце задачу
- У складзе рэчыва “Х” знаходзіцца 40,01% вугляроду, 6,66% вадароду і 53,33% кіслароду. Вызначце сапраўдную формулу рэчыва “Х”, калі адносная малекулярная маса яго роўна 180
2. У складзе рэчыва “Х” знаходзіцца 40% вугляроду, 6,7% вадароду і 53,3% кіслароду. Вызначце сапраўдную формулу рэчыва “Х”, калі адносная шчыльнасць яго па паветру роўна 6,207
 СН 2 О 2) n = М(р-ва) : М(СН 2 О) n = 180 : 30 = 6 –– С 6 Н 12 О 6 - глюкоза " width="640"
СН 2 О 2) n = М(р-ва) : М(СН 2 О) n = 180 : 30 = 6 –– С 6 Н 12 О 6 - глюкоза " width="640"
Рашыце задачу
1. У складзе рэчыва “Х” знаходзіцца 40,01% вугляроду, 6,66% вадароду і 53,33% кіслароду. Вызначце сапраўдную формулу рэчыва “Х”, калі адносная малекулярная маса яго роўна 180
2. У складзе рэчыва “Х” знаходзіцца 40% вугляроду, 6,7% вадароду і 53,3% кіслароду. Вызначце сапраўдную формулу рэчыва “Х”, калі адносная шчыльнасць па паветру яго роўна 6,207
Дадзена: Рашэнне:
w (С) = 40% (0,4)
w (Н) = 6,7% (0,067)
w (О) = 53,3% (0,533)
М(р-ва) = 180 г/моль 1) х : у : z = 0,4/12 : 0,067/1 : 0,533/16 СхНуОz х : у : z = 0,033 : 0,067 : 0,033 х : у : z = 1 : 2 : 1 –– СН 2 О 2) n = М(р-ва) : М(СН 2 О) n = 180 : 30 = 6 –– С 6 Н 12 О 6 - глюкоза
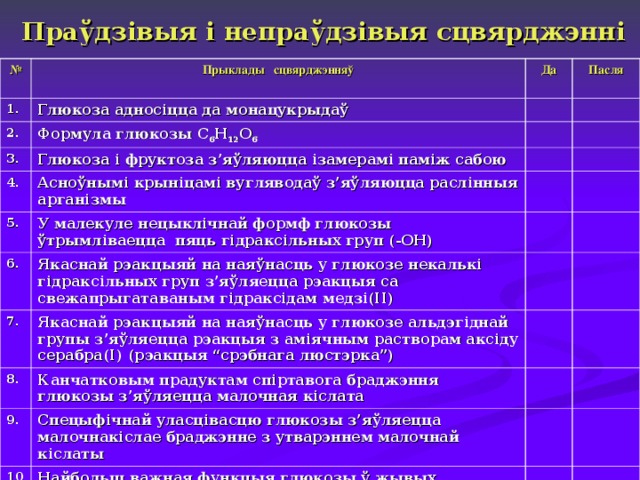
Праўдзівыя і непраўдзівыя сцвярджэнні
№
Прыклады сцвярджэнняў
1.
Да
Глюкоза адносіцца да монацукрыдаў
2.
3.
Пасля
Формула глюкозы С 6 Н 12 О 6
4.
Глюкоза і фруктоза з’яўляюцца ізамерамі паміж сабою
Асноўнымі крыніцамі вугляводаў з’яўляюцца раслінныя арганізмы
5.
У малекуле нецыклічнай формф глюкозы ўтрымліваецца пяць гідраксільных груп (-ОН)
6.
Якаснай рэакцыяй на наяўнасць у глюкозе некалькі гідраксільных груп з’яўляецца рэакцыя са свежапрыгатаваным гідраксідам медзі(ІІ)
7.
Якаснай рэакцыяй на наяўнасць у глюкозе альдэгіднай групы з’яўляецца рэакцыя з аміячным растворам аксіду серабра(І) (рэакцыя “срэбнага люстэрка”)
8.
Канчатковым прадуктам спіртавога браджэння глюкозы з’яўляецца малочная кіслата
9.
Спецыфічнай уласцівасцю глюкозы з’яўляецца малочнакіслае браджэнне з утварэннем малочнай кіслаты
10.
Найбольш важная функцыя глюкозы ў жывых арганізмах – забеспячэнне клетак энергіяй

Тэма: Глюкоза – хімічныя ўласцівасці, атрыманне і прымяненне
Мэта:
Арганізаваць пазнавальную дзейнасць, якая будзе спрыяць фарміраванню ведаў аб хімічных уласцівасцях, атрыманні і прымяненні глюкозы
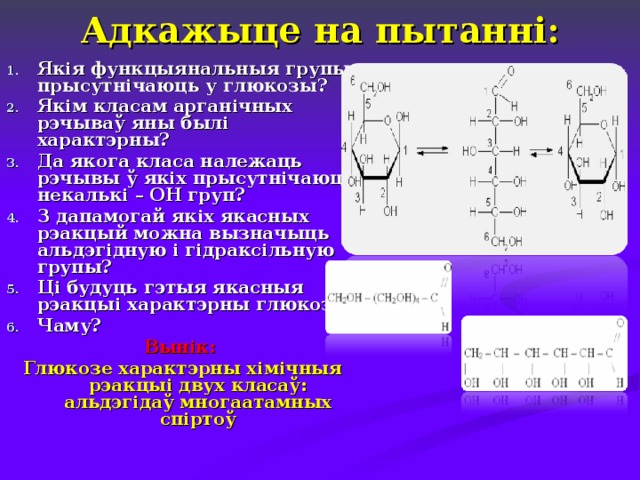
Адкажыце на пытанні:
- Якія функцыянальныя групы прысутнічаюць у глюкозы?
- Якім класам арганічных рэчываў яны былі характэрны?
- Да якога класа належаць рэчывы ў якіх прысутнічаюць некалькі – ОН груп?
- З дапамогай якіх якасных рэакцый можна вызначыць альдэгідную і гідраксільную групы?
- Ці будуць гэтыя якасныя рэакцыі характэрны глюкозе?
- Чаму?
Вынік:
Глюкозе характэрны хімічныя рэакцыі двух класаў: альдэгідаў многаатамных спіртоў

Видеопыты
- Качественная реакция с гидроксидом меди ( II )
- Реакция глюкозы с аммиачным раствором оксида серебра

Хімічныя ўласцівасці глюкозы:
Глюкоза
Па альдэгіднай групе
(-СОН)
Па гідраксільнай групе
(-ОН)
1. Акісленне
1. Рэакцыя з бромнай вадой
CH 2 OH - CH ( OH ) 4 - COH + Br 2 + H 2 O → CH 2 OH - CH ( OH ) 4 - C О OH +2 HBr
глюконава кіслата
2. Рэакцыя з аміячным растворам аксіду серебра (І) ( р-я “срэбнага люстэрка”)
СН 2 ОН – (СНОН) 4 – СОН + Ag 2 O = CH 2 OH - CH ( OH ) 4 – СООН + 2Ag
Спецыфічныя
2. Аднаўленне
3. Браджэнне
1. Рэакцыя з гідраксідам медзі (ІІ);
утвараецца раствор ярка-сіняга (васільковага) колеру, пры награванні выпадае чырвоны асадак аксіду медзі(І)
C 6 H 12 O 6 + 2Cu(OH) 2 C 6 H 1 2 O 7 + Cu 2 O+ 2H 2 O
CH 2 OH - CH ( OH ) 4 - COH → CH 2 OH - CH ( OH ) 4 - CH 2 OH
сарбіт
- Спіртавое
- Малочнакіслае
- Маслянакіслае

Якасныя рэакцыі на глюкозу:
1. Рэакцыя «срэбнага люстэрка»
- 1. Рэакцыя «срэбнага люстэрка»
t
C 6 H 12 O 6 + Ag 2 O C 6 H 12 O 7 + 2Ag↓
люстраны налёт серабра
- t C 6 H 12 O 6 + Ag 2 O C 6 H 12 O 7 + 2Ag↓ люстраны налёт серабра
2. Узаемадзеянне з гідраксідам медзі (ІІ) пры награванні
t C 6 H 12 O 6 +2Cu(OH) 2 C 6 H 1 2 O 7 +Cu 2 O↓+ 2H 2 O чырвоная афарбоўка асадку

Лабараторны дослед №7
А
Б
Й
К
В
У
Л
Э
Г
Ф
Ю
Д
М
Х
Н
Е
Я
Ц
О
Ё
Ч
П
Ш
Ж
Р
ў
З
І
С
‘
Т
Ы
Ь
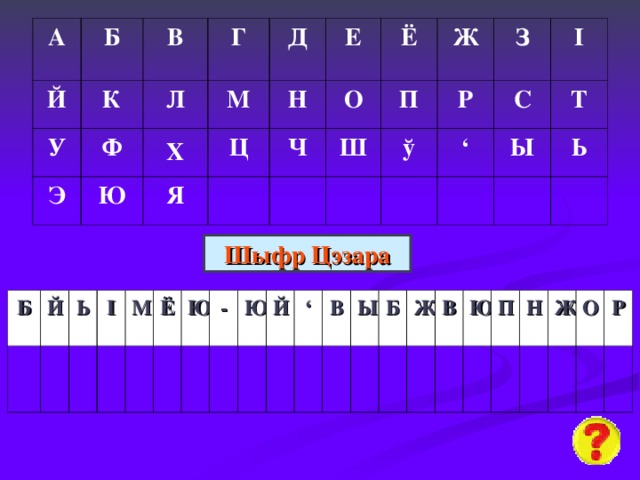
Шыфр Цэзара
Б
Й
Ь
І
М
Ё
Ю
-
Ю
Й
‘
В
Ы
Б
Ж
В
Ю
П
Н
Ж
О
Р

А
Б
Й
К
В
У
Э
Г
Ф
Л
Ю
Д
М
Х
Н
Е
Я
Ц
О
Ё
Ч
П
Ш
Ж
ў
З
Р
І
С
‘
Т
Ы
Ь
Шыфр Цэзара
Б
г
Й
Ь
л
І
ю
М
к
о
Ё
з
Ю
-
а
Ю
-
а
Й
л
‘
ь
В
д
Ы
э
Б
Ж
г
В
і
Ю
д
а
П
Н
с
Ж
п
і
О
Р
р
т

Спецыфічныя ўласцівасці глюкозы
1. Спіртавое браджэнне С 6 Н 12 О 6 ферменты дрожжаў 2С 2 Н 5 ОН+2СО 2 2. Малочнакіслае браджэнне С 6 Н 12 О 6 ферменты 2СН 3 СН(ОН)СООН 3. Маслянакіслае браджэнне С 6 Н 12 О 6 ферменты С 3 Н 7 СООН+СО 2 +2Н 2

Хімічныя ўласцівасці глюкозы:
Глюкоза
Па альдэгіднай групе
(-СОН)
Па гідраксільнай групе
(-ОН)
1. Акісленне
1. Рэакцыя з бромнай вадой
CH 2 OH - CH ( OH ) 4 - COH + Br 2 + H 2 O → CH 2 OH - CH ( OH ) 4 - C О OH +2 HBr
глюконава кіслата
2. Рэакцыя з аміячным растворам аксіду серебра (І) ( р-я “срэбнага люстэрка”)
СН 2 ОН – (СНОН) 4 – СОН + Ag 2 O = CH 2 OH - CH ( OH ) 4 – СООН + 2Ag
Спецыфічныя
2. Аднаўленне
3. Браджэнне
1. Спіртавое
С 6 Н 12 О → 2С 2 Н 5 ОН+
+2СО 2
2. Малочнакіслае
С 6 Н 12 О 6 →
2СН 3 СН(ОН)СООН
3. Маслянакіслае
1. Рэакцыя з гідраксідам медзі (ІІ);
утвараецца раствор ярка-сіняга (васільковага) колеру, пры награванні выпадае чырвоны асадак аксіду медзі(І)
C 6 H 12 O 6 + 2Cu(OH) 2 C 6 H 1 2 O 7 + Cu 2 O+ 2H 2 O
CH 2 OH - CH ( OH ) 4 - COH → CH 2 OH - CH ( OH ) 4 - CH 2 OH
сарбіт
С 6 Н 12 О 6 → С 3 Н 7 СООН+СО 2 +2Н 2

Этапы даследвання: Праблема – гіпотэза - праверка гіпотэзы – аналіз - вынік
1.Выстаўленне гіпотэзы:
- Калі..., то…
- Так, як…
- Пры ўмове, што..
- Прапаноўваецца, што..
- Дапусцім..
- Магчыма, што…
Магчыма гіпотэза: калі даследуемае рэчыва змяшчае глюкозу, то яно будзе валодаць энергетычнай каштоўнасцю і забяспечваць наш арганізм вугляводамі, якія з’яўляюцца аднымі з асноўных кампанентаў ежы чалавека.

Праверка гіпотэзы
Да дзена рэчыва
П адзейнічаем
С u(OH) 2
Даследуем колер злучэння
Не зм яніў ся
З м яніў ся
Ярка-сіні (васільковы)
Чырванее пры награванні
Г люкозы н яма
Глюкоза ёсць

“ Раскажы - і я забуду, пакажы - і я запомню. Дай дзейнічаць самаму - і я навучуся“ Усходняя мудрасць
3. Праверка гіпотэзы
План рашэння эксперыментальнай задачы :
1. Падрыхтуйце гідраксід медзі ( II ). 2. Раздзяліце яго на 2 часткі. 3. У кожную частку прыліце даследуемае рэчыва
4. Нагрэйце змесціва прабірак. 5. Запішыце вынікі назіранняў.
4. Аналіз назіранняў доследаў
5. Фармуліроўка выніка
Вынік: калі мы выявілі глюкозу…

“ Раскажы - і я забуду, пакажы - і я запомню. Дай дзейнічаць самаму - і я навучуся“ Усходняя мудрасць
3. Праверка гіпотэзы
План рашэння эксперыментальнай задачы :
1. Падрыхтуйце гідраксід медзі ( II ). 2. Раздзяліце яго на 2 часткі. 3. У кожную частку прыліце даследуемае рэчыва
4. Нагрэйце змесціва прабірак. 5. Запішыце вынікі назіранняў.
4. Аналіз назіранняў доследаў
5. Фармуліроўка выніка
Вынік: калі мы выявілі глюкозу, то гіпотэза падцвердзілася, значыць тавар валодае энергетычнай каштоўнасцю і забяспечвае наш арганізм вугляводамі

Атрыманне глюкозы
1) Рэакцыя фотасінтэзу
6СО 2 + 6 H 2 O → С 6 Н 12 О 6 + 6О2 + Q
2) Рэакцыя полімерызацыі
6 НСОН → С 6 Н 12 О 6
3) Гідроліз крухмалу
(С 6 Н 10 О 5 ) n + n H 2 O → n С 6 Н 12 О 6

Прымяненне глюкозы (медыцынскай і тэхнічнай)
- в пищевой промышленности;
- в кондитерской промышленности;
- в хлебопечении;
- в производстве мороженого;
- при производстве фруктовых консервов, соков, вин и безалкогольных напитков;
- в молочной промышленности
- продуктов детского питания;
- в ветеринарии;
- в птицеводстве;
- в фармацевтической промышленности;
- для питания больных, травмированных, выздоравливающих, работающих с большими перегрузками;
- в антибиотиках и других лекарственных препаратах, для внутривенных вливаний,
- для получения витамина С;
- в качестве восстановителя в кожевенном производстве;
- в текстильном – при производстве вискозы;
- в качестве питательной среды при выращивании различных видов микроорганизмов;
- в медицинской и микробиологической промышленности.

Наливаешь крепкий чай, Хорошенько сахарозу В чашке ложкой размешай. Виноградную глюкозу, И медовую фруктозу, И молочную лактозу Любят взрослый и малыш. Но крахмалом и клетчаткой, Что совсем-совсем несладки, Тоже нас не удивишь. Так устроена природа – Это тоже……

Наливаешь крепкий чай, Хорошенько сахарозу В чашке ложкой размешай. Виноградную глюкозу, И медовую фруктозу, И молочную лактозу Любят взрослый и малыш. Но крахмалом и клетчаткой, Что совсем-совсем несладки, Тоже нас не удивишь. Так устроена природа – Это тоже……
углеводы
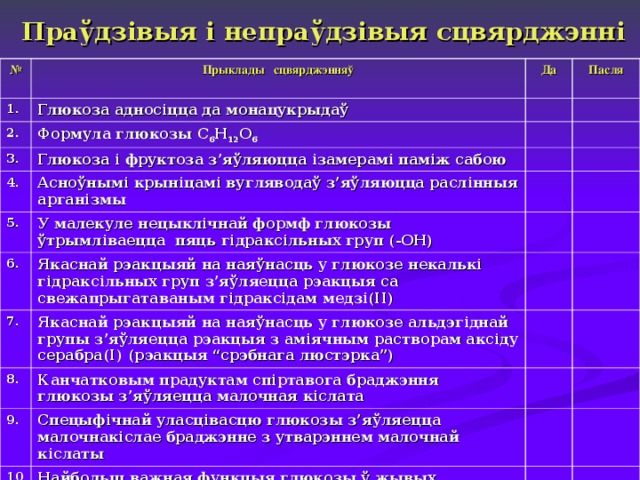
Праўдзівыя і непраўдзівыя сцвярджэнні
№
Прыклады сцвярджэнняў
1.
Да
Глюкоза адносіцца да монацукрыдаў
2.
3.
Пасля
Формула глюкозы С 6 Н 12 О 6
4.
Глюкоза і фруктоза з’яўляюцца ізамерамі паміж сабою
Асноўнымі крыніцамі вугляводаў з’яўляюцца раслінныя арганізмы
5.
У малекуле нецыклічнай формф глюкозы ўтрымліваецца пяць гідраксільных груп (-ОН)
6.
Якаснай рэакцыяй на наяўнасць у глюкозе некалькі гідраксільных груп з’яўляецца рэакцыя са свежапрыгатаваным гідраксідам медзі(ІІ)
7.
Якаснай рэакцыяй на наяўнасць у глюкозе альдэгіднай групы з’яўляецца рэакцыя з аміячным растворам аксіду серабра(І) (рэакцыя “срэбнага люстэрка”)
8.
Канчатковым прадуктам спіртавога браджэння глюкозы з’яўляецца малочная кіслата
9.
Спецыфічнай уласцівасцю глюкозы з’яўляецца малочнакіслае браджэнне з утварэннем малочнай кіслаты
10.
Найбольш важная функцыя глюкозы ў жывых арганізмах – забеспячэнне клетак энергіяй
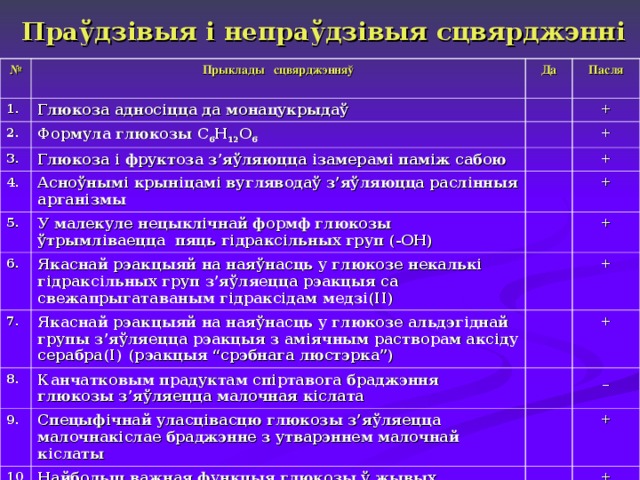
Праўдзівыя і непраўдзівыя сцвярджэнні
№
1.
Прыклады сцвярджэнняў
Глюкоза адносіцца да монацукрыдаў
2.
Да
Пасля
Формула глюкозы С 6 Н 12 О 6
3.
+
Глюкоза і фруктоза з’яўляюцца ізамерамі паміж сабою
4.
+
Асноўнымі крыніцамі вугляводаў з’яўляюцца раслінныя арганізмы
5.
+
У малекуле нецыклічнай формф глюкозы ўтрымліваецца пяць гідраксільных груп (-ОН)
6.
+
Якаснай рэакцыяй на наяўнасць у глюкозе некалькі гідраксільных груп з’яўляецца рэакцыя са свежапрыгатаваным гідраксідам медзі(ІІ)
7.
+
Якаснай рэакцыяй на наяўнасць у глюкозе альдэгіднай групы з’яўляецца рэакцыя з аміячным растворам аксіду серабра(І) (рэакцыя “срэбнага люстэрка”)
8.
+
Канчатковым прадуктам спіртавога браджэння глюкозы з’яўляецца малочная кіслата
9.
+
Спецыфічнай уласцівасцю глюкозы з’яўляецца малочнакіслае браджэнне з утварэннем малочнай кіслаты
10.
_
Найбольш важная функцыя глюкозы ў жывых арганізмах – забеспячэнне клетак энергіяй
+
+

Дыялог - рэфлексія
Адкажыце на пытанні:
- Як часта вы сёння здзіўляліся? Прачытайце яшчэ раз эпіграф. Вы згодны з Арыстоцелем?
- Ці дасягнулі мэтаў, пастаўленых у пачатку ўрока?
- Ці выканалі мы з вамі ўсё, што планавалі на ўроку?
- Ці зможаце вы, атрыманыя на сённяшнім ўроку веды, прымяніць у сваім паўсядзённым жыцці? У якіх выпадках?
- Як вы думаеце, ці часта чалавеку прыходзіцца ў паўсядзённым жыцці сутыкацца з пытаннямі, якія мы закранулі на ўроку?

Дамашняе заданне
- § 45, заданне 5 – 9 ( па выбару)
Творчыя заданні :
- Напішыце казку-апавяданне аб ролі глюкозы ў жывых арганізмах, пачынючы са словаў “Жыла-была каралева Глюкоза…”;
- Напішыце SMS – сябру аб адносінах да ўроку;
- Прыдумайце хімічны камплімент глюкозе;
- Міні-даследванне: параўнайце кандытарскія прадукты гандлёвай сеткі на % ўтрымання ў іх вугляводаў.












 СН 2 О 2) n = М(р-ва) : М(СН 2 О) n = 180 : 30 = 6 –– С 6 Н 12 О 6 - глюкоза " width="640"
СН 2 О 2) n = М(р-ва) : М(СН 2 О) n = 180 : 30 = 6 –– С 6 Н 12 О 6 - глюкоза " width="640"










































