
Типы химических реакций
в органической химии

Специфические особенности органических реакций
1. Органические реакции идут медленно , часто требуют жёстких условий (температура, давление, участие катализатора).
2. Органические реакции протекают в несколько стадий , из-за чего дают невысокий выход продукта .
3. В органических уравнениях реакций, вместо знака равенства ставится стрелка , на которой записываются условия протекания реакций .
4. В органических реакциях, которые идут в живых организмах, изменению подвергается не вся молекула, а только её часть, так называемые реакционные центры молекулы.

Химическая реакция
Исходные вещества
Продукты реакции
=
Реакционным центром можно считать функциональную группу или кратную связь .
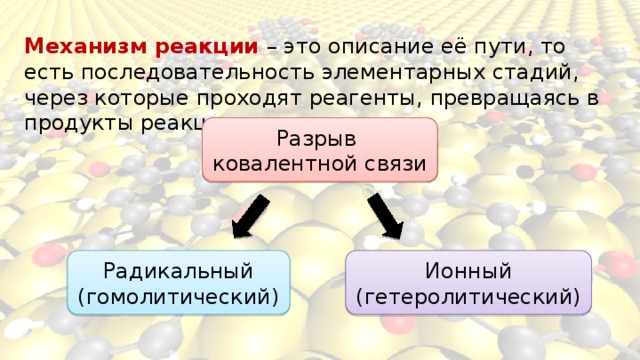
Механизм реакции – это описание её пути, то есть последовательность элементарных стадий, через которые проходят реагенты, превращаясь в продукты реакции.
Разрыв
ковалентной связи
Радикальный
Ионный
(гомолитический)
(гетеролитический)

Радикальный (гомолитический) разрыв ковалентной связи (гомолиз) – от греческого homos – «равный», «одинаковый» и lysis – «растворение», «распад».
В
А
В
А
•
→
+
•
•
•
Радикалы
Радикальному , или гомолитическому разрыву обычно подвергаются неполярные или малополярные ковалентные связи:
С – С , С – Н , Cl – Cl , N – N , Br – Br .
• СН 3
• Сl
• СН 3 СН 2

Радикальный (гомолитический) разрыв ковалентной связи:
Радикалы – это частицы с неспаренными электронами на внешних орбиталях, обладающие высокой реакционной способностью .
температура
свет
радиация

Ионный , или гетеролитический разрыв ковалентной связи (гетерозис) от греческого heteros – «другой», «иной» и lysis – «распад».
А
-
В
+
В
А
→
•
+
•
электрофил
нуклеофил
К гетеролитическому разрыву склонны полярные и легко поляризуемые связи , кроме этого, такому разрыву способствуют и полярные растворители.
CH 3 I → CH 3 + + I -
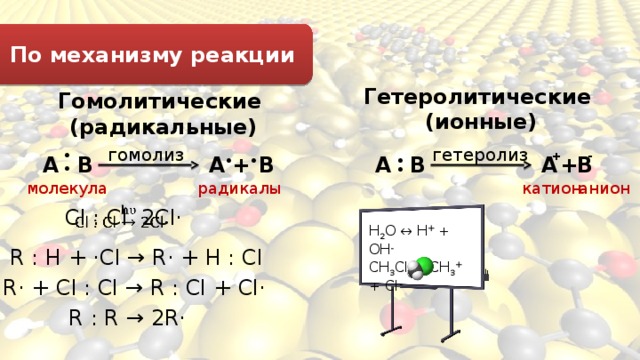
По механизму реакции
Гетеролитические
(ионные)
Гомолитические
(радикальные)
гомолиз
гетеролиз
-
+
•
В
А
В
+
А
А
А
В
В
+
•
•
•
•
•
катион
анион
радикалы
молекула
Сl : Cl 2Cl·
H 2 O ↔ H + + OH -
CH 3 Cl → CH 3 + + Cl -
R : H + ·Cl → R· + H : Cl
R· + Cl : Cl → R : Cl + Cl·
R : R → 2R·

В зависимости от природы атакующего реагента
Электрофильные
Нуклеофильные
Реагент – нуклеофил (предоставляет пару электронов).
Реагент – электрофил (имеет свободную орбиталь).
CH 3 – Br + Na + OH - → CH 3 – OH + Na + Br -
H 2 O, F - , Cl - , Br - , NH 3 , OH - , CN - , RO -
H + , CH 3 + , NO 2 + , ZnCl 2 , AlCl 3
Возрастает сила нуклеофила

По направлению и конечному продукту
Реакции замещения
Протекают с заменой атома или группы атомов на другой атом или группу.
В результате данных реакций образуются два различных продукта.
(элиминирования);
Это реакции галогенирования и нитрирования алканов, этерификации и алкилирования карбоновых кислот.
восстановления.

Реакции замещения
CH 3 – CH 3 + Br 2 → CH 3 – C H 2 Br + HBr
бромэтан
бромоводород
C 2 H 5 Cl + Na OH → C 2 H 5 OH + NaCl
этанол
хлорид натрия
Кат.
C 6 H 6 + Cl 2 → C 6 H 5 Cl + HCl
хлорбензол
хлороводород

Реакции присоединения
– C = C –
– C – C –
– C ≡ C –
– C = C –
Реакции гидрирования – присоединения водорода.
Реакции гидратации – присоединения воды.
Реакции гидрогалогенирования – присоединения
галогеноводородов.

Реакции присоединения
Реакции полимеризации –
это реакции присоединения
CH 2 = CH 2 + Br 2 → CH 2 Br – CH 2 Br
1,2-дибромэтан
CH 2 = CH 2 + HOH CH 3 – CH 2 OH
этанол
CH 3 CH 2 CH 2 CHO + H 2 CH 3 CH 2 CH 2 CH 2 ОН
бутанол-1
n(CH 2 = CH 2 ) (-CH 2 – CH 2 ) n
полиэтилен

Реакции отщепления, или элиминирования
К реакциям отщепления , или элиминирования относятся реакции, в ходе которых происходит отщепление атомов или групп атомов от органических молекул, в результате которых образуются кратные связи .
Реакции дегидрирования – реакции отщепления водорода.
Реакции дегидратации – реакции отщепления воды.
Реакции дегидрогалогенирования – реакции отщепления
галогеноводородов.

Реакции отщепления, или элиминирования
CH 3 – CH 2 – OH СH 2 = CH 2 + H 2 O
этилен
CH 3 – CH 2 – CH 2 Br CH 3 – CH = CH 2 + HBr
пропен
CH 3 CH 2 CH 2 CH 2 Br + NaOH СН 3 CH 2 CH=CH 2 + NaBr + H 2 O
бутен-1
бромид
вода
натрия

Реакции окисления и восстановления
Формула
соединения
Валентность
углерода
IV
IV
IV
IV
Степень
окисления
-4
-2
0
+2
Реакции окисления и восстановления сопровождаются изменением степени окисления атомов углерода , которые являются реакционными центрами .

Реакции окисления и восстановления
+1
+3
CH 3 – CHO CH 3 – COOH
-2
-2
-3
-3
CH 2 = CH 2 + H 2 СН 3 – СН 3








































